L'idée d'une perfusion artificielle revient au physiologiste français Jean-Jacques Le Gallois qui avait perfusé la tête de lapins décapités pour prouver que la circulation du sang maintenait la fonction de l'organe [7]. Le prototype de machine coeur-poumon avec contrôle de la température a été imaginé en 1884 par von Frey et Gruber [10], mais c'est Hooker, en 1915, qui a construit le précurseur des oxygénateurs à film: il s'agissait d'un disque de caoutchouc sur lequel le sang se répandait en un film oxygéné par contact direct avec un flux d'O2 [5]. Ces montages avaient peu de succès, car le sang coagulait très rapidement. En effet, il a fallu attendre la découverte de l'héparine en 1916 et celle de la protamine 20 ans plus tard pour que ce problème soit résolu [9]. Ce n'est qu'en 1937 que John Gibbon créa la première machine de circulation extracorporelle (CEC) complète qui permette la survie d'animaux en laboratoire; l'oxygénateur était un écran à disques rotatifs [3].
Le 5 avril 1951 à Minneapolis, Dennis utilisait pour la première fois une machine de CEC en clinique pour procéder à la correction d'un canal atrio-ventriculaire chez un enfant de 6 ans; ce fut un échec chirurgical [1]. L'année suivante, la deuxième tentative (fermeture de CIA) se solda également par le décès de l'enfant. Mais le 20 mai 1953, à Philadelphie, la machine de Gibbon permit de fermer avec succès une CIA chez un patient de 18 ans au cours d'une CEC de 45 minutes [4]. Pour Gibbon, c'était l'aboutissement de 23 ans de recherche et de conceptions de circuits extracorporels. Il devint ainsi le "père de la CEC" et le premier perfusionniste de l'histoire. Les premiers circuits de CEC étaient encombrants et dangereux; ils demandaient un amorçage de plusieurs litres de sang, et fonctionnaient avec un oxygénateur fait de grands disques plongeant partiellement dans le sang et tournant dans une chambre pleine d'oxygène. Le tout était lavé et réutilisé pour un autre patient. Seuls les tuyaux étaient à usage unique. C'était le cas de la première machine lausannoise, celle de Livio-Mettraux, qui date de 1960 (Figure 1.2).

Figure 1.2: Machine de CEC de Livio-Mettraux, construite à Lausanne en 1960 et utilisée en clinique jusqu'en 1966. Elle contient déjà tous les éléments d'une machine moderne: réservoir veineux, pompe à galet, oxygénateur, échangeur thermique, monitorage. Seuls les tuyaux sont à usage unique; le réservoir veineux, l'oxygénateur et l'échanger thermique sont des systèmes réutilisables. L'oxygénateur est un modèle à disques: une série de disques verticaux tourne sur un axe légèrement incliné et plonge dans le sang qui coule au fond de la cuve cylindrique; le sang emporté à la surface des disques est ainsi exposé à un courant d'oxygène qui traverse de cylindre. La pompe est une pompe à galet très similaire à celles utilisées sur les circuits actuels. Le seul moniteur est un manomètre de pression sur le circuit artériel.
Le problème de l'oxygénateur restait lancinant, car les modèles à disques causaient d'innombrables ennuis et manquaient d'efficacité. Dès 1956, DeWall et Lillehei dessinèrent un système réalisable en plastic et consistant en une chambre où le sang était oxygéné par barbotage de bulles d'oxygène, surmontée d'une chambre de débullage remplie d'un agent anti-mousse et d'un réservoir hélicoïdal [2]. De nouvelles entreprises se lancèrent dans la commercialisation de ces appareils: Bentley™, Travenol™, etc. Le premier appareil de ce type largement utilisé en Europe fut celui de Rygg et Kyvsgaard; c'était un sac de polyéthylène disposable contenant l'ensemble des éléments (Figure 1.3) [8]; il fut très répandu jusqu'à la fin des années soixante-dix parce qu'il était simple, efficace et bon marché.
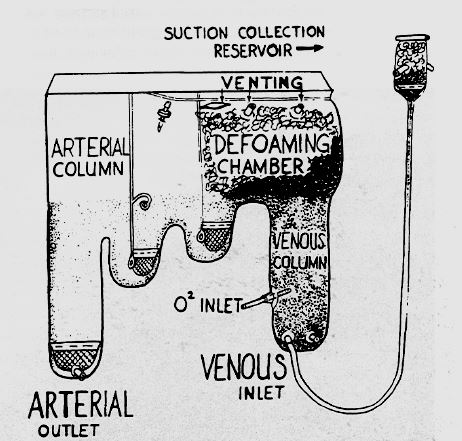
Figure 1.3: Oxygénateur à bulles de Rygg et Kyvsgaard (1956). Le sang veineux est oxygéné par simple barbotage. Une chambre remplie d'anti-mousse assure le débullage. Une cascade de trois petits réservoirs complète l'élimination des bulles et permet le stockage de volume [8].
Mais l'oxygénateur à bulles restait une cause majeure d'embolie gazeuse; de plus, dès que la CEC dépassait une heure, le contact direct du sang avec l'air entraînait une dénaturation protéique et une activation du complément qui étaient la cause d'un syndrome inflammatoire systémique massif et très souvent d'un SDRA, que l'on appelait le pump lung. Comme les membranes de dialyse rénale étaient performantes, l'idée vint de les utiliser pour la diffusion de l'O2 sans que ce dernier soit en contact direct avec le sang. On utilisa des plaques d'éthyl-cellulose, de Teflon™ puis de silicone, arrangées en couches ou en tubules [6]. Bien que les problèmes de contact air-sang soient résolus, les oxygénateurs à membranes ont mis du temps à s'imposer à cause de leur complexité et de leur prix. Actuellement, leurs perfectionnements et leur facilité d'utilisation en font les seuls systèmes utilisés dans les machines de CEC; ils sont inclus en un bloc comprenant l'oxygénateur, le réservoir veineux et l'échangeur thermique (Figure 1.4).

Figure 1.4: L'oxygénateur de CEC. Il est en général couplé au réservoir veineux et à l'échangeur thermique par le fabriquant. A: corps de l'oxygénateur contenant les microfibres pour les échanges gazeux. B: sang veineux en provenance du réservoir via la pompe. C: sang artériel sortant de l'oxygénateur. D: arrivée des gaz (avec filtre micropore). E: échangeur thermique. F: tuyaux pour la circulation de l'eau de refroidissement / réchauffement.
A l'exception de la pompe, tous les éléments de la CEC sont maintenant à usage unique. Le circuit comprend également de nombreux systèmes de sécurité qui n'existaient pas sur les premiers modèles: moniteur de bulles, filtres artériels et veineux, monitorage de SaO2 et de SvO2, asservissement de la pompe au niveau du réservoir, etc. Les travaux actuels portent essentiellement sur l'amélioration de la biocompatibilité des surfaces de contact et sur la miniaturisation de tout le système (voir Chapitre 7, Machines et circuits).
| Histoire de la CEC |
|
La circulation extra-corporelle (CEC) en quelques dates: - 1953: première réussite d'une fermeture de CIA en CEC
- 1956: oxygénateur à bulle
- 1967: oxygénateur à membrane
- 2000: mini-CEC
|
© CHASSOT PG Avril 2007 Mise à jour Janvier 2012, Juillet 2017
Références
- DENNIS C, SPRENG DS, NELSON GE, et al. Development of a pump-oxygenator to replace the heart and lung: An apparatus applicable to human patients and an application to one case. Ann Surg 1951; 134:709-21
- DEWALL RA, WARDEN HE, GOTT VL, et al. Total body perfusion for open cardiotomy using bubble oxygenator. J Thorac Surg 1956; 32:591-603
- GIBBON JH. Artificial maintenance of circulation during experimental occlusion of the pulmonary artery. Arch Surg 1937; 34:1105-31
- GIBBON JH. Application of the mechanical heart and lung apparatus to cardiac surgery. Minn Med 1954; 36:171-85
- HOOKER DR. The perfusion of the mammalian medulla: The effect of calcium or potassium on the respiratory and cardiac centers. Am J Physiol 1915; 38:200-8
- LANDE AJ, DOS SJ, CARLSON RG, et al. A new membrane oxygenator dialyser. Surg Clin N Am 1967; 47:1461-70
- LE GALLOIS JC. Expériences sur le principe de la vie, notamment sur le siège de ce principe. Paris, D'Hautel 1812
- RYGG IH, KYVSGAARD E. A disposable polyethylene oxygenation system applied in the heart/lung machine. Acta Chir Scand 1956; 112:433-7
- STAMMERS AH. Historical aspects of cardiopulmonary bypass: From antiquity to acceptance. J Cardiothorac Vasc Anesth 1997; 11:266-74
- VON FREY M, GRUBER M. Ein respirations-apparat für isolierte organe. Arch Physiol 1885; 9:519-32
