Il est difficile de mettre en évidence cliniquement une insuffisance diastolique. Il s'agit avant tout d'un diagnostic de présomption basé sur la présence de dyspnée. On ne peut l'objectiver que par une échocardiographie, une ventriculographie ou une IRM. Comme cette notion est importante pour la prise en charge hémodynamique périopératoire des patients chirurgicaux, il faut garder à l'esprit les situations dans lesquelles la diastole est très probablement perturbée [5,8].
- Age : nouveau-né, vieillard;
- Hypertrophie ventriculaire gauche concentrique: HTA, sténose aortique;
- Ischémie, infarctus étendu, ischémie à l'effort;
- Insuffisance cardiaque systolique;
- Dilatation ventriculaire;
- Hypertrophie ventriculaire droite: pneumopathies chroniques;
- Cardiomyopathie restrictive;
- Œdème myocardique : post-CEC, rejet de transplant;
- Pathologie péricardique.
L’insuffisance diastolique représente 40% des cas d’insuffisance cardiaque congestive ; elle est caractérisée par une stase et une dyspnée, mais une fonction systolique conservée (FE > 0.5) [5,7]. La dysfonction diastolique est un facteur pronostique de mortalité (HR 1.78) indépendant de la fonction systolique [1].
Comme il n’est pas possible de construire la courbe de compliance avec les données cliniques habituelles, la surveillance de la fonction diastolique se restreint à observer trois éléments :
- Relation de la pression artérielle et du volume systolique avec le remplissage;
- PVC et PAP ;
- Indices échocardiographiques de la performance diastolique des ventricules.
La courbe de Frank-Starling étant très redressée en cas d’insuffisance diastolique, les patients sont très sensibles aux variations de précharge (voir Figure 6.47). Une hypovolémie ou une augmentation de la pression intrathoracique provoquent une baisse du volume éjecté, donc de la pression artérielle. Les variations de la PAsyst avec le cycle ventilatoire du respirateur sont plus amples que normalement.
Les pressions de remplissage (PVC et PAPO) sont supérieures à la norme pour le même volume télédiastolique parce que la courbe de compliance est déplacée vers le haut. D’autre part, la courbe est redressée et présente une pente moyenne supérieure à celle de la courbe normale (Figure 6.16) [8]. De ce fait, il existe une bonne cohérence entre la pression et le volume de remplissage, même si elle n’est pas linéaire. La PVC et la PAPO sont donc très utiles pour le suivi du remplissage de ces patients. Les malades en insuffisance diastolique sévère avec fonction systolique conservée présentent une stase pulmonaire chronique ; dans ces cas, la PAPO est de première importance pour la gestion des perfusions.
Indices échocardiographiques
Les seuls indices de fonction diastolique qui soient pratiques en clinique sont fournis par l’échocardiographie. La diastole est divisée en 4 périodes, comme l’illustre l’image ETO du flux mitral (Figure 6.68).
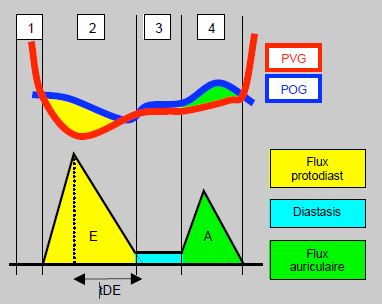
Figure 6.68 : Phases de la diastole. 1: phase de relaxation isovolumétrique (tRI). 2: phase de relaxation active, flux mitral E. 3: diastasis. 4: contraction auriculaire, flux mitral A. La partie supérieure de l'image représente les gradients de pression instantanés entre le le VG (courbe rouge) et l'OG (courbe bleue). La phase de flux protodiastolique (relaxation active) est représentée en jaune, le diastasis (équilibre des pressions OG – VG) en bleu et la phase de contraction auriculaire (distensibilité) en vert.
- Relaxation isovolumétrique;
- Remplissage protodiastolique (relaxation active), flux mitral E;
- Diastasis (remplissage passif);
- Contraction auriculaire, flux mitral A.
La dysfonction diastolique évolue en trois phases, qui sont définies par la silhouette du flux mitral, par celle du flux dans les veines pulmonaires et par la vélocité de déplacement de l’anneau mitral (Figure 6.69) [3,4].
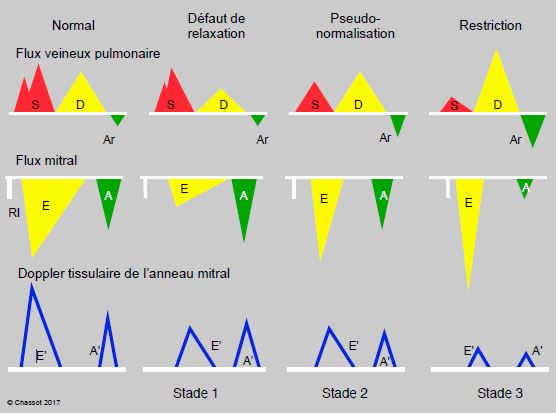
Figure 6.69 : Modifications du flux veineux pulmonaire, du flux mitral et de la vélocité de l’anneau mitral selon l'évolution de la dysfonction diastolique. Stade I, défaut de relaxation : allongement de la phase de relaxation isovolumétrique (tRI > 220 msec), diminution de vélocité du flux mitral E, augmentation de la contribution auriculaire (flux A ↑). Peu de modification sur le flux veineux pulmonaire. Diminution de la vélocité de l’anneau mitral (E' et A'). Stade 2, pseudo-normalisation : l'augmentation progressive de la pression auriculaire gauche rétablit le gradient de pression OG – VG; la vélocité du flux E augmente et retrouve sa valeur normale, mais sa morphologie est pathologique: pente d'accélération et de décélération accentuée (tDE < 150 msec), raccourcissement de la relaxation isovolumétrique (tRI < 200 msec). La composante S du flux veineux pulmonaire diminue parce que la POG augmente. Diminution de la vélocité de l’anneau mitral E'. Stade 3, restriction : c'est la situation la plus grave; le ventricule devient tellement rigide et la pression auriculaire tellement haute que la vélocité du flux E devient très élevée et sa décélération très brutale (tDE < 100 msec); l'onde A de la contraction auriculaire est minime parce que le ventricule n'est plus distensible en fin de diastole. La composante S du flux veineux pulmonaire est minime, le remplissage auriculaire a lieu en diastole, le reflux dû à la contraction auriculaire augmente car le VG n’est pas distensible et la vidange de l'OG par la mitrale est minime. La vélocité de l’anneau mitral (E' et A') est infime.
- Défaut de relaxation protodiastolique, caractéristique du vieillissement, de l’hypertrophie ventriculaire (hypertension artérielle, sténose aortique), de l’ischémie, de la dilatation, de l’obésité et du syndrome d’apnée du sommeil ; c'est un trouble fréquent et bénin. Le flux E diminue, et la proportion du remplissage diastolique dû à la systole auriculaire, normalement de 20%, augmente considérablement ; sa contribution va jusqu'à 50%.
- Pseudo-normalisation : l'augmentation progressive de la pression auriculaire gauche rétablit le gradient de pression OG – VG, mais la morphologie des flux est pathologique.
- Restriction par non-compliance ventriculaire, caractéristique des cardiomyopathies restrictives, des infiltrations (collagénoses, amyloïdose) et de la péricardite. Il s'agit d'une situation sévère conduisant à la stase et à l’oedème pulmonaire, même si la fonction systolique est conservée. On rencontre le même phénomène dans la dilatation ventriculaire massive, dans le rejet après transplantation ou dans l’oedème myocardique post-CEC.
Les indices échocardiographiques sont décrits en détail dans le Chapitre 25 (Fonction diastolique). Comme ils sont très nombreux, on ne mentionnera ici que deux d’entre eux [2,3,6].
- Dilatation de l’OG, (> 40 mL/m2), bombement du septum interauriculaire dans l’OD (Figure 6.70).
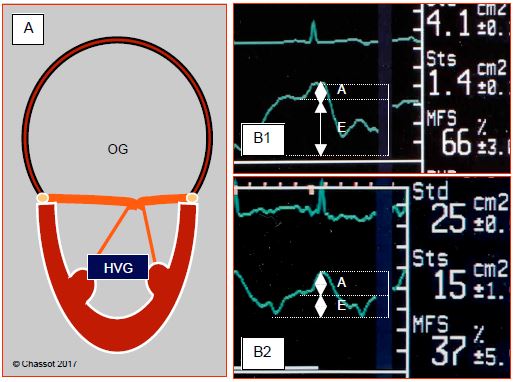
Figure 6.70 : Dysfonction diastolique, images bidimensionnelles. A : dilatation de l’OG (> 30 mL/m2, diamètre > 5 cm, POG > 16 mmHg) ; le septum interauriculaire bombe dans l’OD, le VG est hypertrophié (HVG). B : Evolution de la surface ventriculaire gauche au cours du cycle cardiaque par la technique Automated Border Detection™. B1: VG normal; l'accroissement de surface diastolique due à la contraction auriculaire (A) est de l'ordre de 20% (flèche), celui dû au remplissage E est de 80%. B2: dysfonction diastolique; l'accroissement de surface télédiastolique est dû pour la moitié à la contraction de l'oreillette.
- Rapport entre la vélocité du flux mitral E et celle de l’anneau mitral E’ ; il permet de différencier l’effet respectif de la précharge et du défaut de relaxation. Lorsqu’il est bas (E/E' < 8), la relaxation et le remplissage sont normaux, et la PAPO est basse. S’il est > 15, la PAPO est > 18 mmHg (r = 0.82) (Figure 6.71) [2,3].
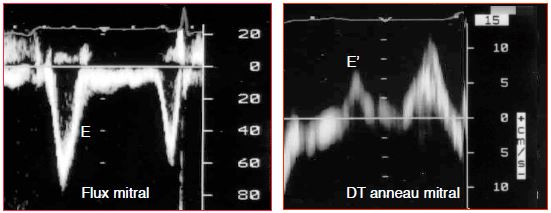
Figure 6.71 : Evaluation non-invasive d’une élévation de la pression auriculaire gauche par le rapport entre la vélocité du flux mitral E et celle du déplacement de l’anneau mitral E’ au Doppler tissulaire (DT). Lorsque ce rapport E/E’ est > 15, la PAPO est > 18 mmHg [2,3].
| Evaluation de la fonction diastolique du VG |
|
Environ 40% des insuffisances cardiaques congestives caractérisées par une stase et une dyspnée sont des insuffisances diastoliques à fonction systolique conservée (FE > 0.5). L'insuffisance diastolique est fréquente en cas de: âge avancé, HVG concentrique, ischémie, dilatation VG/VD, HVD, nouveau-né. Elle est pathognomonique de: infiltrations (fibrose, œdème), cardiomyopathie restrictive, restriction péricardique, œdème post-CEC.
Impact hémodynamique en clinique:
- Pression de remplissage élevée (PVC, PAPO ↑)
- Dépendance accentuée de la précharge, intolérance à l'hypovolémie
- Intolérance à la bradycardie et à la tachycardie
- Dépendance du rythme sinusal
Indices échocardiographiques signant une augmentation de la POG (parmi de nombreux autres):
- Dilatation de l’OG
- Rapport E/E’ > 15
|
© CHASSOT PG Août 2010, dernière mise à jour Août 2017
Références
- AL JAROUDI W, ALRAIES C, HALLEY C, et al. Impact of progression of diastolic dysfunction on mortality in patients with normal ejection fraction. Circulation 2012 ; 125 :782-8
- ARQUES S, ROUX E, LUCCIONI R. Current clinical applications of spectral tissue Doppler echocardiography (E/E’ ratio) as a noninvasive surrogate of left ventricular diastolic pressures in the diagnosis of heart failure with preserved left ventricular systolic function. Cardiovasc Ultrasound 2007; 5:16
- NAGUEH SF, SMISETH OA, APPLETON CP, et al. Recommendations for the evaluation of left ventricular diastolic function by echocardiography: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr 2016; 29:277-314
- PAULUS WJ, TSCHÖPE C, SANDERSON JE, et al. How to diagnose diastolic heart failure: a consensus statement on the diagnosis of heart failure with normal left ventricular ejection fraction by the Heart Failure and Echocardiography Associations of the European Society of Cardiology. Eur Heart J 2007; 28:2539-50
- REDFIELD MM. Heart failure with preserved ejection fraction. N Engl J Med 2016; 375:1868-77
- SKUBAS N. Intraoperative Doppler Tissue imaging is a valuable addition to cardiac anesthesiologist’s armamentarium: A core review. Anesth Analg 2009; 108:48-66
- VASAN RS, LARSON MG, BENJAMIN EJ, et al. Congestive heart failure in subjects with normal versus reduced left ventricular ejection fraction: prevalence and mortality in a population-based cohort. J Am Coll Cardiol 1999; 33:1948-55
- ZILE MR, BRUTSAERT DL. New concept in diastolic dysfunction and diastolic heart failure: Part I. Diagnosis, prognosis, and measurement of diastolic function. Circulation 2002; 105:1387-93
