Un certain nombre de conditions sont requises pour sevrer le patient de la CEC (Figure 7.45 et Tableau 7.7) [1].
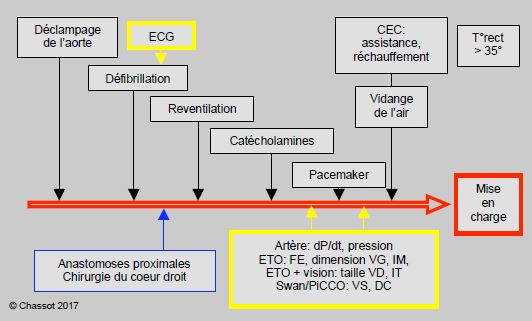

Figure 7.45 ; Enchaînement des évènements et des actions anesthésiques conduisant à la mise en charge. Les éléments de monitorage sont cadrés en jaune et les évènements chirurgicaux en bleu.

- Patient uniformément réchauffé; la T° rectale doit être ≥ 35°C, la température oesophagienne ≥ 36°C.
- Poumons ré-expandus par des manoeuvres de capacité vitale (insufflations manuelles à 30-40 cm H2O pendant 20-30 secondes), en veillant à ne pas interférer avec les manœuvres dans le champ opératoire ni à distendre le greffon mammaire [4].
- Ventilation efficace; la FiO2 est réglée de manière à assurer une SpO2 > 98%, contrôlée par une gazométrie (PaO2 ≥ 100 mmHg); la ScO2 (NIRS) est également un repère efficace. Une FiO2 excessive peut aggraver les lésions de reperfusion myocardiques. La ventilation est reprise lorsque le coeur est reperfusé, c'est-à-dire après déclampage de l'aorte et la reprise d'un rythme cardiaque spontané, ou après la revascularisation par les pontages aorto-coronariens. La ventilation doit parfois être interrompue parce que les poumons envahissent le champ opératoire et gènent le chirurgien.
- Au début de la reventilation, la pression dans les voies aériennes peut être momentanément élevée et la bronchoconstriction conduire à un air-trapping. Ceci est lié au collapsus pulmonaire, aux atélectasies et au relargage de substances bronchoactives. Il est important de reventiler assez tôt pour que ce phénomène se soit dissipé au moment de la mise en charge [2].
- Sommeil assuré par un agent intraveineux (propofol, midazolam) et arrêt des halogénés si la fonction ventriculaire est réduite. Même une faible concentration d'halogéné peut avoir des effets néfastes au moment critique de la mise en charge. L'halogéné utilisé en CEC devrait être arrêté 10-15 minutes avant la mise en charge pour être certain que son effet vasodilatateur et inotrope négatif a disparu.
- Analgésie: adjonction d'une dose du fentanil choisi pour le cas. L’administration de 10 mg de morphine en fin de CEC assure une analgésie pour le début de la phase postopératoire et minimise les risques de dépression respiratoire par rapport à une injection plus proche du réveil. Pour les cas en circuit rapide, l'infiltration sternale et les blocs intercostaux pratiqués à la fermeture sont préférables. La dexmédétomidine (0.2-1.0 mcg/kg/heure) a des effets à la fois analgésiques et sédatifs [5]; elle tend à devenir une mesure de routine dès la fin de la CEC.
- Rythme sinusal à 75-90 batt/min; cardioversion (10-20 joules) en cas de fibrillation auriculaire. Défibrillations itératives (20-50 J) en cas d'épisodes répétitifs de fibrillation ventriculaire. Stabilisation du rythme par de l'amiodarone (Cordarone® 150 mg iv lent). Il peut arriver que l'on doive défibriller 10-20 fois de suite lors de lésions de reperfusion, mais la récupération est complète à long terme (ne jamais abandonner !).
- Fils de pace-maker ventriculaires en place et fonctionnels (pace-maker testé). Stimulation électrique ventriculaire à 75 batt/min en cas de bloc AV ou de bradycardie. Si le rythme est trop lent, le VG n'éjecte pas au fur et à mesure le sang qui le remplit par la circulation bronchique ou une insuffisance aortique; il risque de se dilater dangereusement. En attendant le pace-maker, l'opérateur peut déclencher mécaniquement des ESV régulières avec un instrument métallique.
- PAM > 60 mmHg et < 120 mmHg; dans le cas contraire, régler d'abord le problème hémodynamique.
- Valeurs de PAP correspondant aux valeurs préopératoires, ou plus basses.
- En utilisant la formule du calcul des résistances, on peut facilement évaluer si le malade est vasoconstricté ou vasoplégique, puisque la PVC est la pression ambiante (PVC = 0) et le débit cardiaque est celui de la pompe (DP = débit de pompe). Donc : RAS = (PAM • 80) / DP [3].
- Courbe d'AP sur le tracé du cathéter de Swan-Ganz, ballonnet dégonflé; il est impératif de ne jamais gonfler le ballonnet du cathéter sans avoir une courbe claire d’artère pulmonaire. Le gonfler alors que l'extrémité du cathéter est en position bloquée provoquerait une rupture artérielle et une hémorragie pulmonaire massive chez un patient encore hépariné.
- Volémie adéquate (volume dans le réservoir de CEC), degré de remplissage du VD dans le champ opératoire.
- Vidange adéquate de l'air qui a pu s'introduire dans le coeur gauche (contrôle ETO).
- Contrôle de la kaliémie (< 6 mmol/L); un bolus de Ca2+ contrecarre les effets de l'hyperkaliémie, mais peut induire un spasme artériel, notamment du greffon mammaire. Autres moyens d'abaisser la kaliémie: hémofiltration, perfusion insuline/glucose, diurétique.
- Contrôle de l'équilibre acido-basique, de la glycémie (< 10 mmol/L) et du taux d'Hb (> 60 g/L); traiter selon besoin avant la mise en charge.
- Status coagulatoire: ACT, ROTEM™ (Fibtem, Heptem), éventuellement thrombocytes [6].
- ETO: débullage efficace; contractilité ventriculaire droite et gauche, cinétique segmentaire normale pour le cas, volume des cavités et éventuelle insuffisance valvulaire correspondant aux images attendues en fonction de la pathologie [3].
- Catécholamine et/ou autre agent inotrope choisi administré sur la voie centrale (ou OD de la Swan-Ganz) 5-10 minutes avant la mise en charge.
- Perfusions rétablies et voies veineuses fonctionnelles.
- Alarmes fonctionnelles et volume sonore rétabli; zéro des capteurs vérifié.
- A disposition selon besoins probables: poches de sang, fibrinogène, facteurs de coagulation, thrombocytes.
| Contrôles avant la mise en charge |
|
Patient normotherme (T° rectale ≥ 35°, T° oeso ≥ 36°) et ventilé (FiO2 pour SpO2 > 98% et PaO2 > 100 mmHg), poumons ré-expandus
Sommeil, analgésie et curarisation assurés
ECG satisfaisant
Activité cardiaque spontanée, rythme sinusal ou électro-entraîné; défibrillation/cardioversion si nécessaire
Pace-maker (fils ventriculaires) en place et testé
Cavités gauches débullées
ETO : fonction ventriculaire, insuffisance mitrale/tricuspide, contractilité segmentaire, volémie
Agent(s) inotrope(s) choisi(s) : perfusion en marche
Retrait du cathéter de Swan-Ganz pour obtenir une courbe d’AP avant de gonfler le ballonnet
PAM, PAP, RAS, SvO2, Ht, lactate, électrolytes, glycémie : dans les limites acceptables selon le cas
Zéro des lignes de pression vérifié, alarmes rétablies sur le moniteur
|
© CHASSOT PG, GRONCHI F, Avril 2008, dernière mise à jour, Avril 2018
Références
- BARRY AE, CHANEY MA, LONDON MJ. Anesthetic management during cardiopulmonary bypass: a systematic review. Anesth Analg 2015; 120:749-69
- BAUFRETON C, MOREAU X, CORBEAU JJ, et al. Déroulement de la CEC standard et avec les nouveaux dispositifs consommables. In: JANVIER G, LEHOT JJ (ed). Circulation extracorporelle: principes et pratique, 2ème édition. Paris, Arnette Groupe Liaison SA, 2004, pp 113-45
- DENAULT AY, BUSSIERES J, CARRIER M, et al. The importante of difficult separation from cardiopulmonary bypass: the Montreal and Quebec Heart Institute experience. Exp Clin Cardiol 2006; 11:37
- MAGNUSSON L, ZEMGULIS V, RENLING A, et al. Use of a vital capacity maneuver to prevent atelectasis after cardiopulmonary bypass. Anesthesiology 1998; 88:134-42
- SCHNABEL A, MEYER-FRIEBEM C, REICHL S, et al. Is intraoperative dexmedetomidine a new option for postoperative pain treatment ? A meta-analysis of randomized controlled trials. Pain 2013; 154: 1140-9
- WEBER CF, GÖRLINGER K, MEININGER D. Point-of-care testing : a prospective randomized clinical trial of efficacy in coagulopathic cardiac surgery patients. Anesthesiology 2012 ; 117 : 531-47
