Transducteurs
Le transducteur est composé de 128 à 256 cristaux piézo-électriques de zirconate-titanate de plomb ; il y en a jusqu’à 3'200 dans les sondes tridimensionnelles. Ces cristaux fonctionnent comme des convertisseurs d’énergie électrique – mécanique.
Le transducteur est composé de 128 à 256 cristaux piézo-électriques de zirconate-titanate de plomb ; il y en a jusqu’à 3'200 dans les sondes tridimensionnelles. Ces cristaux fonctionnent comme des convertisseurs d’énergie électrique – mécanique.
- Lorsqu’ils sont stimulés par un courant électrique, ils changent de forme et émettent des US en fonction de leur fréquence vibratoire;
- Lorsqu’ils sont heurtés par des US, ils émettent un courant électrique correspondant.
Une rangée de cristaux émet un front d’onde qui lui est parallèle et n’explore que la tranche de tissu qui lui fait face. Afin de balayer un large secteur, on peut faire tourner les cristaux mécaniquement, ce qui était la première technique utilisée, ou stimuler chacun des cristaux dans un ordre tel que le front d’onde est oblique, ce qui est la technique actuelle (système à décalage de phase ou phased-array). En variant constamment la séquence de stimulation des capteurs, on peut ainsi balayer le secteur sans rotation mécanique du capteur (Figure 25.4). On peut utiliser le même procédé pour créer une focalisation en émettant et en réceptionnant les échos des capteurs extérieurs avant ceux des capteurs intérieurs, de manière à avoir un front d’onde concave [2,3].
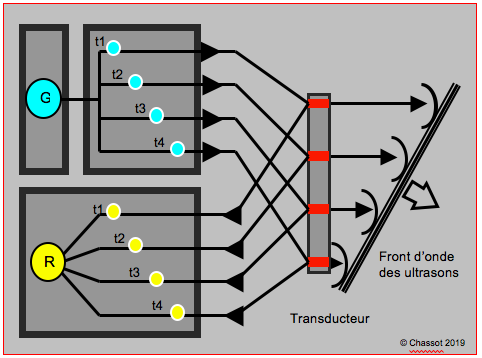
Figure 25.4 : Fonctionnement d’un transducteur à décalage de phase (phased-array). Le générateur (G) émet une stimulation électrique décalée des cristaux émetteurs-capteurs aux temps t1, t2, t3 et t4, ce qui fait que le front d’onde est oblique par rapport au plan du transducteur sur lequel sont alignés les cristaux. Ce décalage est réglé par un chronomètre électronique; il est de l'ordre de 10 nanosecondes. Le même décalage à la réception (R : récepteur) permet de reconstruire l’image. En variant l’ordre de stimulation et de réception des cristaux, le transducteur balaye électroniquement le secteur.
Comme les US émis ont tendance à diverger progressivement, il est impératif de focaliser les rayons sur la zone que l’on veut examiner, parce que les rayons sont parallèles et concentrés dans la zone focale, donnant ainsi une image plus précise et mieux définie. Il existe donc trois zones dans un faisceau d'ultrasons: la zone convergente proximale, la zone focale et la zone divergente distale (Figure 25.5). L’ajustement de la zone focale se fait en déplaçant de petits repères situés sur les bords de l’écran. Le meilleur réglage est de placer le point focal au niveau ou juste au-delà de la structure à examiner, de manière à ce que cette dernière soit dans la partie proximale du faisceau [1].
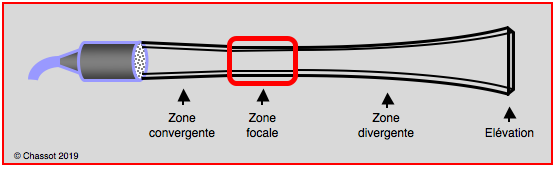
Figure 25.5 : Représentation d'un faisceau d'ultrasons, avec ses trois zones: la zone convergente proximale, la zone focale et la zone divergente distale. Dans la troisième dimension, ce faisceau représente une fine lame caractérisée par son épaisseur ou élévation, qui est négligeable dans l'imagerie bidimensionnelle mais devient aussi importante que la largeur du faisceau en imagerie tri-dimensionnelle. Dans la zone focale, les rayons sont parallèles et concentrés, l'énergie et la précision sont maximales.
Alors que le plan de coupe est obtenu par le balayage électronique au sein du faisceau d'ultrason, la rotation de ce plan de coupe par la rotation mécanique du transducteur lui-même au moyen d’un moteur électrique permet un balayage sur 180° dans l'espace; c'est le principe des sondes multiplan (Figures 25.6).
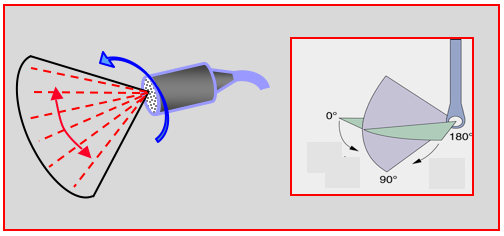
Figure 25.6 : Plans de coupe en mode bi-dimensionnel. Le plan de coupe est une tranche triangulaire de 30-90° selon le degré d'ouverture choisi (en vert pâle); il est réalisé par le balayage électronique des faisceaux d'ultrason (lignes traitillées rouges, double flèche rouge). Ce plan est orienté dans l'espace par la rotation du transducteur sur 180° au sein de la sonde (flèche bleue); le plan de référence à 0° est horizontal.
La fréquence d'émission propre du transducteur (2-15 MHz) est déterminante pour le rendu de l'image. Une fréquence élevée garantit une meilleure résolution spatiale mais une plus faible pénétration en profondeur, alors qu'une fréquence basse offre des propriétés inverse. Les transducteurs montés actuellement sur les sondes ETO sont à fréquences multiples (4-9 MHz, par exemple), ce qui permet d'ajuster l'émission en fonction du type d'examen. La recherche d'une lésion mitrale (située à 4-5 cm de la sonde) sera plus fructueuse avec une fréquence élevée, alors que l'exploration de l'apex d'un VG dilaté (visible à 15-20 cm) sera plus adéquate avec une fréquence basse.
Cadences de travail
L'échocardiographe émet un train de quelques ondes ultrasonores (packet size) de fréquence déterminée (4-8 MHz), puis attend l’écho en retour. En analysant le temps mis par le train d’onde émis pour revenir au transducteur, l’appareil détermine la profondeur de l’objet sur lequel se sont réfléchies les ondes selon la formule : Δt = 2 D / c. La vitesse de déplacement des US étant une constante qui ne dépend que du milieu (c = 1'540 m/s dans les tissus), il est facile de déterminer la distance de la cible qui représente le temps mis pour l’aller-retour (Δt) au transducteur (Figure 25.7). Celui-ci émet pendant 1-2 μsec, et reçoit pendant 250 μsec; il passe donc plus de 99% de son temps de travail en écoute.
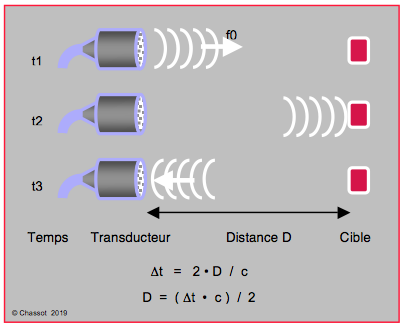
Figure 25.7 : Le transducteur émet un paquet d’ondes ultrasonores (temps t1) qui est réfléchi par une structure échodense (cible, temps t2) et revient en direction de sa source qu’il atteint au temps t3. Comme la vitesse de déplacement des ultrasons (c) est une constante qui ne dépend que du milieu (1'540 m/s dans les tissus du corps), le temps d’un aller-retour du paquet d’ondes (Δt) permet de calculer la distance (D) entre le transducteur et la cible, donc la profondeur de l’objet dans le corps. Plus la distance est grande, plus le temps pour obtenir une image de la cible est long. La fréquence d’analyse de l’appareil diminue donc lorsqu’il examine des images profondes.
Afin de donner une image cohérente à l’écran, la machine met en mémoire les échos les plus proximaux en attendant le retour des échos les plus lointains (profondeur maximale) et n’affiche une image que lorsqu’elle a la totalité des échos. Plus la profondeur est grande, plus la cadence ralentit, car le temps d'attente est de 13 μsec par cm; il est donc important d'ajuster en permanence la profondeur de lecture à l'écran pour la limiter à la zone d'intérêt. La cadence d’émission et de réception est de 1'000 à 6'000 cycles par seconde. C’est la fréquence de travail de la machine, ou fréquence de récurrence (Pulse Repetition Frequency, PRF). Cette fréquence est fonction de plusieurs paramètres. Elle augmente dans trois circonstances [4].
Les cadences élevées ne sont pas utiles pour la représentation des images à l’écran, parce que notre œil ne voit pas de différence au-delà de 35 images/s (les écrans sont souvent limités à cette valeur), mais elles sont nécessaires à l’enregistrement digital pour certaines fonctions comme le Doppler tissulaire ou le speckle-tracking (voir Technologies particulières). Un cycle cardiaque représente un poids de 5 à 500 Mo selon la quantité de données enregistrées (image tri-dimensionnelle, flux couleur, etc).
Traitement électronique
L’information reçue du transducteur subit une série de manipulations informatiques avant et après être acquise dans le processeur central de la machine. On parle de Preprocessing et de Postprocessing. Ceci correspond à une série de réglages qui sont des plus importants pour obtenir une image satisfaisante et exclure un certain nombre d’artéfacts (Figure 25.8) [2.3]. Une partie de ces réglages est automatisées dans les appareils récents sous forme d'une optimalisation électronique des conditions de réception des ultrasons.
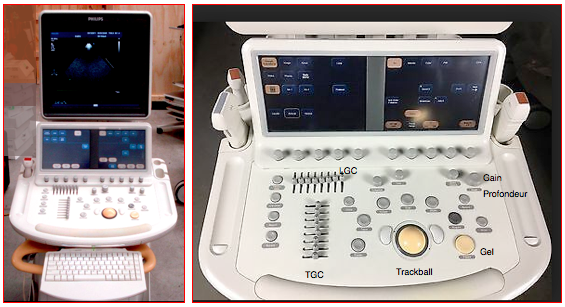
Figure 25.8 : Exemple du panneau de réglages et de l'écran des programmes d'un appareil d'écho-cardiographie. La rangée de boutons située sous l'écran permet de choisir et d'actionner les programmes qui y figurent. Les boutons situés autour de la boule (trackball) commandent les modalités principales (Doppler, couleur, mode TM, curseur, enregistrement, etc). LGC: lateral gain compensation. TGC: time-gain compensation.
Le Preprocessing comprend plusieurs éléments qui sont ajustés avant l'émission des ultrasons.
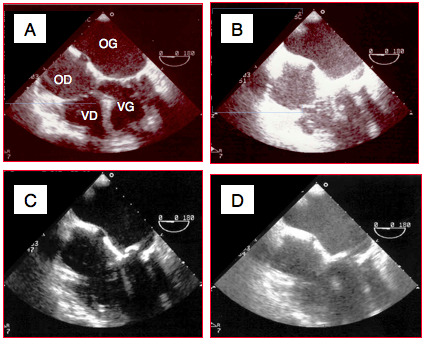
Figure 25.9 : Effets du gain et de la compression sur le rendu d'une même image à l'écran (vue 4-cavités 0°). A: gain et compression normaux. B: excès de gain; le contraste noir-blanc est violent, les structures fines ont disparu. C: faible compression; le contraste noir-blanc est accentué par manque de nuance dans les gris. D: excès de compression; le niveau des gris est trop élevé, le degré de contraste est trop faible pour distiguer des structures fines.
Trois manœuvres particulières de postprocessing sont très utiles en cours d'examen.
© CHASSOT PG, BETTEX D. Mars 2011, Avril 2019; dernière mise à jour, Mars 2020
Références

Figure 25.4 : Fonctionnement d’un transducteur à décalage de phase (phased-array). Le générateur (G) émet une stimulation électrique décalée des cristaux émetteurs-capteurs aux temps t1, t2, t3 et t4, ce qui fait que le front d’onde est oblique par rapport au plan du transducteur sur lequel sont alignés les cristaux. Ce décalage est réglé par un chronomètre électronique; il est de l'ordre de 10 nanosecondes. Le même décalage à la réception (R : récepteur) permet de reconstruire l’image. En variant l’ordre de stimulation et de réception des cristaux, le transducteur balaye électroniquement le secteur.
Comme les US émis ont tendance à diverger progressivement, il est impératif de focaliser les rayons sur la zone que l’on veut examiner, parce que les rayons sont parallèles et concentrés dans la zone focale, donnant ainsi une image plus précise et mieux définie. Il existe donc trois zones dans un faisceau d'ultrasons: la zone convergente proximale, la zone focale et la zone divergente distale (Figure 25.5). L’ajustement de la zone focale se fait en déplaçant de petits repères situés sur les bords de l’écran. Le meilleur réglage est de placer le point focal au niveau ou juste au-delà de la structure à examiner, de manière à ce que cette dernière soit dans la partie proximale du faisceau [1].

Figure 25.5 : Représentation d'un faisceau d'ultrasons, avec ses trois zones: la zone convergente proximale, la zone focale et la zone divergente distale. Dans la troisième dimension, ce faisceau représente une fine lame caractérisée par son épaisseur ou élévation, qui est négligeable dans l'imagerie bidimensionnelle mais devient aussi importante que la largeur du faisceau en imagerie tri-dimensionnelle. Dans la zone focale, les rayons sont parallèles et concentrés, l'énergie et la précision sont maximales.
Alors que le plan de coupe est obtenu par le balayage électronique au sein du faisceau d'ultrason, la rotation de ce plan de coupe par la rotation mécanique du transducteur lui-même au moyen d’un moteur électrique permet un balayage sur 180° dans l'espace; c'est le principe des sondes multiplan (Figures 25.6).

Figure 25.6 : Plans de coupe en mode bi-dimensionnel. Le plan de coupe est une tranche triangulaire de 30-90° selon le degré d'ouverture choisi (en vert pâle); il est réalisé par le balayage électronique des faisceaux d'ultrason (lignes traitillées rouges, double flèche rouge). Ce plan est orienté dans l'espace par la rotation du transducteur sur 180° au sein de la sonde (flèche bleue); le plan de référence à 0° est horizontal.
La fréquence d'émission propre du transducteur (2-15 MHz) est déterminante pour le rendu de l'image. Une fréquence élevée garantit une meilleure résolution spatiale mais une plus faible pénétration en profondeur, alors qu'une fréquence basse offre des propriétés inverse. Les transducteurs montés actuellement sur les sondes ETO sont à fréquences multiples (4-9 MHz, par exemple), ce qui permet d'ajuster l'émission en fonction du type d'examen. La recherche d'une lésion mitrale (située à 4-5 cm de la sonde) sera plus fructueuse avec une fréquence élevée, alors que l'exploration de l'apex d'un VG dilaté (visible à 15-20 cm) sera plus adéquate avec une fréquence basse.
| Transducteur |
| Le transducteur situé à l'extrémité de la sonde d'échocardiographie est un ensembe de cristaux piézo-électriques qui ont la particularité de convertir une stimulation électrique en une émission d'ultrason, et inversement de convertir une réception d'ultrason en courant électrique. Ils émettent les ultrasons dans un plan triangulaire (90°) par balayage électronique (phased array). Le transducteur tourne sur lui-même de 180° pour réaliser divers plans de coupe (sonde multiplan). |
Cadences de travail
L'échocardiographe émet un train de quelques ondes ultrasonores (packet size) de fréquence déterminée (4-8 MHz), puis attend l’écho en retour. En analysant le temps mis par le train d’onde émis pour revenir au transducteur, l’appareil détermine la profondeur de l’objet sur lequel se sont réfléchies les ondes selon la formule : Δt = 2 D / c. La vitesse de déplacement des US étant une constante qui ne dépend que du milieu (c = 1'540 m/s dans les tissus), il est facile de déterminer la distance de la cible qui représente le temps mis pour l’aller-retour (Δt) au transducteur (Figure 25.7). Celui-ci émet pendant 1-2 μsec, et reçoit pendant 250 μsec; il passe donc plus de 99% de son temps de travail en écoute.

Figure 25.7 : Le transducteur émet un paquet d’ondes ultrasonores (temps t1) qui est réfléchi par une structure échodense (cible, temps t2) et revient en direction de sa source qu’il atteint au temps t3. Comme la vitesse de déplacement des ultrasons (c) est une constante qui ne dépend que du milieu (1'540 m/s dans les tissus du corps), le temps d’un aller-retour du paquet d’ondes (Δt) permet de calculer la distance (D) entre le transducteur et la cible, donc la profondeur de l’objet dans le corps. Plus la distance est grande, plus le temps pour obtenir une image de la cible est long. La fréquence d’analyse de l’appareil diminue donc lorsqu’il examine des images profondes.
Afin de donner une image cohérente à l’écran, la machine met en mémoire les échos les plus proximaux en attendant le retour des échos les plus lointains (profondeur maximale) et n’affiche une image que lorsqu’elle a la totalité des échos. Plus la profondeur est grande, plus la cadence ralentit, car le temps d'attente est de 13 μsec par cm; il est donc important d'ajuster en permanence la profondeur de lecture à l'écran pour la limiter à la zone d'intérêt. La cadence d’émission et de réception est de 1'000 à 6'000 cycles par seconde. C’est la fréquence de travail de la machine, ou fréquence de récurrence (Pulse Repetition Frequency, PRF). Cette fréquence est fonction de plusieurs paramètres. Elle augmente dans trois circonstances [4].
- Lorsque la profondeur diminue (la durée de l’aller-retour des US diminue);
- Lorsque la durée de l’émission diminue (diminution du packet size);
- Lorsque la fréquence d’émission (f = 2-12 MHz) augmente.
- Diminution de la profondeur;
- Rétrécissement latéral du champ;
- Réduction des fonctions simultanées (flux couleur, par exemple);
- Utilisation de l’imagerie temps-mouvement (TM);
- Technologie électronique du parallel processing (jusqu’à 300 images/s).
Les cadences élevées ne sont pas utiles pour la représentation des images à l’écran, parce que notre œil ne voit pas de différence au-delà de 35 images/s (les écrans sont souvent limités à cette valeur), mais elles sont nécessaires à l’enregistrement digital pour certaines fonctions comme le Doppler tissulaire ou le speckle-tracking (voir Technologies particulières). Un cycle cardiaque représente un poids de 5 à 500 Mo selon la quantité de données enregistrées (image tri-dimensionnelle, flux couleur, etc).
| Cadences de fonctionnement |
| Pulse Repetition Frequency (PRF) : fréquence d’émission et de réception du transducteur par seconde (1'000 – 6'000 cycles/sec). Frame rate (FR) : cadence d’afficharge des images sur l’écran (8-80/sec selon la profondeur et la largeur du champ). |
Traitement électronique
L’information reçue du transducteur subit une série de manipulations informatiques avant et après être acquise dans le processeur central de la machine. On parle de Preprocessing et de Postprocessing. Ceci correspond à une série de réglages qui sont des plus importants pour obtenir une image satisfaisante et exclure un certain nombre d’artéfacts (Figure 25.8) [2.3]. Une partie de ces réglages est automatisées dans les appareils récents sous forme d'une optimalisation électronique des conditions de réception des ultrasons.

Figure 25.8 : Exemple du panneau de réglages et de l'écran des programmes d'un appareil d'écho-cardiographie. La rangée de boutons située sous l'écran permet de choisir et d'actionner les programmes qui y figurent. Les boutons situés autour de la boule (trackball) commandent les modalités principales (Doppler, couleur, mode TM, curseur, enregistrement, etc). LGC: lateral gain compensation. TGC: time-gain compensation.
Le Preprocessing comprend plusieurs éléments qui sont ajustés avant l'émission des ultrasons.
- Transmission ; c’est l'amplitude d’émission des US (en dB) ; elle est en général préréglée par le fabricant ; la puissance maximale est 100-200 mW/cm2. Augmenter la puissance a un effet similaire à celui d'une augmentation de gain, mais au prix d'un transfert d'énergie plus élevé, donc avec un risque plus grand d'effet biologique (dégagement de chaleur, cavitation).
- Profondeur : durée de l’écoute à la réception; plus le champ d'investigation est profond, plus la cadence d'image diminue.
- Taille du secteur de balayage; la rétrécir augmente la cadence des images.
- Zone focale; elle est centrée sur la zone d'intérêt.
- Fréquence d'émission du transducteur (en ETO 4-9 MHz); elle est ajustable sur la plupart des sondes. Les hautes fréquences donnent une meilleure résolution spatiale mais une plus faible pénétration.
- Réglages spécifiques au Doppler (voir Echocardiographie Doppler).
- Gain : modification de l’intensité des échos en retour; un gain élevé fait apparaître les échos de faible intensité mais donne une image brillante et saturée. Avec un gain optimal, le sang apparaît noir, sans trace d'écho, et le muscle donne une image granuleuse en nuances de gris mais sans zones blanches.
- Compression : cette réduction non-linéaire du spectre ultrasonore de 0-100 dB à 0-40 dB détermine le nombre de nuances de gris; beaucoup de compression intensifie et homogénéise les gris, alors que peu de compression donne des images au contraste noir-blanc excessif (Figure 25.9).
- Compensation de profondeur (time-gain compensation, TGC) : les ultrasons perdent de l’énergie en traversant les tissus ; les échos revenant de la profondeur sont plus faibles que ceux revenant de la zone proximale. Un système de 6 à 8 coulisseaux horizontaux permet d’amplifier sélectivement les échos par tranches de profondeur correspondantes. Ils sont normalement réglés de manière à atténuer les échos très forts venant de la zone proche du capteur et à renforcer les échos plus faibles venant de la zone distale.
- Compensation latérale (lateral-gain compensation, LGC) : un système analogue permet de régler l’intensité des échos par tranches radiaires. Ces deux systèmes de compensation participent au gain général. Ils sont partiellement automatisés dans les nouveaux appareils.
- Rejet: le bruit de fond peut être éliminé par le rejet de certaines fréquences et amplitudes.
- Filtres : un système de filtre propre au Doppler permet d’éliminer les échos des tissus lorsqu’on examine les vélocités du sang, en filtrant les basses fréquences (les tissus ont des mouvements de faible vélocité) et les hautes amplitudes (les tissus sont beaucoup plus échogènes que les hématies).
- Renforcement (edge enhancement): il est possible d'accentuer le contraste entre les tissus et le sang pour faciliter la détection de l'endocarde.
- Interpolation: des algorithmes comblent les "trous" qui peuvent apparaître entre les parties échogènes des structures cardiaques; ceci est particulièrement utile en échograpgie 3D.
- Persistence: l'addition d'images intermédiaires entre la précédente et la suivante donne un résultat plus fondu et moins saccadé sur l'écran, notamment lorsque la cadence d'affichage est basse.

Figure 25.9 : Effets du gain et de la compression sur le rendu d'une même image à l'écran (vue 4-cavités 0°). A: gain et compression normaux. B: excès de gain; le contraste noir-blanc est violent, les structures fines ont disparu. C: faible compression; le contraste noir-blanc est accentué par manque de nuance dans les gris. D: excès de compression; le niveau des gris est trop élevé, le degré de contraste est trop faible pour distiguer des structures fines.
Trois manœuvres particulières de postprocessing sont très utiles en cours d'examen.
- Gel (freeze): la machine conserve en mémoire vive 10-20 secondes d’enregistrement, que l’on peut faire défiler en manipulant la boule de contrôle (track-ball). L'appareil est mis en veilleuse dans cette position dès qu'on n'observe plus les images.
- Zoom : il est possible d’agrandir un secteur de l’image; le zoom n’augmente pas la résolution de l’image mais agrandit sa présentation à l'écran.
- Mesures: la quantification des données demande de très nombreuses mesures qui sont effectuées sur l'image gelée; elles concernent des distances (caliper), des surfaces (trace) ou des vélocités (Doppler). En activant les programmes concernés, le volume, la fonction (fraction d'éjection, par ex), le débit ou la sévérité d'une valvulopathie sont calculés automatiquement et transférés dans le rapport d'examen.
| Traitement électronique |
| Toute une série de réglages permet d'adapter le rendu de l'image par rapport à l'émission et au retour des ultrasons. Ce sont le preprocessing (puissance, fréquence, profondeur, taille du secteur) et le postprocessing (gain, compensation de profondeur, filtres, gel, zoom). |
© CHASSOT PG, BETTEX D. Mars 2011, Avril 2019; dernière mise à jour, Mars 2020
Références
- BARRICK BP, PODGOREANU MV, PROKOP EK. Physics of ultrasound imaging. In: MATHEW JP, SWAMINATHAN M, AYOUB CM. Clinical manual and review of transesophageal echocardiography, 2nd edition. New York: McGraw-Hill 2010, 1-15
- BETTEX D, CHASSOT PG. Echocardiographie transoesophagienne en anesthésie-réanimation. Paris: Masson, Williams & Wilkins, 1997, 13-39
- CHASSOT PG. Physical principles of ultrasound. In: POELAERT J, SKARVAN K, eds. Transoesophageal echocardiography in anaesthesia and intensive care medicine. 2nd ed. London: BMJ Books, 2004, 1-22
- GARBI M, D'HOOGE J, SHKOLNIK E. General principles of echocardiography. In: LANCELOTTI P, ZAMORANO JL, HABIB G, BADANO L. The EACVI Textbook of echocardiography. Oxford: Oxford University Press, 2017, 1-14
- HRABAK H, FORSBERG E, ADAMS D. Understanding ultrasound system controls. In: MATHEW JP, SWAMINATHAN M, AYOUB CM. Clinical manual and review of transesophageal echocardiography, 2nd edition. New York: McGraw-Hill 2010, 16-35
