Le clopidogrel est la thiénopyridine d’utilisation la plus courante depuis l’abandon de la ticlopidine à cause de ses effets secondaires (hémorragie digestive, neutropénie, thrombocytopénie). Les thiénopyridines sont des inhibiteurs non-compétitifs irréversibles du récepteur ADP P2Y12 ; elles empêchent les plaquettes de sécréter leurs médiateurs thrombogènes et inflammatoires, et préviennent leur agrégation. Administré seul, notamment chez les patients intolérants à l’aspirine, le clopidogrel n’est que marginalement plus efficace que celle-ci ; il présente le même risque hémorragique. Mais le clopidogrel est en général prescrit en combinaison avec l’aspirine (bithérapie). Dans ces conditions, il diminue le risque cardiovasculaire de 36% en moyenne en prévention secondaire (Figure 29.5) [4,5, 13,16,19,20,28,31,32].
- Baisse de récidive et mortalité après STEMI 46%
- Baisse de mortalité après SCA 26%
- Baisse de mortalité et de thrombose après stent 31-50%
- Baisse de récidive après ictus 30%
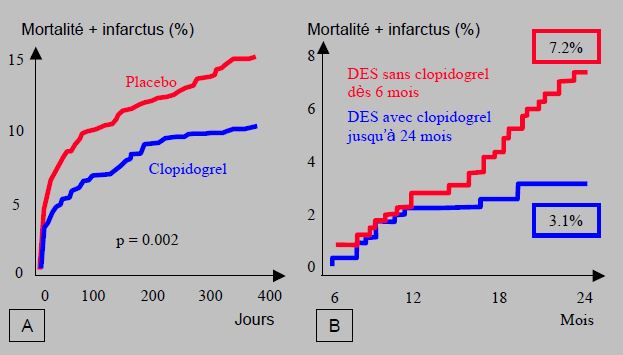
Figure 29.5 : Evidences de l’efficacité du clopidogrel associé à l’aspirine. A : à 1 an, l’incidence combinée de mortalité, d’infarctus et de revascularisation après stent coronarien est de 31% plus basse avec du clopidogrel par rapport à un placebo en plus de l’aspirine (étude PCI-CURE) [20]. B : les porteurs de stents coronariens à élution (DES, drug-eluting stent) de 1ère génération ont un risque de mortalité et d’infarctus à 2 ans diminué de plus de moitié lorsqu’ils sont en permanence sous clopidogrel par rapport à ceux qui ont arrêté après 6 mois [13].
Mais la bithérapie augmente le risque hémorragique de 2.1%/an (incidence de saignements : 1.5 - 2.1%). Or, l’hémorragie est un risque en soi ; lors de syndrome coronarien aigu, elle augmente de 5 fois la mortalité à un mois (HR 5.37), soit autant que la nécrose de la zone à risque [12]. L’addition de clopidogrel à l’aspirine ne présente aucun intérêt en prévention primaire [8].
Le métabolisme du clopidogrel présente plusieurs particularités [1,17,24].
- 85% de la substance absorbée dans le tube digestif est détruit par les estérases ; ces enzymes sont particulièrement actives chez les diabétiques, ce qui diminue d’autant l’efficacité du médicament chez ces patients [2].
- Le clopidogrel est un précurseur inactif dont la demi-vie est de 6-8 heures ; il doit être oxydé par des cytochromes hépatiques du groupe P450 (CYP3A4, CYP3A5, CYP2C19) en deux étapes : transformation en 2-oxo-clopidogrel puis en composé thiol actif mais instable, dont la demi-vie est d’environ 60 minutes.
- Ce métabolite actif bloque irréversiblement le récepteur ADP P2Y12 de manière covalente (pont disulfure avec la cystéine) pour toute la durée de vie de la plaquette.
- Bien qu’irréversible, l’inhibition n’est pas totale ; la réduction de l’agrégation plaquettaire est de 40-60%.
Il existe une forte compétition avec d’autres médicaments pour la métabolisation par les enzymes hépatiques. Cette compétition diminue la synthèse de métabolite actif du clopidogrel, donc son efficacité antiplaquettaire, alors qu’elle freine la dégradation des autres substances, donc augmente leur effet clinique. Parmi les nombreuses substances incriminées (statines, inhibiteurs de la pompe à proton, diazepam, bloqueurs calciques, ketoconazole), deux seules semblent avoir un impact clinique sur le devenir des patients : l’atorvastatine et l’omeprazole [3,6,21]. L’administration concomitante de clopidogrel et d’atorvastatine, qui est la statine la plus souvent prescrite, tend à augmenter le risque cardiovasculaire des patients ; cet effet n’a pas été retrouvé avec les autres statines [6]. D’autre part, l’utilisation simultanée d’omeprazole et de clopidogrel diminue l’efficacité de ce dernier de 25% ; mais là encore, l’interférence est discutée car elle n’a pas été retrouvée dans le seul essai randomisé réalisé jusqu’ici [7] ; elle ne semble pas exister pour les autres inhibiteurs de la pompe à proton (IPP) [11,14, 18,29]. Malgré la discordance de ces résultats, il est préférable d’éviter la prescription d’atorvastatine et d’omeprazole chez les patients sous clopidogrel, particulièrement lorsqu’ils sont à haut risque de thrombose ou qu’ils ont un degré d’inhibition plaquettaire réduit. Par contre, la prescription d’un autre IPP (lanzoprazole, pantoprazole, etc) diminue de 50% le risque d’hémorragie digestive sévère sous aspirine et clopidogrel [27].
Le temps nécessaire à atteindre le pic d’effet dépend de la dose de charge : il est de 72 heures avec 75 mg, de 8 heures avec 300 mg et de 4 heures avec 600 mg. La dose d’entretien est de 75 mg/jour ; bien que l’augmentation de l’effet clinique ne suive pas linéairement celui de la dose, un dosage doublé (150 mg/j) accroît le degré d’inhibition plaquettaire de 31 à 50%, améliore la fonction endothéliale et diminue le taux de protéine C-réactive [24]. Cinq jours après l’arrêt du clopidogrel, 57% des individus ont ≤ 20% d’inhibition plaquettaire résiduelle, et 87% ont une agrégabilité normale [25,26].
Le clopidogrel présente cinq inconvénients majeurs [9,10] :
- Sa biodisponibilité est faible et sa biotransformation variable ;
- Son degré d’inhibition plaquettaire n’est que de 40-60% ;
- Son effet s’installe lentement et met plus de 5 jours à disparaître ;
- Son inhibition plaquettaire est irréversible ; il faut attendre le renouvellement des plaquettes (10%/jour) pour que son activité cesse ;
- Son activité antiplaquettaire est sujette à une grande variabilité interindividuelle (12-35% de non-répondeurs) (voir Résistance aux antiplaquettaires).
Il existe quelques possibilités de surmonter ces difficultés :
- Augmenter les doses : dose de charge 600-900 mg, dose quotidienne 150 mg ;
- Adjonction de cilostazol ou d’anticoagulant (rivaroxaban) à la combinaison aspirine + clopidogrel (triple thérapie) ;
- Remplacement par de nouvelles substances plus efficaces, telles le prasugrel ou le ticagrelor ;
- Tests d’activité plaquettaire et tests génomiques pour identifier les non-répondeurs (voir Réactivité plaquettaire et évènements cliniques).
Avec l'introduction du ticagrelor et du prasugrel, le clopidogrel n'est plus le médicament de première ligne en cas de syndrome coronarien aigu (SCA) ou de revascularisation par PCI. Sa place s'est rétrécie aux situations suivantes [30]:
- Situations où le ticagrelor et le prasugrel sont indisponibles;
- Alternative au ticagrelor dans les SCA sans surélévation ST (N-STEMI);
- PCI et stent en cas de coronaropathie stable;
- Situation à haut risque hémorragique comme la thrombolyse;
- Triple thérapie: en association avec un anticoagulant (aspirine + clopidogrel + anticoagulant).
L’arrivée sur le marché de génériques du clopidogrel soulève le problème de l’efficacité des différents sels de la substance. La molécule originale est du sulfate de clopidogrel, alors que les génériques sont du bésylate ou de l’hydrochlorure de clopidogrel. Bien qu’ils soient équivalents chez les individus normaux chez qui ils ont été testés, ces sels peuvent présenter des différences chez les patients âgés, insuffisants cardiaques ou rénaux, et polymédicalisés [22,23]. Les copies contiennent également beaucoup de l’énantiomère-R du clopidogrel, qui est inactif [15]. Pour l’instant, on ne dispose pas de preuves cliniques que les génériques soient inférieurs à l’original, mais la question est certainement biaisée par le marketing du fabricant (Sanofi-Aventis), qui s’est vu infliger une amende considérable par la Commission Européenne de la Concurrence en 2013 pour dénigrement infondé des génériques.
| Antiplaquettaires classiques: clopidogrel |
|
Le clopidogrel est une thiénopyridine bloquant irréversiblement le récepteur ADP (P2Y12) et réduisant l’agrégation plaquettaire de 40-60% ; métabolisme particulier :
- Destruction à 85% par les estérases (hyperactives chez les diabétiques) ;
- Oxydation en un métabolite actif par des cytochromes hépatiques ;
- Demi-vie du clopidogrel 7 heures, demi-vie des métabolites < 1 heure ;
- Compétition pour ces cytochromes avec de nombreuses substances ; seuls l’atorvastatine et l’oméprazole semblent réduire le métabolisme du clopidogrel au
point de diminuer son efficacité clinique.
Administré seul, il a le même effet et le même risque hémorragique que l’aspirine ; en double thérapie (aspirine + clopidogrel), il réduit le risque cardiovasculaire de 36%, mais augmente le risque hémorragique de 2.1%/an. Dose de charge : 300-600 mg, entretien : 75 (150) mg/j. Inconvénients :
- Faible biodisponibilité, biotransformation variable ;
- Inhibition plaquettaire incomplète ;
- Long délai d’action (4 heures pour 600 mg), effet pour la durée de vie de la plaquette ; disparition de l’effet clinique en ≥ 5 jours ;
- Grande variabilité interindividuelle (taux moyen de faibles répondeurs : 25%) ;
- Durée d’interruption recommandée avant chirurgie : 5 jours.
|
© CHASSOT PG, DELABAYS A, SPAHN D Mars 2010, dernière mise à jour Août 2018
Références
- ACHAR S. Pharmacokinetics, drug metabolism, and safety of prasugrel and clopidogrel. Postgrad Med 2011 ; 123 :73-9
- ANDERSSON C, LYNGBAEK S, NGUYEN CD, et al. Association of clopidogrel treatment with risk of mortality and cardiovascular events following myocardial infarction in patients with and without diabetes. JAMA 2012; 308:882-9
- ANGIOLILLO DJ, FERNANDEZ-ORTIZ A, BERNARDO E, et al. Variability in individual responsiveness to clopidogrel: clinical implications, management and future perspectives. J Am Coll Cardiol 2007; 49:1505-16
- ATTC - Antithrombotic Trialist's Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002, 324:71-86
- ATTC - Antithrombotic Trialist's Collaboration. Aspirin in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials. Lancet 2009; 373:1849-60
- BATES ER, LAU WC, ANGIOLILLO DJ. Clopidogrel-drug interactions. J Am Coll Cardiol 2011; 57:1251-63
- BHATT DL, CRYER BL, CONTANT CF, et al. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med 2010; 363:1909-17
- BHATT DL, FOX KA, HACKE W, et al. Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events. N Engl J Med 2006; 354:1706-17
- CATTANEO M. New P2Y12 inhibitors. Circulation 2010; 121:171-9
- CHASSOT PG, MARCUCCI C. Thérapie antiplaquettaire. Potentiels et dangers des nouveaux agents. Cardiovasc 2010; 9:9-12
- CUISSET T, FRERE C, QUILICI J, et al. Comparison of omeprazole and pantoprazole influence on a high 150 mg clopidogrel maintenance dose. J Am Coll Cardiol 2009; 54:1149-53
- EIKELBOOM JW, MEHTA SR, ANAND SS, et al. Adverse impact of bleeding on prognosis in patients with acute coronary syndromes. Circulation 2006; 114:774-82
- EISENSTEIN EL, ANSTROM KJ, KONG DF, et al. Clopidogrel use and long-term clinical outcomes after drug-eluting stent implantation. JAMA 2007; 297:159-68
- GILARD M, ARNAUD B, CORNILY JC, et al. Influence of omeprazole on the antiplatelet action of clopidogrel associated with aspirin: The randomized, double-blind OCLA study. J Am Coll Cardiol 2008; 51:256-60
- GOMEZ Y, ADAMS E, HOOGMARRENS J. Analysis of purity in 19 drug product tablets containing clopidogrel: 18 copies versus the original brand. J Pharma Biomed Anal 2004; 34:341-8
- GURBEL PA, TANTRY US. Combination antithrombotic therapies. Circulation 2010; 121:569-83
- HALL R, MAZER CD. Antiplatelet drugs: A review of their pharmacology and management in the perioperative period. Anesth Analg 2011; 112:292-318
- HO PM, MADDOX TM, WANG L, et al. Risk of adverse outcomes associated with concomitant use of clopidogrel and proton pump inhibitors following acute coronary syndrome. JAMA 2009; 301:937-44
- KUSHNER FG, HAND M, SMITH SC, et al. 2009 focused update: ACC/AHA Guidelines for the management of patients with ST-elevation myocardial infarction and ACC/AHA/SCAI Guidelines on percutaneous coronary intervention. J Am Coll Cardiol 2009; 54:2205-41
- MEHTA SR, YUSUF S, PETERS RJ, et al. Effects of pretreatment with clopidogrel and aspirin followed by long-term therapy in patients undergoing percutaneous coronary intervention: the PCI-CURE study. Lancet 2001; 358:527-33
- MOUKARBEL GV, BHATT DL. Antiplatelet therapy and proton pump inhibition: clinician update. Circulation 2012; 125:375-80
- NEUBAUER H, KRÜGER JC, LASK S, et al. Comparing the antiplatelet effect of clopidogrel hydrogensulfate and clopidogrel besylate: a crossover study. Clin Res Cardiol 2009; 98:533-40
- PATEL A, JONES SA, FERRO A, PATEL N. Pharmaceutical salts: a formulation trick or a clinical conundrum ? Br J Cardiol 2009; 16:281-6
- PATTI G, GRIECO D, DICUONZO G, et al. High versus standard clopidogrel maintenance dose after percutaneous coronary intervention and effects on platelet inhibition, endothelial function, and inflammation. J Am Coll Cardiol 2011; 57:771-8
- PRICE MJ, TEIRSTEIN PS. Dynamics of platelet functional recovery following a clopidogrel loading dose in healthy volunteers. Am J Cardiol 2008; 102:790-5
- PRICE MJ, WALDER JS, BAKER BA, et al. Recovery of platelet function after discontinuation of prasugrel or clopidogrel maintenance dosing in aspirin-treated patients with stable coronary disease. J Am Coll Cardiol 2012; 59:2338-43
- RAY WA, MURRAY KT, GRIFFIN MR, et al. Outcomes with concurrent use of clopidogrel and proton-pump inhibitors. Ann Intern Med 2010; 152:337-45
- SABATINE MS, CANNON CP, GIBSON CM, et al. Addition of clopidogrel to aspirin and fibrinolytic therapy for myocardial infarction with ST-segment elevation. N Engl J Med 2005; 352:1179-89
- SIMON T, STEG PG, GILARD M, et al. Clinical events as a function of proton pump inhibitor use, clopidogrel use, and cytochrome P450 2C19 genotype on a large nationwide cohort of acute myocardial infarction. Circulation 2011; 123:474-82
- VALGIMIGLI M, BUENO H, BYRNE RA, et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS. Eur Hesrt J 2018; 39:213-54
- WRIGHT RS, ANDERSON JL, ADAMS CD, et al. 2011 ACCF/AHA focused update of the Guidelines for the management of patients with unstable angina/non-ST-elevation myocardial infarction. J Am Coll Cardiol 2011; 57:1920-59
- YUSUF S, ZHAO F, MEHTA SR, et al. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndrome without ST-segment elevation. N Engl J Med 2001; 345:494-502
