Indices préopératoires
Les indices de risque servent à sélectionner les malades à risque cardiovasculaire élevé, chez qui la cardioprotection pharmacologique et les investigations cardiologiques ont le maximum d’impact et le plus de chance de modifier la thérapeutique. Ils sont utiles pour identifier les 4-5% des patients à risque intermédiaire ("zone grise") qui risquent de développer des complications cardiaques [4,7]. D’une manière générale, ils ont une bonne valeur prédictive négative mais une faible valeur prédictive positive. Les critères postopératoires utilisés pour justifier la prédiction sont les complications cardio-vasculaires et la mortalité. Toutefois, cette dernière est biaisée par le fait que les décès cardiaques ne représentent que le 45% de la mortalité postopératoire [4]. Parmi les nombreux indices imaginés, les plus fréquemment utilisés sont le score ASA, le Revised Cardiac Risk Index (RCRI), l'indice du National Surgical Quality Improvement Program (NSQIP), et l'indice du New England Vascular Study Group (NEVSG).
Le score ASA comprend cinq catégories de risque: I (patient sain), II (maladie systémique modérée sans limitation fonctionnelle), III (maladie systémique sévère avec limitation fonctionnelle), IV (maladie incapacitante menaçant la survie), V (malade moribond) et VI (état de mort cérébrale). Entre les stades II et IV, l'augmentation du risque d'accident cardiaque est de presque 10 fois [4,12].
Le Revised Cardiac Risk Index de Lee est basé sur une cohorte de 4'315 patients de la Nouvelle-Angleterre, âgés de > 50 ans et opérés d’une intervention chirurgicale majeure élective. Cet indice a été validé dans une cohorte prospective de 2'893 patients. Sa valeur discriminative est satisfaisante (ROC = 0.76) [18]. Il comprend les six variables suivantes (Tableau 3.6A) :
- Intervention chirurgicale majeure ;
- Présence ou anamnèse de coronaropathie ;
- Présence ou anamnèse d’insuffisance cardiaque;
- Anamnèse d’AVC ou d’AIT, avec ou sans séquelles ;
- Diabète insulino-requérant ;
- Insuffisance rénale (créatininémie > 200 μmol/L).
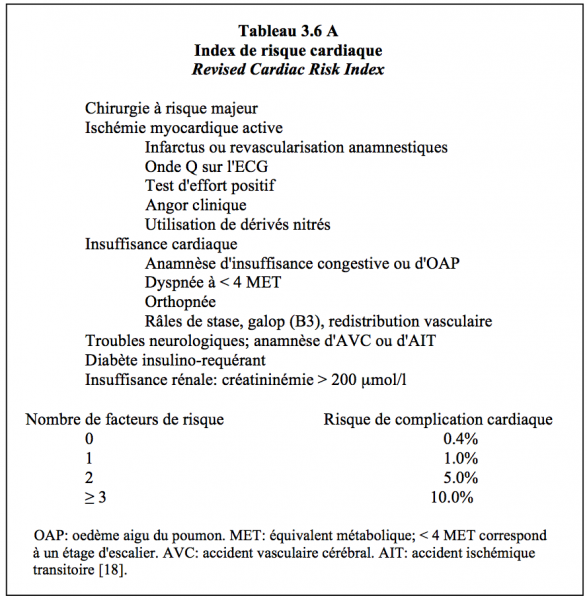
Basée sur la présence de zéro, un, deux ou trois de ces facteurs, l’incidence de complications cardiaques majeures est respectivement de 0.4%, 1%, 5% et 10%. Différents points peuvent être ajoutés pour améliorer la performance de cet indice: clairance à la créatinine (< 30 mL/min) au lieu de la créatininémie [7], âge, sténose aortique serrée, capacité fonctionnelle (< 4 MET), vasculopathie, différentiation des coronariens revascularisés par rapport à ceux qui ne le sont pas (infarctus, angor stable, angor instable), catégorisation du type de chirurgie [4]. Les diabétiques insulino-requérants doivent être considérés de facto comme des coronariens; en effet, le diagnostic de diabète type I (diabetes mellitus) est équivalent à un diagnostic de maladie coronarienne puisque les diabétiques sans anamnèse coronarienne souffrent de la même mortalité cardiovasculaire à 5 ans que les patients non-diabétiques qui ont fait un infarctus [2,19].
L’indice de Lee définit bien les malades qui présentent peu de facteur de risque (1-2), mais il n'est pas performant pour discriminer ceux qui sont à risque élevé (≥ 3) ; il est également peu efficace pour évaluer les patients vasculaires (ROC = 0.59) et les malades souffrant de SIDA [10]. En effet, pour être efficace un indice doit quantifier des affections dont l’incidence est basse dans les bons cas et élevée dans les hauts risques ; or les malades vasculaires souffrent quasiment tous de diabète, d’athéromatose et d’hypertension, ce qui rend ces affections non discriminantes dans cette catégorie. Malgré ses limites et sa faible performance pour les groupes à haut risque comme la chirurgie vasculaire, cet index est un standard dans l’évaluation préopératoire.
Par régression logistique multivariée à partir d'un collectif de 211'410 patients, le National Surgical Quality Improvement Program (NSQIP) de l'American College of Surgeons a mis au point un premier indice comprenant 5 facteurs indépendants [14]:
- Type de chirurgie (21 opérations spécifiées);
- Status fonctionnel (indépendant, peu dépendant, totalement dépendant);
- Créatininémie (< 200 μmol/L ou > 200 μmol/L);
- Classe de risque ASA (I à V);
- Age (en clair).
Malgré l'absence de pathologies comme la coronaropathie ou l'insuffisance cardiaque, cet indice a une bonne corrélation (ROC 0.88) avec les deux complications postopératoires choisies comme critères d'évaluation: l'infarctus et l'arrêt cardiaque [14]. L'indice NSQIP a été modifié et complété en 2013; il comprend maintenant 21 facteurs (Tableau 3.6 B).

Le calculateur de risque se présente comme un formulaire téléchargeable qu'il suffit de remplir et qui donne le taux de risque d'une série de complications postopératoires, dont l'infarctus, l'arrêt cardiaque et la mortalité (https://www.riskcalculator.facs.org/RiskCalculator/index.jsp). La corrélation avec le devenir des malades est améliorée par rapport à la première version: 0.90 pour l'arrêt cardiaque et l'infarctus, 0.94 pour la mortalité [20].
Le Vascular Study Group of New England Cardiac Risk Index (VSG-CRI) est dédié particulièrement à la chirurgie vasculaire, pour laquelle les indices classiques sont peu performants. Il comprend neuf items différents [3].
- Age : > 80 ans (4 points), 70-79 ans (3 points), 60-69 ans (2 points) ;
- Insuffisance cardiaque congestive (2 points) ;
- BPCO (2 points) ;
- Coronaropathie active (2 points) ;
- Créatinine > 200 μmol /L (2 points) ;
- Tabagisme (1 point) ;
- Diabète insulino-dépendant (1 point) ;
- Béta-blocage de longue durée (1 point) ;
- Anamnèse de coronaropathie (pontage, PCI) (1 point).
Le risque de morbi-mortalité postopératoire est quantifié comme suit selon l’échelle des points obtenus.
- 0-3 points : 2.5% ;
- 4 points : 3.5% ;
- 5 points : 6% ;
- 6 points : 6.6% ;
- 7 points : 8.9% ;
- ≥ 8 points : ≥ 14%.
Pour simplifier l’évaluation, un nouvel indice, basé sur une cohorte de près de 300'000 malades, permet un calcul rapide en ne se basant que sur trois critères simples [13].
- Status ASA : I (0 point), II (2 points), III (4 points), IV (5 points), V (6 points) ;
- Type de chirurgie : risque intermédiaire (1 point) ou risque élevé (2 points) ;
- Urgence (1 point).
La mortalité postopératoire est corrélée à cette échelle de la manière suivante :
- 0-4 points : < 0.5% ;
- 5-6 points 1.5-4.0% ;
- > 6 points : > 10%.
Outre leur sus- ou sous-estimation du risque réel selon les catégories de patients, ces indices présentent le défaut de ne pas inclure les biomarqueurs, qui sont devenus un élément-clef dans l'évaluation préopératoire. Ces derniers ont l'avantage de l'objectivité par rapport à l'interprétation d'un status clinique. Toutefois, le jugement d'un clinicien expérimenté est d'une grande valeur pour la synthèse des différents éléments.
Plus de 25 calculateurs de risque cardiovasculaire sont actuellement disponibles sur le Web. Bien que leur utilisation soit recommandées par les directives internationales [9,17], leur degré de concordance est malheureusement faible (67%): un même patient est classé dans 2 catégories différentes (risque bas, modéré ou élevé) dans un tiers des cas. Au sein de la même catégorie, le risque de mortalité varie de 1 à 5 selon le calculateur utilisé ; la variabilité est d’autant plus grande que le risque est plus élevé [1]. De fait, la performance des calculateurs n’améliore guère celle du jugement clinique, qui n’est elle aussi pertinente que dans 60 à 70% des cas. La situation est différente pour les scores de risque coronariens spécifiques, comme le score SYNTAX basé sur une série de variables angiographiques quantitatives. Combiné à des données cliniques (âge, sexe, BPCO, clairance de la créatinine, fraction d’éjection), le score SYNTAX-II a une valeur prédictive élevée pour les accidents ischémiques, mais il est essentiellement destiné à la chirurgie de revascularisation coronarienne (ir-nwr.ru/calculators/syntaxscore.htm) [29].
Un indice simple comme le score ASA permet déjà de stratifier les examens de routine dans les cas électifs de chirurgie non-cardiaque, que celle-ci soit mineure, intermédiaire ou majeure [16].
- ASA I: pas de test pour chirurgie mineure ou intermédiaire; ECG, Hb et créatinine pour chirurgie majeure.
- ASA II: pas de test pour chirurgie mineure; ECG, Hb et créatinine pour chirurgie intermédiaire et majeure.
- ASA III et IV: ECG, Hb et créatinine pour chirurgie mineure; idem + tests de coagulation, fonction pulmonaire et radio du thorax pour chirurgie intermédiaire et majeure.
L'échocardiographie est indiquée en présence d'un souffle cardiaque, d'une symptomatologie d'insuffisance ventriculaire, ou d'angor.
Indice peropératoire
Le poids des évènements peropératoires est tel qu'il peut faire perdre leur valeur prédictive aux indices de risque préopératoire. La tachycardie et l'hypotension prolongées, ou les pertes sanguines et les transfusions, sont des éléments particulièrement puissants pour engendrer des conséquences néfastes dans le postopératoire. Le taux d'infarctus et de mortalité est multiplié par un facteur de 2 à 4 (OR 2.4-4.0) par une hémorragie massive entraînant des transfusions répétitives [14]. De ce fait, on a imaginé un score d'Apgar chirurgical basé sur un maximum de 10 points, calculé à partir de 3 données [12].
- Pertes sanguines (mL): 0 (> 1'000), 1 (600-1'000), 2 (100-600), 3 (< 100).
- PAM minimale (mmHg): 0 (< 40), 1 (40-55), 2 (55-70), 3 (> 70).
- Fréquence la plus basse (batt/min): 0 (> 85), 1 (75-85), 2 (65-75), 3 (55-65), 4 (< 55).
Lorsque le score est 9-10, le taux de complications est de 3.6%; il est de 56% pour un score ≤ 4. Ceci représente un risque 16 fois supérieur lorsque le score est au plus bas (RR = 16.1) [12]. Ce score peut s'appliquer à tous les types de chirurgie [25].
Biomarqueurs
Deux marqueurs biologiques sont de bons traducteurs d’une souffrance myocardique : les troponines T et I pour les lésions ischémiques, et le BNP/NT-proBNP pour l’insuffisance ventriculaire. Leur dosage est réservé aux cas suspects d’ischémie active ou de distension myocardique, mais il s'avère qu'ils ont une forte valeur pronostique pour les complications postopératoires.
Même une faible élévation de leurs taux (troponine T > 0.02 ng/mL) reflète une lésion cellulaire significative et prédit une aggravation du pronostic cardiovasculaire postopératoire. Les tests à haute sensibilité capables d’identifier des traces de troponine T (TnT-hs) permettent de détecter des lésions myocardiques minimes et d’augmenter la pertinence de l’évaluation préopératoire. Ainsi, les patients qui ont un taux de TnT-hs préopératoire > 14 ng/L ont un risque d’infarctus postopératoire significativement plus élevé (8.6%) après chirurgie non-cardiaque majeure que ceux qui ont un taux inférieur à cette valeur (2.5%) (OR 3.67) [23]. La moitié de ceux qui ont un taux > 14 ng/L souffrent d'ailleurs d'une coronaropathie justifiant une revascularisation préopératoire [22]. Ils doivent être suivis par des tests répétés en postopératoire.
Définie par les troponines à haute sensibilité (TnT-hs), une ischémie myocardique postopératoire est présente chez 8-19% des patients à risque intermédiaire et élevé, bien que 58% d’entre eux ne remplissent pas les critères d’un infarctus et que 84% soient asymptomatiques [6,26]. Ils souffrent de ce qu’il est convenu d’appeler MINS (Myocardial Injury after Noncardiac Surgery) [6,27]. Cette souffrance myocardique sans traduction clinique ni électrocardiographique correspond toutefois à une pathologie bien réelle, puisqu'elle est associée à une péjoration significative du pronostic et à une mortalité 3 fois plus élevée (OR 2.9) [24]. Cette mortalité est proportionnelle au taux de troponine. Ainsi, une élévation de 0.02 ng/L, 0.03-0.25 ng/L et de ≥ 0.3 ng/L est associée à une élévation de la mortalité postopératoire de 2.41, 5.0 et 10.5 fois respectivement [28]. Toutefois, l’élévation du taux de troponine postopératoire à des valeurs inférieures à celles admises pour le diagnostic non-équivoque d’infarctus est un marqueur de risque pour les complications cardiovasculaires et générales (embolie pulmonaire, insuffisance respiratoire, AVC, sepsis) plus que pour l’infarctus per se [27]. La question est de savoir si la mise en évidence de MINS réclame une sanction thérapeutique, bien que le taux de troponine soit faible et l’ECG sans altération. Une étude portant sur 667 patients de chirurgie vasculaire a montré que le traitement correspondant à celui d’une ischémie myocardique stable asymptomatique (antiplaquettaires, statine, béta-bloqueur, inhibiteur de l’enzyme de conversion et, à long terme, modifications du style de vie) est bénéfique: le risque de complication est nettement diminué (HR 0.63) chez les patients traités activement alors qu'il est augmenté chez ceux qui ne l'ont pas été (HR 2.8) [11]. Ce traitement est parfaitement concevable comme préparation préopératoire également.
Le dosage préopératoire du BNP/NT-proBNP prédit assez bien le risque de décompensation ventriculaire, d'infarctus et de décès postopératoire. Ces complications surviennent chez 22% des patients dont la valeur préopératoire est au-dessus du seuil (BNP 92 ng/L, NT-proBNP 300 ng/L), comparé à 4.9% lorsque cette valeur est inférieure à ces seuils (OR 3.4) [26]. Le risque est proportionnel au taux des biomarqueurs: l'incidence de complications est de 5.1%, 11.6% et 26.3% lorsque le BNP est respectivement < 100, 100-250 ou > 250 ng/L; elle s'élève jusqu'à 39.5% lorsque le NT-proBNP est > 3000 ng/L [26]. La capacité discriminante du BNP et du NT-proBNP est du même ordre de grandeur que celle d'un test d'effort, comme le montre leur valeur prédictive: ROC 0.75 et 0.81, respectivement [15].
La copeptine est un marqueur de l’activité arginine-vasopressine qui s’élève dans les situations de stress physiologique et qui peut être un prédicteur complémentaire des complications postopératoires lorsque les troponines sont normales. Un taux préopératoire ≥ 9.6 pmol/L est associé à une augmentation des lésions myocardiques (AUC 0.66) et à une amélioration de la stratification du risque opératoire [21]. La présepsine est un marqueur de la réaction inflammatoire systémique. En chirurgie cardiaque, son élévation présente une bonne corrélation (0.81-0.88) avec la mortalité postopératoire [5]. La portée de ces tests n’est toutefois pas encore établie.
Pour affiner le pronostic préopératoire et pour pouvoir juger de l'élévation postopératoire, il est donc actuellement suggéré (recommandation classe IIb, degré d'évidence B) de doser les biomarqueurs chez les patients à risque intermédiaire et majeur (> 1 facteur de risque) avant des interventions majeures [9,17]. Cette attitude permet de limiter les investigations cardiologiques (épreuves d'effort, IRM, coronarographie) aux patients chez qui elles ont le plus de chance d'être positives et de conduire à une modification de la prise en charge thérapeutique (Figure 3.8) [8]. Mais ceci permet aussi de déceler des malades à troponines élevées que leur absence de symptômes n'aiguillerait pas vers des tests cardiologiques, alors qu'ils présentent un risque de complications cardiovasculaires de 5-40%.
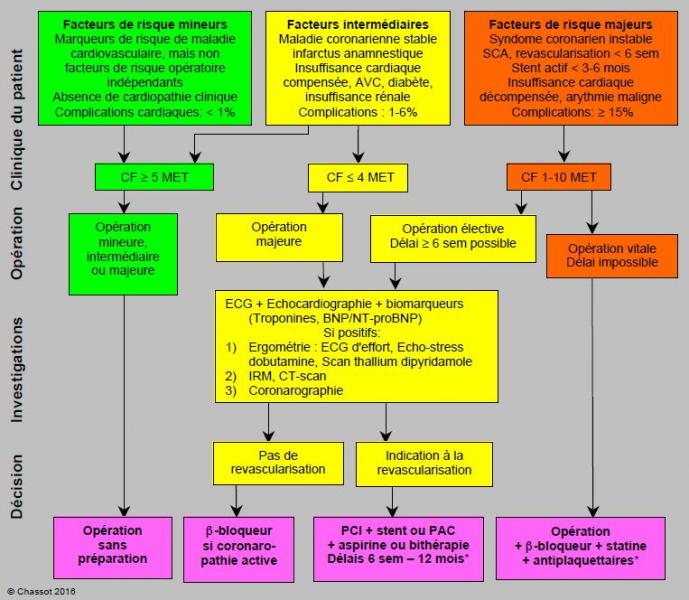
Figure 3.8 : Algorithme d'évaluation du patient ischémique ou à risque coronarien pour la chirurgie non-cardiaque. Les patients à risque mineur et intermédiaire avec une bonne capacité à l'effort peuvent subir une intervention sans investigation ni préparation particulière. Des investigations cardiologiques sont indiquées chez les patients à risque intermédiaire avec une mauvaise performance à l'effort lors d'opération majeure, et chez les patients à risque majeur (cardiopathie instable), pour autant que les délais le permettent. L'ECG, l'échocardiographie et les biomarqueurs sont une étape intermédiaire qui permet de sélectionner les malades chez qui les investigations cardiologiques sont le plus utiles. La revascularisation coronarienne impose des délais importants (variables selon le mode de revascularisation) avant de procéder à la chirurgie. Complications cardiaques: ischémie myocardique, infarctus, défaillance ventriculaire, arythmie grave, décès cardiovasculaire. Dans le syndrome coronarien instable, le risque de thrombose coronarienne à l'arrêt des antiplaquettaires (aspirine + clopidogrel/prasugrel/ticagrelor) est en général plus grave que celui d'hémorragie chirurgicale sur continuation de ces derniers. MET: équivalent métabolique. PCI: Percutaneous Coronary Intervention. PAC: pontage aorto-coronarien. SCA: syndrome coronarien aigu. *: voir Tableaux 3.9A et 3.9B, et Antiplaquettaires.
| Indices de risque opératoire |
|
De nombreux indices permettent d'identifier les malades à risque cardiovasculaire avant une opération. Bien que leur concordance soit modeste, ils offrent la possibilité de calculer la mortalité prévisible d'une intervention. Le plus couramment utilisé est le RCRI qui comprend 6 facteurs: opération majeure, ischémie myocardique, insuffisance cardiaque, AVC, diabète et insuffisance rénale. Comme ils ont une influence prépondérante, les évènements peropératoires doivent aussi être pris en compte.
L'élévation des marqueurs biologiques comme les troponines T et I ou le BNP/NT-proBNP a une forte valeur pronostique pour le risque d'ischémie myocardique ou de décompensation ventriculaire, respectivement. Leur élévation préopératoire est une indication à des investigations cardiologiques.
|
© CHASSOT PG, DELABAYS A, SPAHN DR, Mars 2010, dernière révision Décembre 2019
Références
- ALLAN GM, NOURI F, KOROWNYK C, et al. Agreement among cardiovascular disease risk calculators. Circulation 2013 ; 127 :1948-56
- ARMSTRONG EJ, RUTLEDGE JC, ROGERS JH. Coronary artery revascularization in patients with diabetes mellitus. Circulation 2013; 128:1675-85
- BERTGES DJ, GOODNEY PP, VEITH FJ, et al. The vascular study group of New England cardiac risk index (VSG CRI) predicts cardiac complications more accurately than the revised cardiac risk index in vascular surgery patients. J Vasc Surg 2010; 52:674-83
- BICCARD BM. Proposed research plan for the derivation of a new cardiac risk index. Anesth Analg 2015; 120:543-53
- BOMBERG H, KLINGELE M, WAGENPFEIL M, et al. Presepsin (sCD14-ST) is a novel marker for risk stratification in cardiac surgery patients. Anesthesoilogy 2017; 126:631-42
- BOTTO F, ALONSO-COELLO P, CHAN MT, et al. Myocardial injury after noncardiac surgery: a large international prospective cohort study establishing diagnostic criteria, characteristics, predictors, and 30-day outcomes. Anesthesiology 2014; 120:564-78
- DAVIS C, TAIT G, CARROLL J, et al. The Revised Cardiac Risk Index in the new millennium: a single-centre prospective cohort re-evaluation of the original variable in 9'519 consecutive elective surgical patients. Can J Anaesth 2013; 60:855-63
- DEVEREAUX PJ, SESSLER DI. Cardiac complications in patients undergoing major noncardiac surgery. N Engl J Med 2015; 373:2258-69
- FLEISHER LA, FLEISCHMANN KE, AUERBACH AD, et al. 2014 ACC/AHA Guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2014; 130:e278-e333
- FORD MK, BEATTIE WS, WIJEYSUNDERA DN. Systematic review: prediction of perioperative cardiac complications and mortality by the revised cardiac risk index. Ann Intern Med 2010; 152:26-35
- FOUCRIER A, RODSETH R, AISSAOUI M, et al. The long-term impact of early cardiovascular therapy intensification for postoperative troponin elevation after major vascular surgery. Anesth Analg 2014; 119:1053-63
- GAWANDE AA, KWAAN MR, REGENBOGEN SE, et al. An Apgar score for surgery. J Am Coll Surg 2007; 204:201-8
- GLANCE LG, LUSTIK SJ, HANNAN EL, et al. The surgical mortality probability model: Derivation and validation of a simple risk prediction rule for noncardiac surgery. Ann Surg 2012; 255:696-702
- GUPTA PK, GUPTA H, SUNDARAM A, et al. Development and validation of a risk calculator for prediction of cardiac risk after surgery. Circulation 2011; 124:381-7
- JAMES S, JHANJI S, SMITH A, et al. Comparison of the prognostic accuracy of scoring systems, cardiopulmonary exercise testing, and plams biomarkers: a single-centre observational pilot study. Br J Anaesth 2014; 112:491-7
- KAISER HA, ZURRON N, BEILSTEIN CM, et al. Evaluation préopératoire du risque cardiaque avant des interventions chirurgicales non cardiaques. Forum Méd Suisse 2018; 18:725-32
- KRISTENSEN SD, KNUUTI J, SARASTE A, et al. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management. Eur Heart J 2014; 35:2383-431
- LEE TH, MARCANTONIO ER, MANGIONE CM, ET AL. Derivation and prospective validation of a simple index for prediction of cardiac risk of major noncardiac surgery. Circulation 1999; 100:1043-9
- LINDENAUER PK, PEKOW P, WANG K, et al. Perioperative beta-blocker therapy and mortality after major noncardiac surgery. N Engl J Med 2005, 353 (4), 349-361
- LIU Y, COHEN ME, HALL BL, BILIMORIA KY. Evaluation and enhancement of calibration in the American College of Surgeons NSQIP surgical risk calculator. J Am Coll Surg 2016; 223:231-9
- MAUERMANN E, BOLLIGER D, SEEBERGER E, et al. Incremental value of preoperative copeptin for predicting myocardial injury. Anesth Analg 2016; 123:1363-71
- MOL KHM, HOEKS SA, VAN MIEGHEM NM, et al. Preoperative coronary angiography in vascular patients with symptomatic elevated high-sensitivity troponin T: a case series. Br J Anaesth 2019; 123:565-9
- NAGELE P, BROWN F, GAGE BF, et al. High-sensitivity cardiac troponin T in prediction and diagnosis of myocardial infarction and long-term mortality after noncardiac surgery. Am Heart J 2013; 166:325-32.e1
- OBERWEIS BS, SMILOWITZ NR, NUKALA S, et al. Relation of perioperative elevation of troponin to long-term mortality after orthopedic surgery. Am J Cardiol 2015; 115:1643-8
- REYNOLDS PQ, SANDERS NW, SCHILDCROUT JS, et al. Expansion of the surgical Apgar score across all surgical subspecialties as a means to predict postoperative mortality. Anesthesiology 2011; 114:1305-12
- RODSETH RN, BICCARD BM, LE MANACH Y, et al. The prognostic value of pre-operative and post-operative B-type natriuretic peptides in patients undergoing noncardiac surgery. J Am Coll Cardiol 2014; 63:170-80
- VAN WAES JA, NATHOE HM, DE GRAAFF JC, et al. Myocardial injury after noncardiac surgery and its association with short-term mortality. Circulation 2013; 127:2264-71
- VISION – The Vascular Events in Noncardiac Surgery Patients Cohort Evaluation study investigators. Association between postoperative troponin levels and 30-day mortality among patients undergoing noncardiac surgery. JAMA 2012; 307:2295-304
- YADAV M, PALMERINI T, CAIXETA A, et al. Prediction of coronary risks by SYNTAX and derived scores. J Am Coll Cardiol 2013; 62:1219-30
