Bien que la capacité à l’effort soit plus rapidement limitée dans l’insuffisance aortique que dans la sténose, les symptômes de l’IA sont tardifs dans l’évolution de la maladie, et ne se manifestent qu’après une période de 3 à 10 ans lorsque survient la cardiomégalie et la dysfonction ventriculaire, habituellement entre 40 et 50 ans [3]. La symptomatologie dominante est d’emblée celle de l’hypertension veineuse pulmonaire: dyspnée d’effort puis de repos, orthopnée, et enfin oedème pulmonaire; l’angor est plus rare (20% des cas). Classiquement, la dyspnée et l’angor réveillent le malade au milieu de la nuit, lorsque la baisse de la fréquence cardiaque provoque une dilatation progressive du VG et que la pression diastolique chute considérablement (jusqu’à 30 mmHg). Souvent, il lui suffit de déambuler pendant une demi-heure pour que la fréquence cardiaque augmente et que la dyspnée régresse.
Le grand volume systolique, le pouls bondissant, la très grande pression différentielle et le flux diastolique rétrograde dans l’aorte thoracique descendante sont à l’origine des signes physiques classiques: apex arrondi et hyperdynamique, signe de Musset (hochement de tête avec chaque systole), pouls de Corrigan (pulsus altus et celer) [4]. La courbe artérielle est très ample ; la pente ascendante est verticale, la diastolique basse et la pression pulsée (PAsyst – PAdiast) de 80-100 mmHg.
A l’auscultation, on entend un souffle diastolique decrescendo de tonalité élevée irradiant vers l’apex, maximum au troisième et quatrième espace intercostal gauche en position parasternale (Figure 11.130). Il est souvent accompagné d’un roulement mésodiastolique (souffle d’Austin Flint), occasionné par la vibration du feuillet antérieur de la valve mitrale contre lequel le jet de l’IA se réfléchit (Vidéo) [1]. La sévérité de l’insuffisance est mieux corrélée à la durée qu’à l’intensité du souffle [4].
Vidéo: vibrations diastoliques du feuillet antérieur de la valve mitrale occasionnées par le jet de l'insuffisance aortique qui se réfléchit sur sa face inférieure (vue 4-cavités 0°), à l'origine du roulement de Flint.
Vidéo: vibrations diastoliques du feuillet antérieur de la valve mitrale occasionnées par le jet de l'insuffisance aortique qui se réfléchit sur sa face inférieure (vue 4-cavités 0°), à l'origine du roulement de Flint.
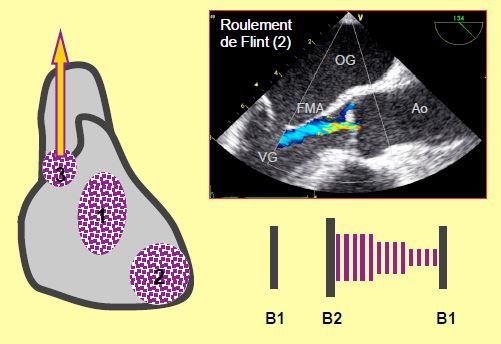
Figure 11.130 : Souffles d'insuffisance aortique: souffle diastolique doux et piaulant (1) ; il est accompagné du roulement de Flint au foyer mitral (2), dont l’origine est une vibration diastolique du feuillet mitral antérieur (FMA) sous l’effet du jet de régurgitation qui en longe sa face ventriculaire; il s’y ajoute un souffle éjectionnel aortique si le flux systolique est très élevé (3).
L’ECG affiche les signes d’une dilatation gauche: déviation gauche, Q prédominant et T pointu dans les territoires gauches; une inversion de l’onde T et un sous-décalage du segment ST non spécifique sont souvent visibles. La radiographie thoracique montre une cardiomégalie très prononcée.
Alors qu’il n’est que de 6%/an lorsque la fonction du VG est conservée, le taux d’apparition des symptômes est de 25%/an lorsque le VG est défailllant et dilaté ; la mortalité est alors de 20%/an [5]. Encore une fois, c’est le diamètre télésystolique excessif du VG (> 2.5 cm/m2) qui est le meilleur prédicteur indépendant de survie [2].
L’insuffisance aiguë se manifeste brutalement par une dyspnée grave, un collapsus cardiovasculaire et un pré-oedème pulmonaire; le patient est tachycarde et hypoperfusé. Le souffle diastolique est moins prononcé et moins long, car la pression intraventriculaire est élevée et le gradient aorto-ventriculaire diminue rapidement en diastole.
| Clinique de l’insuffisance aortique |
|
Symptômes apparaissant avec la dilatation et la dysfonction du VG : dyspnée (stase pulmonaire), angor (tardif). Signes typiques : pouls bondissant et rapide, souffle diastolique. IA aiguë : choc cardiogène.
Caractéristiques de l’insuffisance aortique
Surcharge de volume entraînant une HVG dilatative
Surcharge de pression sur augmentation de la tension de paroi (dilatation)
Fonction VG diminuée (critère de dysfonction : Dtd > 2.5 cm/m2)
Si augmentation des RAS : augmentation de l’IA et de la postcharge du VG
Bradycardie dangereuse : augmentation du volume régurgité par diastole
|
© CHASSOT PG, BETTEX D, Août 2011, dernière mise à jour Août 2018
Références
- BONOW RO, BRAUNWALD E. Valvular heart disease. In: ZIPES DP, et al, eds. Braunwald’s heart disease. A textbook of cardiovascular medicine. 7th edition. Philadelphie: Elsevier Saunders, 2005, 1553-632
- BONOW RO, LAKATOS E, MARON BJ, et al. Serial long-term assessment of the natural history of asymptomatic patients with chronic aortic regurgitation and normal left ventricular systolic function. Circulation 1991; 84:1625-31
- BONOW RO, ROSING DR, McINTOSH CL., et al. The natural history of asymptomatic patients with aortic regurgitation and normal left ventricular function. Circulation 1983; 68:509-14
- BRAUNWALD E. Valvular heart disease. In: BRAUNWALD E. ed. Heart disease. Philadelphia, WB Saunders Co, 1997, 1007-76
- NISHIMURA RA, OTTO CM, BONOW RO, et al. 2014 AHA/ACC Guideline for the management of patients with valvular heart disease. Circulation 2014; 129:e521-e643
