Renvoi de l’opération
Le risque cardiaque peropératoire n’est augmenté que de 1.3 fois chez l’hypertendu sévère non équilibré [3]. La présence d'une hypertension de stade I ou II (< 180/110 mmHg), même découverte la veille de l'intervention, n'est donc pas une raison suffisante pour renvoyer l'opération, bien qu’il faille s'attendre à davantage d'instabilité hémodynamique [5,8]. Une étude contrôlée sur des hypertendus sévères n’a pas pu mettre en évidence de bénéfice à renvoyer l’intervention pour régulariser la pression artérielle avant la chirurgie [9]. L'HTA préopératoire en soi n'est pas associée à une augmentation du taux d'évènements cardiaques ; c'est l'hypotension peropératoire (baisse > 33% de la valeur de base pendant > 10 min) qui est un prédicteur indépendant de complications postopératoires [6]. On sait aussi que les risques opératoires sont liés aux lésions des organes-cibles comme le cœur (HVG, coronaropathie), le cerveau (AVC) ou les reins (néphropathie hypertensive), mais non à l’HTA elle-même [4,5]. Une hypertension de stade III (PAsyst > 180 mmHg, PAdiast > 110 mmHg) augmente le risque d'ischémie myocardique et d'arythmies, mais n'est pas un obstacle à une intervention chirurgicale nécessaire ou vitale ; seule une intervention majeure élective chez un malade souffrant de lésion des organes-cibles peut justifier un délai pour investiguer une cardiopathie associée et instaurer un traitement anti-hypertenseur. Un certain nombre de facteurs aggravent le devenir de l’hypertendu : l’âge, le diabète, les lésions cardio- ou cérébrovasculaires, et l’anamnèse d’accident cardiovasculaire (Tableau 21.6) [2].

La seule contre-indication opératoire formelle est une poussée d’hypertension maligne symptomatique (PA > 220/120 mmHg).
Il existe essentiellement deux motifs pour justifier le renvoi d’une intervention chirurgicale [4,5,8]:
- Améliorer l’état pathologique lié à des lésions d’un organe-cible si cela peut diminuer le risque opératoire (exemples : ischémie coronarienne, sténose carotidienne)
- Investiguer une lésion organique suspectée si les résultats peuvent modifier la prise en charge du patient (exemple : phéochromocytome).
Contrôle peropératoire de la pression
Le but est de maintenir une pression stable et d’éviter les épisodes d’hypotension puisque leur importance est un prédicteur indépendant de complications cardio- et cérébro-vasculaires [6]. Une fluctuation de plus de 20% de la PAM chez les hypertendus sévères prédit une augmentation des complications postopératoires [1]. Malheureusement, l'hypertendu, traité ou non, est sujet à des variations tensionnelles peropératoires plus amples et plus rapides (sur 5-10 battements) que le sujet normal pour plusieurs raisons :
- Dysrégulation idiopathique de la pression artérielle ;
- Arbre vasculaire peu compliant ;
- Insuffisance diastolique ;
- Volume circulant contracté (diurétique) ;
- Traitement chronique bloquant les régulations autonomes.
Plus le système sympathique est bloqué par le traitement, plus la pression devient dépendante du volume circulant. Chez l'hypertendu, les épisodes de stimulation sympathique peropératoire sont souvent la cause d'un échappement vers le haut qui peut conduire à une hémorragie intracrânienne, une décompensation gauche ou des arythmies graves. Il faut éviter un dépassement de plus de 20% de la pression moyenne de base et corriger immédiatement toute variation significative. En chirurgie cardiaque, les moments critiques à cet égard sont l'intubation, l'incision, l'ouverture du sternum, la péricardiotomie, la manipulation de la racine aortique, l'hypothermie de CEC et la fermeture du sternum. Une anesthésie locale sous forme de spray laryngé (xylocaïne 4%) facilite le contrôle lors de l’intubation. Il est capital que la pression artérielle soit basse au moment de la canulation et de la décanulation aortiques, car la paroi du vaisseau peut se déchirer en étoile au point de ponction ou se laisser cisailler par la bourse de fermeture. Non seulement l'anesthésie doit être profonde à ces moments-là (isoflurane → 5% pendant 1-2 minutes), mais il faut souvent administrer en appoint un hypotenseur à effet rapide et de courte durée d'action (phentolamine, nitroglycérine) ou un β-bloqueur (esmolol) si le patient est simultanément tachycarde.
L'hypertendu avec bonne fonction ventriculaire est souvent hyperkinétique: sa fréquence et sa contractilité sont élevées. Dans ce cas, le β-blocage avec un agent de courte durée d'action (esmolol) est indiqué avant la CEC, car il diminue la fréquence cardiaque et la consommation d'oxygène. Après la mise en charge, la stimulation sympathique par les amines endogènes est intense, mais la fonction cardiaque est toujours amoindrie par l'hypothermie, la cardioplégie et l'ischémie. Le β-blocage n'est envisageable qu'avec infiniment de circonspection, et seulement après un contrôle rigoureux de la performance myocardique (échocardiographie, cathéter pulmonaire de Swan-Ganz). Le choix de l'hypotenseur se porte primairement sur un vasodilatateur artériel (isoflurane, phentolamine, nitroprussiate, anticalcique) et sur l'approfondissement de l'anesthésie. Les anticalciques dérivés de la dihydropyridine (nifédipine, nicardipine, isradipine) sont peu ou pas tachycardisants et ne dépriment pas la fonction ventriculaire, mais leur durée d'action est longue. Leur indication préférentielle est la prévention ou le traitement du spasme artériel mammaire ou coronarien.
Il n'y a pas de technique d'anesthésie propre à l'hypertension artérielle en chirurgie cardiaque, alors que l'anesthésie loco-régionale ou combinée présente probablement un certain avantage en chirurgie non cardiaque. Pour l’anesthésie générale, l'isoflurane est particulièrement indiqué parce qu’il a un effet vasodilatateur artériel significatif mais pas d’effet veinodilatateur. Les diazépines et le propofol, au contraire, abaissent la précharge et causent d'amples variations de la pression artérielle chez ces patients dont le volume systolique dépend du remplissage de manière critique. Les fentanils ont très peu d’effet vasodilatateur direct.
Chez l’hypertendu, la pression de perfusion normale des organes est déplacée vers le haut ; la courbe d'autorégulation cérébrale et rénale est translatée vers la droite; une pression moyenne dite "normale" peut être insuffisante pour assurer la perfusion du rein ou du cerveau. La PA ne doit pas s’abaisser à moins de 20% de sa valeur de base au repos. En CEC, la PAM doit être maintenue à au moins 80 mmHg. Une poussée hypertensive contraint le perfusionniste à baisser le débit de la machine, ce qui diminue la perfusion tissulaire. Bien qu'elle soit maintenue en hypothermie modérée (28°C), l'autorégulation cérébrale peut être dépassée par l'hypertension. La perfusion devient pression-dépendante et excessive (perfusion luxuriante) ; elle engendre alors un risque élevé d'oedème cérébral et d'hémorragie intracrânienne à cause de l’anticoagulation complète.
Traitement de l'hypertension peropératoire
En phase peropératoire, la poussée hypertensive peut se présenter sous des aspects variables, mais la première mesure est de s'assurer que la profondeur de l'anesthésie est adéquate et que l'analgésie est suffisante. Ensuite, une palette de substances est à disposition (Tableau 21.7).
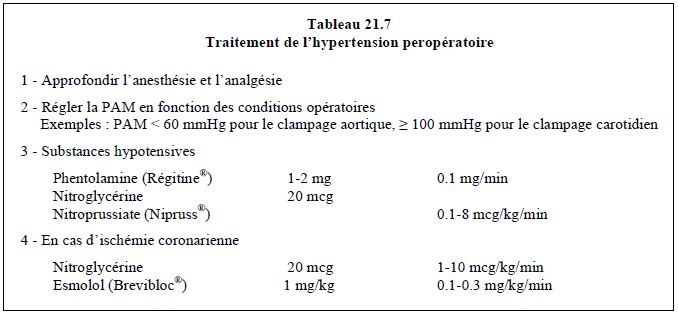
Le choix entre ces différentes possibilités est motivé par un certain nombre de critères cliniques:
- Danger de la tachycardie pour le patient coronarien ;
- Action inotrope négative ;
- Action préférentielle sur la postcharge ou la précharge ;
- Effet sur les coronaires: augmentation du flux distal, risque de vol, durée d'action ;
- Simplicité d'administration et coût.
Les modifications du débit cardiaque dépendent de la fonction myocardique. La baisse des conditions de charge par la nitroglycérine entraîne une tachycardie réflexe chez le coeur normal mais non en cas d’insuffisance congestive; dans cette situation, la baisse de précharge soulage le ventricule. D’une manière générale, l'augmentation du débit par la baisse de la postcharge n'est significative que pour le coeur en insuffisance systolique, mais non pour le patient normal ni pour celui qui est en hypovolémie.
En cours de CEC, la situation est un peu particulière, puisque l'hypertension est exclusivement liée à une augmentation des résistances périphériques (hypothermie, dépulsation du flux, etc). Le coeur est hors-circuit et le débit est réglé par la pompe, dont la précharge dépend du retour veineux central. Il est aisé de calculer les résistances artérielles systémiques (RAS) à partir de l'équation standard : RAS = (PAM – PVC) x 80 / DC. En effet, on peut considérer que la PVC est nulle en CEC, et que le débit cardiaque est celui de la pompe (Dp), qui est connu. L'équation devient donc: RAS = (PAM x 80) / Dp. Le choix de l'hypotenseur se porte sur un médicament vasodilatateur artériel pur de courte durée d'action, par ordre de préférence:
- 1 - isoflurane, jusqu'à 5% ;
- 2 - phentolamine, jusqu'à 20 mg en doses fractionnées de 1 mg ;
- 3 - nitroprussiate en perfusion sur la voie centrale (risque toxique augmenté en hypothermie).
La nitroglycérine n'est efficace qu'à hautes doses et gêne le retour veineux vers la pompe, contraignant le perfusionniste à augmenter le volume circulant. Les β-bloqueurs n'ont pas de sens puisque le coeur est arrêté. Lorsqu’elle est indiquée pour une insuffisance ventriculaire réfractaire ou une hypertension pulmonaire, la dose de charge d’anti-phosphodiestérase-3 (milrinone 50 mg) administrée en CEC a un effet vasodilatateur puissant.
Sous anesthésie, on est tenté de régler une poussée hypertensive par un simple approfondissement du sommeil et de l'analgésie. Rappelons que cette technique est parfaitement adaptée à une légère hausse de pression chez les patients souffrant d'HTA modérée, mais qu'elle est inadéquate dès qu'il s'agit de contrôler une hypertension majeure. Dans ce cas, le traitement doit reposer sur des agents vasodilatateurs spécifiques. Chez les malades dont l'hémodynamique est fragile, d'autre part, il est risqué d'utiliser les agents d'anesthésie pour baisser la pression, car cette manœuvre s'accompagne d'effets hémodynamiques délétères, comme une chute du débit cardiaque, un effet inotrope négatif ou une insuffisance de précharge. Il est préférable de maintenir le sommeil et l'analgésie à un niveau adéquat en "autopilote" et de gérer séparément les problèmes tensionnels par des agents adaptés.
Cas particulier: le phéochromocytome
Le phéochromocytome est une tumeur du tissu chromaffine sécrétant des catécholamines, située habituellement dans la médullo-surrénale mais pouvant se localiser ailleurs dans la chaîne sympathique, ou rarement dans une paroi cardiaque. Selon la prédominance de l’hormone sécrétée, les malades présentent une hypertension artérielle (sécrétion de nor-adrénaline), ou des arythmies, des sudations et des accès de panique (sécrétion d’adrénaline et de dopamine). La sécrétion étant variable au cours du temps, la symptomatologie évolue en dent de scie. L’augmentation de postcharge induit une hypertrophie concentrique du VG, mais peut conduire à un épuisement du ventricule et à une cardiomyopathie dilatée.
L’excès de stimulation sympathique et l’intense sécrétion d’amines α et β s’accompagnent d’une hypovolémie chronique. La préparation préopératoire est essentielle [7].
- α-blocage: la phénoxybenzamine et la prazocine ne sont plus guère utilisées. Elles tendent à être remplacées par des anticalciques (nifédipine, nicardipine, diltiazem) qui inhibent les mouvements du calcium suscités par la nor-adrénaline dans la cellule musculaire lisse.
- β-blocage: indiqué en cas de palpitations, d’arythmies et d’hyperglycémie; en général combiné au blocage α.
- Blocage mixte α et β : labétalol (Trandate® per os et iv), carvédilol (Dilatrend® per os); très pratiques pour le traitement oral préopératoire, ces agents sont peu adaptés à la thérapeutique aiguë peropératoire, car on ne peut pas dissocier les effets α des effets β; de plus la durée d’action des deux effets n’est pas identique.
- Expansion du volume circulant par administration liquidienne sur une dizaine de jours.
- La préparation est adéquate lorsque la pression est stabilisée à < 160/90 mmHg sans hypotension orthostatique et que les extrasystoles sont < 1 par 5 minutes.
La phase peropératoire est caractérisée par trois éléments.
- Poussées massives de sécrétion catécholaminergique lors des manipulations chirurgicales de la tumeur;
- Hypertension, arythmies et hyperglycémie avant le clampage des veines qui drainent la tumeur;
- Hypotension et hypoglycémie dès que la veine est clampée, à cause de la chute brutale des catécholamines endogènes.
La prise en charge peropératoire est axée sur la gestion de l’hypertension très instable qui précède la résection tumorale et de l’hypotension qui peut s’en suivre [7].
- Perfusion continue de nitroprussiate; nitroglycérine en cas d’insuffisance congestive;
- Administration de phentolamine en bolus lors des poussées hypertensives;
- Administration d’esmolol en bolus ou en perfusion en cas d’arythmies, de tachycardie ou d’ischémie myocardique;
- Magnésium iv: hypotenseur et anti-arythmique d’appoint;
- Clévidipine: nouvel anti-calcique intra-veineux de très courte durée d’action (pic d’action en 2-4 minutes, demi-vie d’élimination de 15 minutes); perfusion de 1-2 mg/h augmentée progressivement jusqu’à 4-6 mg/h;
- Administration liquidienne généreuse.
Après la résection, il s’installe en général une période d’hypotension qui peut être assez réfractaire au traitement habituel (arrêt des hypotenseurs, administration liquidienne, néosynéphrine, nor-adrénaline) et réclamer un traitement plus agressif.
- Vasopressine: agit par une voie indépendante des récepteurs alpha; à pression artérielle égale, elle produit moins de vasoconstriction rénale, pulmonaire et coronaire que les autres vasopresseurs;
- Bleu de méthylène: agent de sauvetage dans les cas de vasoplégie intense.
| Anesthésie et HTA |
|
Le risque opératoire est lié aux lésions des organes-cibles (cerveau, cœur, reins) mais non à la valeur de la pression artérielle. L’HTA n’est pas une raison de renvoi de l’opération, sauf en cas d’hypertension maligne (PA ≥ 220/120 mmHg) symptomatique ou d’investigations nécessaires sur des lésions organiques pouvant modifier la prise en charge.
Les fluctuations peropératoires de la PA sont importantes, mais le risque est surtout associé à l’hypotension : ne pas laisser la PAM descendre à < 20% de sa valeur de base chez le patient.
Traitement de la crise hypertensive peropératoire :
- Phentolamine, bolus répétés 1 mg
- Uradipil, 10-20 mg iv en 30 secondes (+ perfusion 5-20 mg/h) - Nitroglycérine, bolus 20 mcg
- Nitroprussiate de Na, 0.3-3 mcg/kg/min
- Approfondissement de l’anesthésie/analgésie
- Isoflurane 5% (pour une courte durée exclusivement)
En cas d’ischémie myocardique associée:
- Nitroglycérine, perfusion 1-10 mcg/kg/min
- Esmolol, bolus répétés 10 mg
- Si spasmes coronariens : diltiazem 0.1-0.1 mg/kg/h
Même s'il peut être momentanément efficace, l'approfondissement de l'anesthésie n'est pas un traitement de l'HTA. La poussée hypertensive doit être gérée par des médicaments hypotenseurs spécifiques pour éviter les conséquences néfastes d'une anesthésie trop profonde.
Phéochromocytome : tumeur sécrétant majoritairement de la nor-adrénaline mais aussi de l’adrénaline et de la dopamine. Préparation préopératoire : labétalol, carvédilol, anti-calcique, expansion liquidienne.
En peropératoire :
- Avant la résection, hypotenseurs (nitroprussiate, phentolamine, clevidipine), β-bloqueur ;
- Poussées hypertensives lors des manipulations chirurgicales de la tumeur ;
- Après la résection : hypertenseurs, expansion liquidienne.
|
© CHASSOT PG, Septembre 2007, dernière mise à jour, Décembre 2018
Références
- CHARLSON ME, MACKENZIE CR, GOLD JP, et al. Intraoperative blood pressure: what patterns identify patients at risk for postoperative complications ? Ann Surg 1990; 212:567-80
- FOEX P, SEAR JW. The surgical hypertensive patient. Contin Educ Anaesth Crit Care Pain 2004; 4:139-43
- HOWELL SJ, SEAR JW, FOËX P. Hypertension, hypertensive heart disease and perioperative cardiac risk. Br J Anaesth 2004; 92:570-83
- HANADA S, KAWAKAMI H, GOTO T, et al. Hypertension and anesthesia. Curr Opin Anesthesiol 2006;19:315-9
- HARTLE A, McCORMACK T, CARLISLE J, et al. The measurement of adult blood pressure and management of hypertension before elective surgery. Joint Guidelines from the Association of Anaesthetists of Great Britain and Ireland and the British Hypertension Society. Anaesthesia 2016; 71:326-37
- LEWINGTON S, CLARKE R, QIZILBASH N, et al. Age-speciific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002; 360:1903-13
- LORD MS, AUGOUSTIDES JGT. Perioperative management of pheochromocytoma: focus on magnesium, clevidipine, and vasopressin. J Cardiothorac Vasc Anesth 2012; 26:526-31
- SPAHN DR, PRIEBE HJ. Preoperative hypertension: remain wary ? "Yes" – Cancel surgery ? "No". Br J Anaesth 2004; 92:461-3
- WEKSLER N, KLEIN M, SZENDRO G, et al. The dilemma of immediate preoperative hypertension: to treat and operate, or to postpone surgery ? J Clin Anesth 2003; 15:179-83
