L’importance d’une IM est tributaire des conditions hémodynamiques, particulièrement lorsqu’elle est de type I ou IIIb. Une quantification adéquate dépend donc de plusieurs éléments.
- Précharge, postcharge et fonction du VG normales: l’anesthésie, la ventilation en pression positive, la dysfonction ventriculaire, l’hypovolémie et l’hypotension diminuent l’IM; l'érétisme ventriculaire, l’hypervolémie et l’hypertension artérielle l’augmentent [9,12]. La quantification n'est adéquate que lorsque les conditions hémodynamiques sont voisines de la normalité pour le patient. Chez les malades arythmiques, notamment en cas de FA, il convient de moyenner les valeurs obtenues sur 3-5 cycles cardiaques de durée correspondant approximativement à un rythme de 60-70 batt/min.
- Utilisation de méthodes de mesure peu dépendantes de l’hémodynamique, telles les dimensions de l’orifice de régurgitation, le volume régurgité, le PISA ou la vena contracta.
- Durée de la régurgitation: le volume régurgité change si l'IM est holosystolique ou si elle n'apparaît qu'en proto- ou qu'en télé-systole. D'autre part, l'IM est dynamique et se modifie au cours de la systole; elle s'accentue en télésystole dans les prolapsus, mais diminue en mésosystole dans les IM secondaires. Les mesures basées sur des images à l'arrêt, comme la vena contracta ou le PISA, peuvent être trompeuses, alors que celle de l'intégrale des vélocités incorpore la durée totale du flux régurgité (équation de continuité).
- Faisceau de mesure Doppler dans l’axe de la fuite et à l’endroit de la vélocité maximale (au niveau de l’orifice de régurgitation). L'alignement est adéquat lorsque s'affichent simultanément sur la même image la zone d'accélération concentrique, le passage à travers l'orifice de régurgitation et la vena contracta; la zone tourbillonnaire distale se répand en-dehors de ce plan, particulièrement dans les IM excentriques (Figure 26.36).
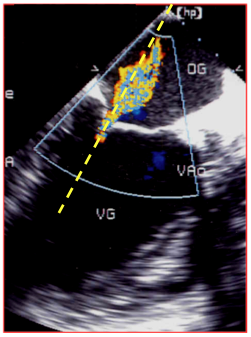
Figure 26.36 : Imagerie échocardiographique en mode Doppler d'une insuffisance mitrale en vue long-axe 120° du VG, qui offre souvent le meilleur alignement. Le faisceau Doppler (traitillé jaune) est bien dans l’axe du flux de l’IM représentée par le Doppler couleur; on voit dans le même plan la zone d'accélération concentrique côté ventriculaire, le passage à travers la valve et la vena contracta.
La morphologie du jet couleur dans l’OG fournit de bonnes indications sur le mécanisme de l’IM, mais sa dimension est un piètre critère de quantification, hormis les cas extrêmes, car elle est trop sensible à l’hémodynamique et aux réglages de l’appareil. D’autres mesures offrent davantage de précision parce qu'elles sont peu dépendantes des conditions d'examen (Vidéos et Figure 26.37) [31].
- Distance libre entre les feuillets (écart de coaptation);
- Mesure planimétrique de l’orifice de régurgitation en 3D;
- Vena contracta: zone de flux laminaire immédiatement distale à l'orifice de régurgitation (voir ci-dessous) [28,32];
- PISA (Proximal isovelocity surface area): zone de convergence de flux en amont de la régurgitation (voir ci-dessous) [22,23,25].
Vidéo: insuffisance mitrale centrale mineure-à-modérée.
Vidéo: insuffisance mitrale massive sur rupture du muscle papillaire antérieur.
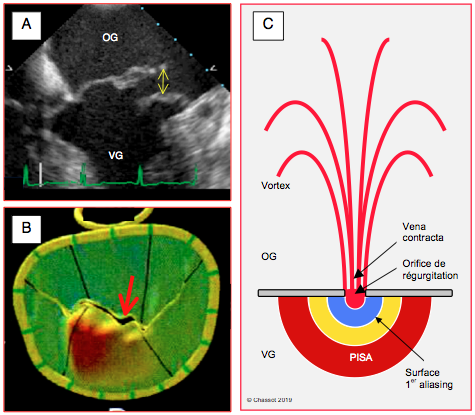
Figure 26.37 : Imagerie permettant la quantification d'une IM. A: Distance de non-occlusion de la valve mitrale en systole; la double flèche mesure la distance entre le feuillet antérieur et le feuillet postérieur dans ce prolapsus du feuillet antérieur. B: planimétrie de l'orifice de régurgitation en reconstruction 3D; l'orifice est une fente et non une surface circulaire comme le présupposent les calculs 2D. Le prolapsus est colorié en rouge. C: représentation schématique de la vena contracta (Vmax) et du PISA (hémisphère de 1er aliasing).
Mesure de l'orifice de régurgitation
La taille de l'orifice de régurgitation (OR) est un point essentiel dans la quantification de l'insuffisance mitrale, puisqu'elle est le principal déterminant de l'importance de la fuite. De plus, sa mesure est indépendante des conditions hémodynamiques (Vidéos).
- Distance libre entre les feuillets (écart de coaptation); elle est > 0.7 cm dans une IM sévère. L’orifice étant plus ou moins elliptique, la mesure doit se faire dans 2 plans orthogonaux.
- Mesure planimétrique de l’orifice de régurgitation en 3D; elle est la seule mesure réellement fiable de la surface de l'OR car elle tient parfaitement compte de sa forme, qui peut être elliptique, coudée, irrégulière ou en fente. Il faut toutefois que les images 2D de base soient d'excellente qualité.
- Mesure paramétrique de la surface des feuillets; la surface des deux feuillets est mesurée en systole, puis est recalculée après avoir redessiné la ligne de coaptation en excluant l'orifice de régurgitation. La surface de ce dernier est obtenue alors en soustrayant la première valeur de la deuxième. L'avantage est de ne pas dépendre d'un plan de section, notamment lorsque l'orifice présente une forme tridimensionnelle non-planaire (voir Figure 26.28) [5].
Vidéo: non-affrontement des feuillets mitraux en systole et recul du point de coaptation en arrière du plan de l'anneau mitral.
Vidéo: reconstruction 3D d'une insuffisance mitrale vue depuis l'OG; en systole, il persiste un orifice de non-coaptation (orifice de régurgitation) qui présente une forme en "8".
La surface de l'orifice de régurgitation (SOR) est le paramètre le plus robuste pour définir la sévérité de l'IM [16]. Les valeurs admises sont les suivantes.
- IM mineure: < 0.2 cm2 (Vrég < 30 mL)
- IM modérée: 0.2-0.4 cm2 (Vrég 30-55 mL)
- IM sévère: > 0.4 cm2 (Vrég > 60 mL)
En imagerie 2D conventionnelle, la SOR se calcule principalement à partir de la vena contracta et de la zone d'accélération hémisphérique du flux (PISA) (Figure 26.38).
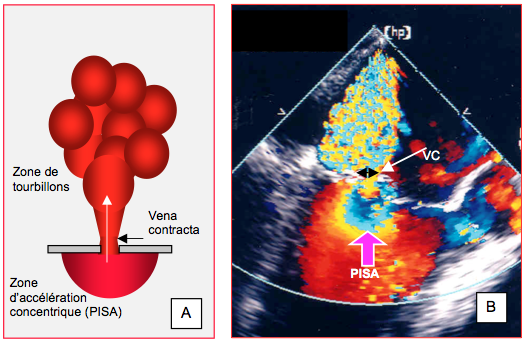
Figure 26.38 : Vena contracta et zone de convergence de flux. A : schéma des signes échocardiographiques Doppler couleur d’une IM sévère : large zone d'accélération intraventriculaire (PISA : Proximal isovelocity surface area), vena contracta (zone de flux laminaire immédiatement distale à l’orifice de régurgitation) de > 0.7 cm de diamètre, et vaste zone tourbillonnaire intra-auriculaire. B: le PISA est bien visible sous forme d'hémisphères concentriques; sa dimension est une traduction directe de l’importance de l’IM. La flèche violette marque la surface de 1er aliasing (passage du jaune au bleu). La flèche blanche indique la vena contracta (VC), et la double flèche noire le diamètre de celle-ci.
Vena contracta
Lorsqu'il franchit un passage rétréci, le flux s'accélère de manière laminaire et se contracte. La contraction maximale a lieu quelques millimètres au-delà de l'orifice, à un endroit appelé en hydrodynamique vena contracta (VC). Comme le flux sanguin y est encore laminaire, la surface de section de cette zone reproduit fidèlement la forme de l'orifice, mais elle est inférieure d'environ 15% à celle de l'orifice anatomique (GOA, geometrical orifice area). La mesure du diamètre de la vena contracta est une excellente technique pour évaluer la dimension de l’orifice effectif de régurgitation (EROA, effective regurgitant orifice area) (voi Chapitre 25, Echocardiographie Doppler). Il convient de moyenner 2-3 mesures effectuées dans deux plans orthogonaux pour obtenir une mesure cohérente. Les valeurs de diamètres sont : < 3 mm pour une IM mineure, 3-6 mm pour une IM modérée et ≥ 7 mm pour une IM primaire sévère [16,30]. La mesure est optimale lorsque le flux convergent proximal, l'orifice, la vena contracta et le jet intra-auriculaire sont alignés. Elle est valable pour les jets centraux et pour les jets excentriques, bien qu'elle soit plus délicate dans ces derniers.
Comme toutes les mesures réalisées sur une image immobilisée (still frame), celle de la vena contracta est tributaire de l'instant auquel a été stoppé le défilement. Les IM de type II (prolapsus) se renforcent au cours de la systole et sont maximales en télésystole, alors que les IM de type I et IIIb diminuent d'intensité en mésosystole; seules les IM de type IIIa (RAA) sont constantes. On surestime ainsi la régurgitation d'un prolapsus en évaluant sa vena contracta en fin de systole lorsqu'elle est la mieux formée.
Cette manière de procéder suppose que l'orifice de régurgitation est de symétrie circulaire. C'est grossièrement le cas dans les IM primaires, mais non dans les IM secondaires, parce que la valve n'y est pas déformée: l'orifice de régurgitation a la forme en croissant de la commissure mitrale normale, et l'assimilation à un cercle devient abusive. A défaut de balayer systématiquement la commissure dans la vue bi-commissurale à 40-60°, l'observation de tous les plans de coupe sous-estime donc l'importance de l'orifice en cas d'IM secondaire. De ce fait, la valeur retenue pour la définition d'une IM secondaire sévère est plus basse que pour celle d'une IM primaire: le diamètre de vena conttracta d'une IM ischémique sévère est une valeur > 4 mm, et non > 7 mm [16,30]. En présence de jets multiples, on ne peut pas additionner les différents diamètres pour obtenir une valeur totale. Pour pallier ces imprécisions, la reconstruction 3D du flux couleur permet de visualiser la section réelle de la vena contracta en opérant une découpe perpendiculaire au flux à l'endroit où il est le plus rétréci; la surface de la VC est alors bien corrélée à celle de l'orifice de régurgitation, notamment dans l'IM secondaire (Figure 26.39) [1,13]. Une IM sévère est définie par une surface de VC > 0.41 cm2. Comparée à la technique 3D, la mesure en 2D sous-estime la surface de la vena contracta de 27% [29].
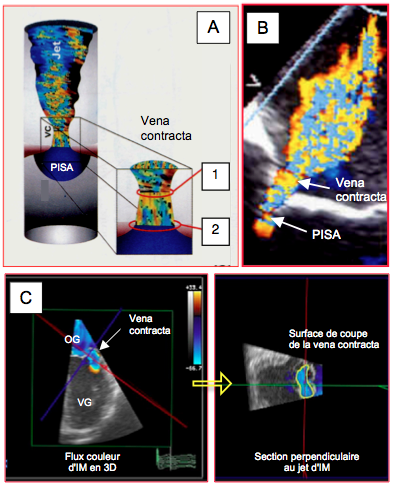
Figure 26.39 : Vena contracta (VC) illustrée dans une insuffisance mitrale en vue mi-oesophagienne rétrocardiaque. A : La section de la vena contracta (1) est un peu plus petite que celle de l'orifice anatomique (2). B: Insuffisance mitrale mineure-à-modérée: La vena contracta et la zone d'accélération concentrique (PISA) sont étroites. C: en imagerie tri-dimensionnelle, le Doppler couleur permet d'évaluer le jet d'IM dans l'espace et de mesurer sa surface dans une coupe perpendiculaire à son axe, à l'endroit où la section du jet est la plus petite, soit juste en aval de l'orifice. Dans le cas présent, la surface n'est pas circulaire mais elliptique et déformée, ce qui est typique des IM secondaires.
Zone de convergence du flux
La zone de convergence hémisphérique du flux correspond à la zone où les molécules de fluide doivent accélérer progressivement pour passer d’une cavité large, le VG, à un orifice étroit, le passage à travers la mitrale (Vidéos). Cette zone est d’autant plus grande que la quantité de liquide qui doit transiter par l’orifice est importante. Cette zone est appelée proximal isovelocity surface area, ou PISA, parce que la vitesse du fluide est la même sur toute la surface de chaque hémisphère concentrique successif [7].
Vidéo: zone d'accélération concentrique (PISA) côté ventriculaire d'une insuffisance mitrale centrale; en accélérant, le flux passe du rouge au jaune puis au bleu.
Vidéo: zone d'accélération concentrique dans une IM excentrique; bien que déformé, le jeu des couleurs est le même.
Selon l’équation de continuité, le produit de la vélocité (V) à la surface d’un hémisphère et de la surface (S) de cet hémisphère est égal au produit de la vélocité maximale (Vmax) à travers l’orifice de régurgitation (OR) et de la surface (SOR) de ce dernier, puisque tout le sang de chaque hémisphère passe à travers l'OR:
(S • V)Hémisphère = (SOR • Vmax)Orifice
Il est facile de mesurer la surface de l’hémisphère concentrique en repérant la limite à laquelle a lieu l’inversion de couleur du flux. Cette inversion (aliasing) survient lorsque la Vmax du flux dépasse celle qui est lisible pour l’échelle de couleur choisie (limite de Nyquist). Le choix de celle-ci est capital: la Vmax lisible doit être de 20-40 cm/s, obtenue préférentiellement en déplaçant la ligne de base de l'échelle couleur dans le sens du flux de régurgitation [11]. Le but est d'obtenir un rayon de 10-15 mm pour l'hémisphère de premier aliasing. Ce rayon permet de calculer la surface de ce dernier (SHémisph = 2 π, r2, soit 6.28 r2), et de là la surface de l'orifice de régurgitation (SOR) selon la formule (Figure 26.40):
SOR = (SHémisph • Valiasing) / VmaxIM
= (6.28 r2 • Valiasing) / VmaxIM
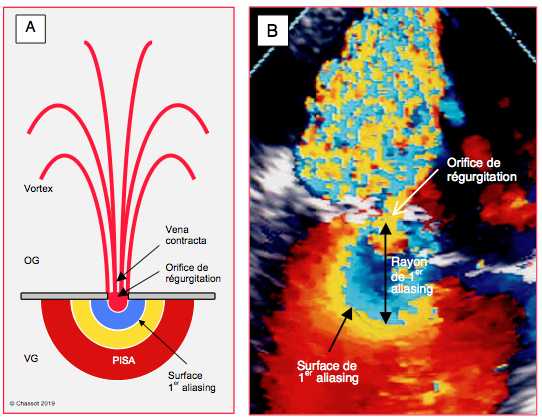
Figure 26.40 : PISA (Proximal isovelocity surface area). A : schéma du flux de régurgitation mitrale. B : mesure du rayon de 1er aliasing dans l’axe du faisceau Doppler dans le cas d’une IM sévère centrale et symétrique. Il va du centre de l'orifice de régurgitation à la surface de l'hémisphère de 1er aliasing; il est situé dans l'axe du flux et du faisceau Doppler.
La Vmax de l'IM doit être mesurée au même moment de la systole que la Vmax du premier aliasing. La définition du rayon de 1er aliasing bute souvent sur la difficulté de savoir précisément où se trouve l'orifice de régurgitation au milieu du flux couleur. Sur l'image gelée à l'écran, on peut le localiser plus facilement en soustrayant momentanément la couleur pour retrouver l'image bidimensionnelle. Le rayon du PISA doit se situer dans l'axe du flux et dans l'axe du faisceau Doppler; la précision de sa mesure est importante car celle-ci est élevée au carré dans le calcul. Dans les IM excentriques, la mesure est moins précise car la configuration géométrique est plus complexe; d'autre part, l'axe du flux se modifie et celui de la vena contracta, lieu de la Vmax, n'est souvent pas dans l'axe du faisceau Doppler. Lorsque les feuillets forment un cône en systole, le PISA n’est plus hémisphérique mais rétréci par l’angle (α) formé par les feuillets ; il faut alors corriger la formule de la surface de l’orifice de régurgitation pour cet angle: SOR = (6.28 r2 • Valiasing / VmaxIM) • α/180 (Figure 26.41).
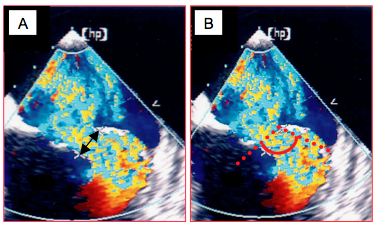
Figure 26.41 : PISA (Proximal isovelocity surface area). A : IM excentrique ; le PISA est décentré et son rayon difficile à mesurer ; la vena contracta n'est pas dans l'axe des ultrasons, mais son diamètre (double flèche noire) reste une manière fiable de mesurer la sévérité de l’IM. B : lorsque les feuillets forment un cône en systole, le PISA n’est plus hémisphérique mais rétréci par l’angle formé par les feuillets ; correction de la surface de l’orifice de régurgitation (SOR) : SOR = (6.28 r2 • Valiasing / VmaxIM) • α / 180.
A partir de la surface de l'orifice de régurgitation (SOR), il est aisé d'obtenir le volume de régurgitation (Vrég) en multipliant celle-ci par l'intégrale des vélocités de l'IM (ITV):
Vrég (cm3) = SOR (cm2) • ITVIM (cm)
En clinique, on peut utiliser une simplification: si l’échelle de couleur est réglée sur une vélocité d’aliasing de 40 cm/s, un rayon de 1 cm pour l’hémisphère de 1er aliasing équivaut à un orifice de régurgitation ≥ 0.5 cm2 (SOR = r2/2), ce qui correspond à une IM sévère [18,30]. Dans les IM secondaires, le seuil est plus bas car le PISA n'est pas hémisphérique ni ellipsoïde mais de volume variable en fonction de la forme de la commissure. La simple mesure du rayon de PISA sousestime l'importance de l'IM. Dans ce cas, l'IM est considérée comme sévère lorsque la SOR est > 0.2 cm2 et le Vrég > 30 mL. L'analyse du flux couleur en 3D montre en effet que le PISA réel est plus grand que celui visualisé en vue 2D dans l'IM secondaire; il en est de même pour la surface de régurgitation calculée [1]. Mais lorsque les mesures sont exécutées en 3D, on tend maintenant à prendre les mêmes critères de sévérité que pour les IM primaires [14,20].
Malgré ses performances, le calcul de la SOR et du Vrég dérivé du PISA dépend de la mesure unidimensionnelle d'un élément tridimensionnel, réalisée à un instant précis de la systole alors que le phénomène varie au cours de l'éjection (voir IM secondaire). Comme tout Doppler couleur, la mesure est influencée par l'échelle couleur (en l'occurrence 20-40 cm/s), la ligne de base (déplacée dans le sens du flux), l'échelle des gris (en l'occurance 50%) et l'angle entre le flux et l'axe d'analyse [6]. D'autres limitations sont encore à prendre en compte: faible précision dans les IM excentriques, difficulté à définir la localisation de l'orifice mitral au milieu du flux couleur, élévation au carré d'une erreur sur la mesure du rayon, géométrie du PISA modifiée par les structures adjacentes, synchronisation supposée entre la Vmax de l'IM et la Vmax du PISA [4,10]. D'autre part, l'instant de la systole choisi pour la mesure a son importance, car le volume du PISA varie pendant la phase d'éjection: il augmente progressivement jusqu'en télésystole dans les IM primaires comme les prolapsus, mais dans les IM secondaires il diminue en mésosystole, entre deux renforcements proto- et télésystoliques (voir Figure 26.42). Les mesures faites sur l'image de plus grande intensité tendent donc à surestimer l'importance de la régurgitation [30]. Enfin, la forme de l'orifice est supposée circulaire, alors qu'à l'imagerie 3D elle est plutôt elliptique dans les IM primaires et en fente dans les IM secondaires. De ce fait, le PISA sousestime la SOR de 10-25% par rapport à l'IRM, et d'environ 0.1 cm2 par rapport à la mesure 3D de la vena contracta [3,29]. Outre l'automaticité des calculs, les nouvelles plateformes d'écho 3D commencent à disposer d'algorithmes de reconnaissance de forme permettant de calculer automatiquement la SOR et le Vrég à partir du PISA et de limiter ainsi les marges d'erreur dans ces mesures.
Mesures volumétriques
Alors que l'intensité de l'insuffisance mitrale varie au cours de la systole, les mesures de la vena contracta et du PISA sont réalisées à un instant isolé sur une image gelée [4]. L'intérêt des mesures du volume de régurgitation (Vrég) est précisément de prendre en compte toute la durée de la systole. Intégrer le flux total augmente donc la fiabilité des mesures.
Comme mentionné précédemment, on obtient le Vrég à partir de la surface de l'orifice de régurgitation (SOR du PISA) en multipliant celle-ci par l'intégrale des vélocités de l'IM (ITV):
Vrég (cm3) = SOR (cm2) • ITVIM (cm)
La surface de l'orifice de régurgitation peut être calculée de manière plus adéquate à partir de sa surface de section par planimétrie 3D. En rapportant le Vrég au volume total qui transite par la valve mitrale en diastole (Vmitr), on obtient la fraction de régurgitation (Frég, en %).
Frég (%) = (Vrég / Vmitr) • 100
Le volume du flux mitral diastolique (Vmitr) est obtenu en multipliant la surface de l'anneau mitral (SAM) par l'intégrale des vélocités (ITVVM) du flux mitral mesuré au niveau de l'anneau au Doppler pulsé:
Vmitr = (S1 + S2 / 2)AM • ITVVM.
La surface de l'anneau mitral (AM) est obtenue en moyennant celle calculée à partir du diamètre (d) en vue bicommissurale 60° (S1) et en vue long-axe 140° (S2) par la formule: S = 0.785 d2. Toutefois, la mesure de volume du flux mitral est biaisée par la difficulté à obtenir une mesure fiable de la surface annulaire de la valve et par l'imprécision liée à l'emplacement du volume d'échantillonnage du Doppler pulsé.
Comme elle permet une définition correcte du volume des chambres cardiaques, l'imagerie 3D peut calculer le Vrég à partir du volume systolique total du VG (Vtd – Vts), comprenant l'éjection antérograde dans l'aorte et l'éjection rétrograde à travers la valve mitrale, dont est soustrait le volume systolique mesuré dans la CCVG (SCCVG • ITVCCVG) [11]. La SCCVG est mesurée par planimétrie 3D et l'ITVCCVG par Doppler pulsé (voie transgastrique).
Pour mieux percevoir la signification de l'insuffisance, on peut rapporter le volume régurgité au volume télédiastolique du VG (Vrég/VtdVG); en effet, le même Vrég représente une fraction de régurgitation (Vrég/VS) très différente selon le degré de dilatation du VG et le volume systolique total [21]. La relation entre la surface S de l'OR et le volume de régurgitation n'est pas linéaire, parce que la première est évaluée à un instant précis de la systole alors que le second représente le volume écoulé pendant la durée totale de celle-ci.
IM sévère
Les critères quantitatifs pour une IM primaire sévère (anciennement degré IV) peuvent se résumer comme suit (Tableau 26.2) [19,30].

Figure 26.38 : Vena contracta et zone de convergence de flux. A : schéma des signes échocardiographiques Doppler couleur d’une IM sévère : large zone d'accélération intraventriculaire (PISA : Proximal isovelocity surface area), vena contracta (zone de flux laminaire immédiatement distale à l’orifice de régurgitation) de > 0.7 cm de diamètre, et vaste zone tourbillonnaire intra-auriculaire. B: le PISA est bien visible sous forme d'hémisphères concentriques; sa dimension est une traduction directe de l’importance de l’IM. La flèche violette marque la surface de 1er aliasing (passage du jaune au bleu). La flèche blanche indique la vena contracta (VC), et la double flèche noire le diamètre de celle-ci.
Vena contracta
Lorsqu'il franchit un passage rétréci, le flux s'accélère de manière laminaire et se contracte. La contraction maximale a lieu quelques millimètres au-delà de l'orifice, à un endroit appelé en hydrodynamique vena contracta (VC). Comme le flux sanguin y est encore laminaire, la surface de section de cette zone reproduit fidèlement la forme de l'orifice, mais elle est inférieure d'environ 15% à celle de l'orifice anatomique (GOA, geometrical orifice area). La mesure du diamètre de la vena contracta est une excellente technique pour évaluer la dimension de l’orifice effectif de régurgitation (EROA, effective regurgitant orifice area) (voi Chapitre 25, Echocardiographie Doppler). Il convient de moyenner 2-3 mesures effectuées dans deux plans orthogonaux pour obtenir une mesure cohérente. Les valeurs de diamètres sont : < 3 mm pour une IM mineure, 3-6 mm pour une IM modérée et ≥ 7 mm pour une IM primaire sévère [16,30]. La mesure est optimale lorsque le flux convergent proximal, l'orifice, la vena contracta et le jet intra-auriculaire sont alignés. Elle est valable pour les jets centraux et pour les jets excentriques, bien qu'elle soit plus délicate dans ces derniers.
Comme toutes les mesures réalisées sur une image immobilisée (still frame), celle de la vena contracta est tributaire de l'instant auquel a été stoppé le défilement. Les IM de type II (prolapsus) se renforcent au cours de la systole et sont maximales en télésystole, alors que les IM de type I et IIIb diminuent d'intensité en mésosystole; seules les IM de type IIIa (RAA) sont constantes. On surestime ainsi la régurgitation d'un prolapsus en évaluant sa vena contracta en fin de systole lorsqu'elle est la mieux formée.
Cette manière de procéder suppose que l'orifice de régurgitation est de symétrie circulaire. C'est grossièrement le cas dans les IM primaires, mais non dans les IM secondaires, parce que la valve n'y est pas déformée: l'orifice de régurgitation a la forme en croissant de la commissure mitrale normale, et l'assimilation à un cercle devient abusive. A défaut de balayer systématiquement la commissure dans la vue bi-commissurale à 40-60°, l'observation de tous les plans de coupe sous-estime donc l'importance de l'orifice en cas d'IM secondaire. De ce fait, la valeur retenue pour la définition d'une IM secondaire sévère est plus basse que pour celle d'une IM primaire: le diamètre de vena conttracta d'une IM ischémique sévère est une valeur > 4 mm, et non > 7 mm [16,30]. En présence de jets multiples, on ne peut pas additionner les différents diamètres pour obtenir une valeur totale. Pour pallier ces imprécisions, la reconstruction 3D du flux couleur permet de visualiser la section réelle de la vena contracta en opérant une découpe perpendiculaire au flux à l'endroit où il est le plus rétréci; la surface de la VC est alors bien corrélée à celle de l'orifice de régurgitation, notamment dans l'IM secondaire (Figure 26.39) [1,13]. Une IM sévère est définie par une surface de VC > 0.41 cm2. Comparée à la technique 3D, la mesure en 2D sous-estime la surface de la vena contracta de 27% [29].

Figure 26.39 : Vena contracta (VC) illustrée dans une insuffisance mitrale en vue mi-oesophagienne rétrocardiaque. A : La section de la vena contracta (1) est un peu plus petite que celle de l'orifice anatomique (2). B: Insuffisance mitrale mineure-à-modérée: La vena contracta et la zone d'accélération concentrique (PISA) sont étroites. C: en imagerie tri-dimensionnelle, le Doppler couleur permet d'évaluer le jet d'IM dans l'espace et de mesurer sa surface dans une coupe perpendiculaire à son axe, à l'endroit où la section du jet est la plus petite, soit juste en aval de l'orifice. Dans le cas présent, la surface n'est pas circulaire mais elliptique et déformée, ce qui est typique des IM secondaires.
Zone de convergence du flux
La zone de convergence hémisphérique du flux correspond à la zone où les molécules de fluide doivent accélérer progressivement pour passer d’une cavité large, le VG, à un orifice étroit, le passage à travers la mitrale (Vidéos). Cette zone est d’autant plus grande que la quantité de liquide qui doit transiter par l’orifice est importante. Cette zone est appelée proximal isovelocity surface area, ou PISA, parce que la vitesse du fluide est la même sur toute la surface de chaque hémisphère concentrique successif [7].
Vidéo: zone d'accélération concentrique (PISA) côté ventriculaire d'une insuffisance mitrale centrale; en accélérant, le flux passe du rouge au jaune puis au bleu.
Vidéo: zone d'accélération concentrique dans une IM excentrique; bien que déformé, le jeu des couleurs est le même.
Selon l’équation de continuité, le produit de la vélocité (V) à la surface d’un hémisphère et de la surface (S) de cet hémisphère est égal au produit de la vélocité maximale (Vmax) à travers l’orifice de régurgitation (OR) et de la surface (SOR) de ce dernier, puisque tout le sang de chaque hémisphère passe à travers l'OR:
(S • V)Hémisphère = (SOR • Vmax)Orifice
Il est facile de mesurer la surface de l’hémisphère concentrique en repérant la limite à laquelle a lieu l’inversion de couleur du flux. Cette inversion (aliasing) survient lorsque la Vmax du flux dépasse celle qui est lisible pour l’échelle de couleur choisie (limite de Nyquist). Le choix de celle-ci est capital: la Vmax lisible doit être de 20-40 cm/s, obtenue préférentiellement en déplaçant la ligne de base de l'échelle couleur dans le sens du flux de régurgitation [11]. Le but est d'obtenir un rayon de 10-15 mm pour l'hémisphère de premier aliasing. Ce rayon permet de calculer la surface de ce dernier (SHémisph = 2 π, r2, soit 6.28 r2), et de là la surface de l'orifice de régurgitation (SOR) selon la formule (Figure 26.40):
SOR = (SHémisph • Valiasing) / VmaxIM
= (6.28 r2 • Valiasing) / VmaxIM

Figure 26.40 : PISA (Proximal isovelocity surface area). A : schéma du flux de régurgitation mitrale. B : mesure du rayon de 1er aliasing dans l’axe du faisceau Doppler dans le cas d’une IM sévère centrale et symétrique. Il va du centre de l'orifice de régurgitation à la surface de l'hémisphère de 1er aliasing; il est situé dans l'axe du flux et du faisceau Doppler.
La Vmax de l'IM doit être mesurée au même moment de la systole que la Vmax du premier aliasing. La définition du rayon de 1er aliasing bute souvent sur la difficulté de savoir précisément où se trouve l'orifice de régurgitation au milieu du flux couleur. Sur l'image gelée à l'écran, on peut le localiser plus facilement en soustrayant momentanément la couleur pour retrouver l'image bidimensionnelle. Le rayon du PISA doit se situer dans l'axe du flux et dans l'axe du faisceau Doppler; la précision de sa mesure est importante car celle-ci est élevée au carré dans le calcul. Dans les IM excentriques, la mesure est moins précise car la configuration géométrique est plus complexe; d'autre part, l'axe du flux se modifie et celui de la vena contracta, lieu de la Vmax, n'est souvent pas dans l'axe du faisceau Doppler. Lorsque les feuillets forment un cône en systole, le PISA n’est plus hémisphérique mais rétréci par l’angle (α) formé par les feuillets ; il faut alors corriger la formule de la surface de l’orifice de régurgitation pour cet angle: SOR = (6.28 r2 • Valiasing / VmaxIM) • α/180 (Figure 26.41).

Figure 26.41 : PISA (Proximal isovelocity surface area). A : IM excentrique ; le PISA est décentré et son rayon difficile à mesurer ; la vena contracta n'est pas dans l'axe des ultrasons, mais son diamètre (double flèche noire) reste une manière fiable de mesurer la sévérité de l’IM. B : lorsque les feuillets forment un cône en systole, le PISA n’est plus hémisphérique mais rétréci par l’angle formé par les feuillets ; correction de la surface de l’orifice de régurgitation (SOR) : SOR = (6.28 r2 • Valiasing / VmaxIM) • α / 180.
A partir de la surface de l'orifice de régurgitation (SOR), il est aisé d'obtenir le volume de régurgitation (Vrég) en multipliant celle-ci par l'intégrale des vélocités de l'IM (ITV):
Vrég (cm3) = SOR (cm2) • ITVIM (cm)
En clinique, on peut utiliser une simplification: si l’échelle de couleur est réglée sur une vélocité d’aliasing de 40 cm/s, un rayon de 1 cm pour l’hémisphère de 1er aliasing équivaut à un orifice de régurgitation ≥ 0.5 cm2 (SOR = r2/2), ce qui correspond à une IM sévère [18,30]. Dans les IM secondaires, le seuil est plus bas car le PISA n'est pas hémisphérique ni ellipsoïde mais de volume variable en fonction de la forme de la commissure. La simple mesure du rayon de PISA sousestime l'importance de l'IM. Dans ce cas, l'IM est considérée comme sévère lorsque la SOR est > 0.2 cm2 et le Vrég > 30 mL. L'analyse du flux couleur en 3D montre en effet que le PISA réel est plus grand que celui visualisé en vue 2D dans l'IM secondaire; il en est de même pour la surface de régurgitation calculée [1]. Mais lorsque les mesures sont exécutées en 3D, on tend maintenant à prendre les mêmes critères de sévérité que pour les IM primaires [14,20].
Malgré ses performances, le calcul de la SOR et du Vrég dérivé du PISA dépend de la mesure unidimensionnelle d'un élément tridimensionnel, réalisée à un instant précis de la systole alors que le phénomène varie au cours de l'éjection (voir IM secondaire). Comme tout Doppler couleur, la mesure est influencée par l'échelle couleur (en l'occurrence 20-40 cm/s), la ligne de base (déplacée dans le sens du flux), l'échelle des gris (en l'occurance 50%) et l'angle entre le flux et l'axe d'analyse [6]. D'autres limitations sont encore à prendre en compte: faible précision dans les IM excentriques, difficulté à définir la localisation de l'orifice mitral au milieu du flux couleur, élévation au carré d'une erreur sur la mesure du rayon, géométrie du PISA modifiée par les structures adjacentes, synchronisation supposée entre la Vmax de l'IM et la Vmax du PISA [4,10]. D'autre part, l'instant de la systole choisi pour la mesure a son importance, car le volume du PISA varie pendant la phase d'éjection: il augmente progressivement jusqu'en télésystole dans les IM primaires comme les prolapsus, mais dans les IM secondaires il diminue en mésosystole, entre deux renforcements proto- et télésystoliques (voir Figure 26.42). Les mesures faites sur l'image de plus grande intensité tendent donc à surestimer l'importance de la régurgitation [30]. Enfin, la forme de l'orifice est supposée circulaire, alors qu'à l'imagerie 3D elle est plutôt elliptique dans les IM primaires et en fente dans les IM secondaires. De ce fait, le PISA sousestime la SOR de 10-25% par rapport à l'IRM, et d'environ 0.1 cm2 par rapport à la mesure 3D de la vena contracta [3,29]. Outre l'automaticité des calculs, les nouvelles plateformes d'écho 3D commencent à disposer d'algorithmes de reconnaissance de forme permettant de calculer automatiquement la SOR et le Vrég à partir du PISA et de limiter ainsi les marges d'erreur dans ces mesures.
Mesures volumétriques
Alors que l'intensité de l'insuffisance mitrale varie au cours de la systole, les mesures de la vena contracta et du PISA sont réalisées à un instant isolé sur une image gelée [4]. L'intérêt des mesures du volume de régurgitation (Vrég) est précisément de prendre en compte toute la durée de la systole. Intégrer le flux total augmente donc la fiabilité des mesures.
Comme mentionné précédemment, on obtient le Vrég à partir de la surface de l'orifice de régurgitation (SOR du PISA) en multipliant celle-ci par l'intégrale des vélocités de l'IM (ITV):
Vrég (cm3) = SOR (cm2) • ITVIM (cm)
La surface de l'orifice de régurgitation peut être calculée de manière plus adéquate à partir de sa surface de section par planimétrie 3D. En rapportant le Vrég au volume total qui transite par la valve mitrale en diastole (Vmitr), on obtient la fraction de régurgitation (Frég, en %).
Frég (%) = (Vrég / Vmitr) • 100
Le volume du flux mitral diastolique (Vmitr) est obtenu en multipliant la surface de l'anneau mitral (SAM) par l'intégrale des vélocités (ITVVM) du flux mitral mesuré au niveau de l'anneau au Doppler pulsé:
Vmitr = (S1 + S2 / 2)AM • ITVVM.
La surface de l'anneau mitral (AM) est obtenue en moyennant celle calculée à partir du diamètre (d) en vue bicommissurale 60° (S1) et en vue long-axe 140° (S2) par la formule: S = 0.785 d2. Toutefois, la mesure de volume du flux mitral est biaisée par la difficulté à obtenir une mesure fiable de la surface annulaire de la valve et par l'imprécision liée à l'emplacement du volume d'échantillonnage du Doppler pulsé.
Comme elle permet une définition correcte du volume des chambres cardiaques, l'imagerie 3D peut calculer le Vrég à partir du volume systolique total du VG (Vtd – Vts), comprenant l'éjection antérograde dans l'aorte et l'éjection rétrograde à travers la valve mitrale, dont est soustrait le volume systolique mesuré dans la CCVG (SCCVG • ITVCCVG) [11]. La SCCVG est mesurée par planimétrie 3D et l'ITVCCVG par Doppler pulsé (voie transgastrique).
Pour mieux percevoir la signification de l'insuffisance, on peut rapporter le volume régurgité au volume télédiastolique du VG (Vrég/VtdVG); en effet, le même Vrég représente une fraction de régurgitation (Vrég/VS) très différente selon le degré de dilatation du VG et le volume systolique total [21]. La relation entre la surface S de l'OR et le volume de régurgitation n'est pas linéaire, parce que la première est évaluée à un instant précis de la systole alors que le second représente le volume écoulé pendant la durée totale de celle-ci.
IM sévère
Les critères quantitatifs pour une IM primaire sévère (anciennement degré IV) peuvent se résumer comme suit (Tableau 26.2) [19,30].
- Ecartement des feuillets > 0.7 cm ou bascule de feuillet dans l’OG;
- Surface du flux couleur > 40% surface de l’OG si l’IM est centrale; le jet atteint la paroi postérieure de l’OG (seulement si l'hémodynamique est normale et si le jet est central);
- PISA ≥ 1 cm (rayon 1er aliasing si Valias 0.4 m/s);
- Largeur du jet à la vena contracta > 0.7 cm;
- Reflux systolique dans les veines pulmonaires (peut être absent);
- Surface de l’orifice de régurgitation ≥ 0.4 cm2;
- Volume régurgité ≥ 60 mL;
- Fraction de régurgitation > 45%.

Ces mesures sont réalisées en mésosystole et dans des conditions hémodynamiques normales (normovolémie, normotension et fonction sastisfaisante). Il faut éviter de se déterminer sur un seul facteur, car c’est la convergence d’un faisceau de données qui permet de définir l’importance de l’IM. Lorsqu’elle est chronique, l’IM entraîne un important remodelage des structures cardiaques : hypertrophie dilatative du VG (diamètre télésystolique > 4.0 cm), dilatation de l’anneau mitral, dilatation de l’OG (> 60 mL/m2), élévation de la PAP (PAPsyst > 50 mmHg) [17,27]. En cas d’IM multiples, on peut additionner la surface des différents orifices de régurgitation, mais non les autres mesures [32].
IM aiguë
Le remodelage caractéristique des cavités cardiaques est absent dans une IM aiguë survenant lors d’une rupture de cordage ou de pilier, d’une endocardite ou d’une ischémie étendue. Face à la surcharge de volume, le VG augmente son débit par tachycardie. La dysfonction ventriculaire gauche qui accompagne en général l’évènement diminue la vélocité du jet couleur. Outre la tachycardie et le choc cardiogène, l’IM aiguë présente des caractéristiques particulières [30,31,32].
- Cavités de taille normale, OG non agrandie et peu compliante.
- Augmentation importante de la pression dans l'OG.
- Rupture de cordage ou de pilier, bascule de feuillet, restriction majeure, déchirure ou orifice d’endocardite.
- Etendue et vélocité du jet d’IM diminuées à cause du large orifice, de la dysfonction importante du VG et de l’élévation de la pression dans l’OG. Le jet de l’IM est de si basse vélocité qu’il peut ne pas donner de tourbillons dans l’OG. La taille du PISA n’est pas fiable.
- Volume régurgité relativement faible à cause de la rapide égalisation des pressions entre le VG et l'OG.
- La dimension de la vena contracta est fiable (vélocité 1 – 4 m/s).
- Reflux systolique important dans les veines pulmonaires (examen à droite et à gauche).
Synthèse
Pour résumer, l’insuffisance mitrale sévère est caractérisée par les critères suivants (voir Tableau 26.2) [2,8,15,16,19,30].
Pour résumer, l’insuffisance mitrale sévère est caractérisée par les critères suivants (voir Tableau 26.2) [2,8,15,16,19,30].
- Dilatation du VG (diamètre télédiastolique en court-axe > 4 cm/m2) (absente si IM aiguë);
- Dilatation de l’OG (diamètre > 5 cm) (absente si IM aiguë);
- Non-coaptation des feuillets ou bascule d’un feuillet en systole;
- Jet de régurgitation traversant toute l’OG (Doppler couleur);
- Diamètre du jet de régurgitation à son origine (vena contracta) ≥ 0.7 cm;
- Large zone de convergence de flux intraventriculaire (PISA) : rayon de 1er aliasing > 1.0 cm (échelle de couleur 0.4 m/s);
- Orifice de régurgitation > 0.4 cm2;
- Volume régurgité ≥ 60 mL (cette donnée a la meilleure corrélation avec le pronostic clinique);
- Fraction de régurgitation > 45%;
- Reflux systolique dans les veines pulmonaires (inconstant);
- PAPsyst > 50 mmHg (> 60 mmHg à l'effort).
Les critères de sévérité sont plus restrictifs pour l'insuffisance secondaire, parce que celle-ci traduit une pathologie ventriculaire grave. D'autre part, les mesures sont moins fiables parce que l'IM secondaire ne présente pas la symétrie circulaire fréquente dans les IM primaires. Une IM ischémique ou dilatative est donc considérée comme sévère lorsque les critères suivants sont remplis [10].
- Diamètre de la vena contracta > 0.4 cm;
- Orifice de régurgitation > 0.2 cm2;
- Volume régurgité > 30 mL;
- Fraction de régurgitation > 30%.
Le diagnostic et la quantification de l'IM se base sur un bouquet de données convergentes et non sur un seul élément qui pourrait être trompeur. Les critères les plus fiables sont ceux qui dépendent le moins des conditions hémodynamiques, tels l'imagerie 2D et 3D, le diamètre de la vena contracta, la taille de la zone d'accélération (PISA) et la surface de l'orifice de régurgitation [9,26]. Dans les insuffisances aiguës, la morphologie de l'OG et du VG n'est pas modifiée; le remodelage est absent, sauf si l'IM aiguë est un accident évolutif dans le cours d'une lésion chronique. Pour être fiables, les différentes mesures doivent respecter certaines conditions.
- L'hémodynamique est stable, la PA et le débit cardiaque sont normaux;
- Les mesures bidimensionnelles sont réalisées dans plusieurs plans;
- Les mesures basées sur les flux sont faites dans une vue où l’on identifie clairement le PISA et la vena contracta;
- Les mesures de flux et de PISA sont faites dans l’axe du Doppler;
- L’échelle des vélocités couleur (limite de Nyquist) est réglée de manière optimale.
L'ETO pratiqué en salle d'opération est souvent discordant par rapport à l'examen transthoracique effectué auparavant par le cardiologue. En effet, l'anesthésie générale et la ventilation en pression positive modifient considérablement la précharge et la postcharge du VG, au point que l'estimation du degré de sévérité de l'IM diminue de 25-30% sous AG [12]. L'étendue du jet couleur et le diamètre de la vena contracta sont significativement abaissés après l'induction, alors que la SOR et le Vrég sont peu modifiés. Un rétablissement de la postcharge par un vasoconstricteur (phényléphrine) augmente le Vrég sans modifier significativement la SOR [24]. On voit donc que l'AG diminue l'IM et que sa mesure tend à la sousestimer chez 40% des patients; malheureusement, le rétablissement artificiel de l'hémodynamique conduit à une surestimation de l'IM chez 20% des malades [724]. En chirurgie mitrale, cependant, le but de l'ETO peropératoire n'est pas tant de quantifier l'IM, ce qui présente une lourde marge d'erreur, mais de déterminer les bases anatomiques de la maladie, de définir les chances de réussite d'une plastie et de guider l'opérateur dans le choix de la technique (Tableau 26.3) [14].

| Quantification de l’IM |
| Conditions de base : - Hémodynamique normale - Mesures peu dépendantes de l’hémodynamique - Faisceau Doppler dans l’axe de la vena contracta - Mesures dans 2 plans orthogonaux Quantification - Ecart de coaptation IM sévère : > 0.7 cm - PISA IM sévère : r 1er aliasing ≥ 1 cm si échelle couleur = 0.4 m/s - Vena contracta (VC) IM sévère : diamètre ≥ 0.7 cm - Orifice de régurgitation (OR) IM sévère : S ≥ 0.4 cm2 - En cas d'IM secondaire IM sévère si VC > 0.4 cm, OR > 0.2 cm2, Vrég > 30 mL Modulation en fonction de : - Durée de l’IM et temps de la mesure au cours de la systole - Etendue de la fuite (localisée, pancommissurale) - Tendance à surestimer une IM centrale et une IM non holosystolique - Tendance à sous-estimer une IM excentrique et une IM secondaire (orifice non circulaire) - Marge d'erreur dans la mesure de l'orifice de régurgitation: 10-20% La quantification d'une IM doit impérativement se baser sur la synthèse d'une série de mesures et non sur une seule donnée. En cas de discordance, les connaissances acquises sur les mécanismes de l'IM et sur les risques de sous- ou de sur-estimation des différentes mesures permettent d'orienter le diagnostic. La distinction entre une IM sévère et une IM modérée est aisée, mais la différence entre une IM modérée et une IM mineure est beaucoup moins tranchée. IM mineure: - Jet couleur central et petit - Feuillets normaux ou peu déformés - Diamètre de vena contracta < 0.3 cm - Absence de PISA - Flux mitral de type E < A IM sévère: - Jet couleur majeur ou excentrique, holosystolique - Feuillets pathologiques si IM primaire (bascule, rutpure cordage/pilier, rétraction sévère) - Diamètre de vena contracta > 0.7 cm - PISA important - Facultatif: flux mitral E > 1.2 m/s, reflux systolique en veine pulmonaire - Dilatation de l'OG si IM chronique |
© CHASSOT PG, BETTEX D. Octobre 2011, Juin 2019; dernière mise à jour, Mars 2020
Références
- ASHIKHMINA E, SHOOK D, COBEY F, et al. Three-dimensional versus two-dimensional echocardiographic assessment of functional mitral regurgitation proximal isovelocity area. Anesth Analg 2015; 120:534-42
- BAUMGARTNER H, FALK V, BAX JJ, et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J 2017; 38:2739-86
- BINER S, RAFIQUE A, RAFIL F, et al. Reproducibility of proximal isovelocity surface area, vena contracta, and regurgitant jet area for assessment of mitral regurgitation severity. JACC Cardiovasc Imaging 2010; 3:235-43
- CHERRY SV, JAIN P, RODRIGUEZ-BLANCO YF, FABBRO M. Noninvasive evaluation of native valvular regurgitation: a review of the 2017 American Society of Echocardiography Guidelines for the perioperative echocardiographer. J Cardiothorac Vasc Anesth 2018; 32:811-22
- COBEY FC, FERREIRA R, URSPRUNG WW, et al. A novel approach to assess the three-dimensional anatomy of a mitral valve regurgitant orifice. J Cardiothorac Vasc Anesth 2017; 31:169-73
- COBEY FC, PATEL V, GOSLING A, URSPRUNG E. The emperor has no clothes: recognizing the limits of current echocardiographic technology in perioperative quantification of mitral regurgitation. J Cardiothorac Vasc Anesth 2017; 31:1692-4
- ENRIQUEZ-SARANO M, MILLER FA, HAYES SN, et al. Effective mitral regurgitant orifice area: clinical use and pitfalls of the proximal isovelocity surface area method. J Am Coll Cardiol 1995; 25:703-9
- FOSTER E. Mitral regurugitation due to degenerative mitral-valve disease. N Engl J Med 2010; 363:156-65
- GISBERT A, SOULIERE V, DENAULT AY, et al. Dynamic quantitative echocardiographic evaluation of mitral regurgitation in the operating department. J Am Soc Echocardiogr 2006; 19:140-6
- GRAYBURN PA, CARABELLO B, HUNG J, et al. Defining "severe" secondary mitral regurgitation. Emphasizing an integrated approach. J Am Coll Cardiol 2014; 64:2792-801
- GRAYBURN PA, WEISSMAN NJ, ZAMORANO JL. Quantitation of mitral regurgitation. Circulation 2012; 126:2005-17
- GREWAL KS, MALKOWSKI MJ, PIRACHA AR, et al. Effect of general anesthesia on the severity of mitral regurgitation by transesoophageal echocardiography. Am J Cardiol 2000; 85:199-203
- GREWAL J, MANKAD S, FREEMAN WK. Real-time three-dimensional transesophageal echocardiography in the intraoperative assessment of mitral valve disease. J Am Soc Echocardiogr 2009; 22:34-41
- JAIN P, FABBRO M. ACC Expert Consensus Decision Pathway on the management of mitral regurgitation: A review of the 2017 document fot cardiac anesthesiologist. J Cardiothorac Vasc Anesth 2019; 33:274-89
- LANCELLOTTI P, MOURA L, AGRICOLA E, et al. European Association of Echocardiography recommendations for the assessment of valvular regurgitation. Part 2: mitral and tricuspid regurgitation (native valve disease). Eur J Echocardiogr 2010; 11:307-32
- LANCELLOTTI P, TRIBOUILLOY C, HAGENDORFF A, et al. Recommendations for the echocardiographic assessment of native valvular regurugitation: an executive summary from the EACI. Eur Heart J Cardiovasc Imaging 2013; 14:611-44
- LE TOURNEAU T, MESSIKA-ZEITOUN D, RUSSO A, et al. Impact of left atrial volume on clinical outcome in organic mitral regurgitation. J Am Coll Cardiol 2010; 56:570-8
- MATSUMARA Y, FUKUDA S, TRAN H. Geometry of the proximal isovelocity surface area in mitral regurgitation by 3-dimensional color Doppler echocardiography: difference between functional mitral regurgitation and prolapse regurgitation. Am Heart J 2008; 155:231-8
- NISHIMURA RA, OTTO CM, BONOW RO, et al. 2014 AHA/ACC Guideline for the management of patients with valvular heart disease. Circulation 2014; 129:e521-e643
- NISHIMURA RA, OTTO CM, BONOW RO, et al. 2017 AHA/ACC focused update of the 2014 AHA/ACC Guideline for the management of patients with valvular heart disease. J Am Coll Cardiol 2017; 70:252-89
- O'GARA PT, GRAYBURN PA, BADHWAR V, et al. 2017 ACC Expert consensus décision pathway on the management of mitral regurgitation. J Am Coll Cardiol 2017; 70:2421-49
- PU M, VANDERVOORT PM, GRIFFIN BP, et al. Quantification of mitral regurgitation by the proximal convergence method using transesophageal echocardiography. Clinical validation of a geometric correction for proximal flow constraint. Circulation 1995; 92:2169-77
- RYAN L, JACKSON B, PARISH L. Regional and global patterns of annular remodeling in ischemic mitral regurgitation. Ann Thorac Surg. 2007 Aug;84:553-9
- SANFILIPPO F, JOHNSON C, BELLAVIA D, et sl. Mitral regurgitation grading in the operating room: a systematic review and meta-analysisi comparing preoperative and intraoperative assessments during cardiac surgery. J Cardiothorac Vasc Anesth 2017; 31:1681-91
- SIMPSON IA, SHIOTA T, GHARIB M, et al. Current status of flow convergence for clinical applications: Is it a leaning tower of “PISA” ? J Am Coll Cardiol 1996; 27:504-9
- SUGENG L, CHANDRA S, LANG RM. Three-dimensional echocardiography for assessment of mitral valve regurgitation. Curr Opin Cardiol 2009; 24:420-5
- TRIBOUILLOY C, GRIGIONI F, AVIERINOS JF, et al. Survival implication of left ventricular end-systolic diameter in mitral regurgitation due to flail leaflets: a long-term follow-up multicenter study. J Am Coll Cardiol 2009; 54:1961-8
- TRIBOUILLOY C, SHEN WF, QUERE JP, et al. Assessment of severity of mitral regurgitation by measuring regurgitant jet width at its origin with transesophageal Doppler color flow imaging. Circulation 1992; 85:1248-53
- ZENG X, LEVINE RA, HUA I, et al. Diagnostic value of vena contracta area in the quantification of mitral regurgitation severity by color Doppler 3D echocardiography. Circ Cardiovasc Imaging 2011; 4:506-13
- ZOGHBI WA, ADAMS D, BONOW RO, et al. Recommendations for noninvasive evaluation of native valvular regurgitation: a report from the ASE developped in collaboration with the SCMR. J Am Soc Echocardiogr 2017; 30:303-71
- ZOGHBI WA, ENRIQUEZ-SARANO M, FOSTER E, et al. Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. Eur J Echocardiogr 2003; 4:237-61
- ZOGHBI WA, ENRIQUEZ-SARANO M, FOSTER E, et al. Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. J Am Soc Echocardiogr 2003; 16:777-802
