Endoprothèses vasculaires
Ponter un anévrysme, une rupture proximale de dissection ou une déchirure traumatique de manière non invasive avec une prothèse endovasculaire diminue les pertes sanguines, la morbidité et la durée du séjour hospitalier; elle améliore la stabilité hémodynamique, évite le clampage aortique et l'anticoagulation; elle autorise même l’anesthésie locale ou loco-régionale [1]. L’endoprothèse est un tube de Dacron armé, introduit replié autour d’un guide par voie généralement fémorale, et immobilisé en place dans l’aorte par auto-expansion ou par le gonflement d’un ballon (Vidéos). Pour être stable, la prothèse doit être ancrée proximalement et distalement sur du vaisseau sain; les collets d’ancrage doivent mesurer 1-2 cm de long, et ne pas dépasser 4 cm de diamètre. L’alignement entre le collet et l’anévrysme doit être satisfaisant (angulation < 60°); la prothèse doit être surdimensionnée de 10-15% par rapporte à l'aorte native [3,9]. Dans les cas de dissection, le choix de la taille est guidé par la seule mesure du collet proximal en amont de la rupture, car l'extrémité distale est située dans une zone qui inclut la vraie et la fausse lumière (Figure 27.126) [5,6].
Vidéo: largage d'une endoprothèse dans l'aorte descendante; le gonflement du ballon provoque l'expansion de la prothèse.
Vidéo: largage d'une endoprothèse dans l'aorte descendante.
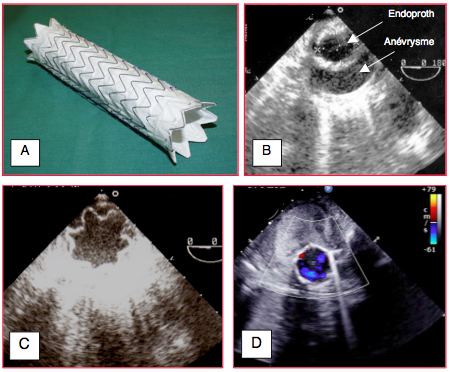
Figure 27.126 : Endoprothèse aortique. A : tube d’endoprothèse ; on voit le système d’ancrage aux deux extrémités. B : endoprothèse en court-axe dans l’aorte descendante, pontant une lésion anévrysmale. C: endoprothèse mal expandue; au vu de cette image, il faut ré-expandre la prothèse au moyen d'un ballon. D: flux normal dans une endoprothèse située à l'intérieur d'un gros anévrysme thrombosé.
L’ETO est d'un immense apport pour seconder l’opérateur au cours des manoeuvres de mise en place [6,8,10].
- Localisation de la lésion.
- Localisation de l’origine des gros vaisseaux.
- Identification de la vraie et de la fausse lumière.
- Appréciation de la zone d'implantation (diamètre, athéromes, coudure, etc).
- Repérage des orifices distaux qui doivent être couverts (longueur ou nombre de prothèses à implanter).
- Guidage du mandrin dans la vraie lumière pour éviter qu’il s’enroule dans un anévrysme ou s’introduise dans la fausse lumière, ce qui est le cas chez 28% des patients [7].
- Positionnement de la prothèse; obstruction éventuelle de la sous-clavière gauche et/ou de la carotide gauche, ce qui est souvent le cas dans les lésions traumatiques de l'isthme. Des pontages de substitution peuvent être réalisés depuis le tronc brachiocéphalique (voir Figures 18.49 et 18.52).
- Identification des endofuites.
- Contrôle de la disparition du flux dans la lésion exclue (limite de Nyquist 0.4 m/s), qui doit se remplir de contraste spontané immobile (Vidéo); la présence de mouvement fait suspecter une endofuite.
- L'ETO est performante lors d'implantation de prothèse en Dacron™ mais non en Gore-Tex™, car cette dernière substance est opaque aux ultrasons.
- L'ETO est limitée par la non-visualisation de la zone aorte ascendante distale - crosse proximale, et par la nécessité d'une anesthésie générale pour supporter la sonde, alors que beaucoup d'endoprothèses peuvent être mises en place sous anesthésie locale et sédation.
Vidéo: flux laminaire normal dans une endoprothèse aortique descendante.
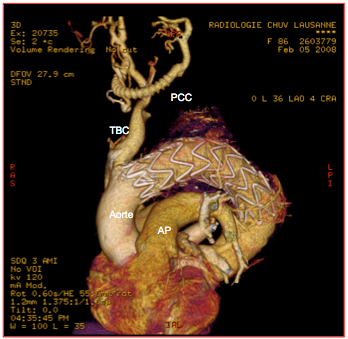
Figure 18.49 : Endoprothèse aortique mise en place dans la partie terminale de la crosse et la partie proximale de l’aorte descendante, pour occlure un anévrysme sacculaire de la crosse distale. Comme la prothèse couvre la sous-clavière gauche et la carotide commune gauche, un pontage carotido-carotidien (PCC) extrathoracique avec un tube en Dacron armé a été réalisé en premier lieu. TBC : tronc brachio-céphalique. Dans ce cas, l’anesthésie a été réalisée par un bloc cervical superficiel bilatéral et une infiltration fémorale.
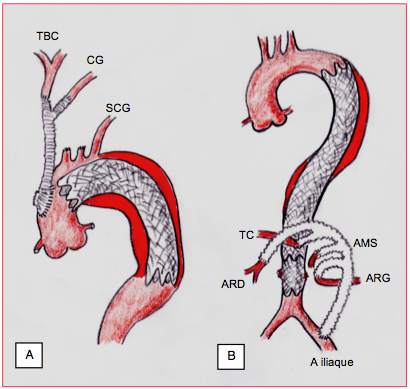
Figure 18.52 : Exemples d’interventions hybrides. A : l’anévrysme situé dans la crosse et la partie proximale de l’aorte descendante est exclu par une endoprothèse qui recouvre les orifices des trois troncs de la gerbe. Au préalable, un pontage chirurgical a été réalisé par sternotomie au moyen d’une prothèse bifurquée entre l’aorte ascendante d’une part et le tronc brachiocéphalique (TBC) et la carotide gauche (CG) d’autre part; l'intérêt de ne ponter que deux vaisseaux est de raccourcir le temps d'ischémie cérébrale. Sans un pontage carotido-sous-clavier gauche accessoire, il existe un risque d'ischémie proximale de la moelle; ce dernier pontage, difficile d'accès par sternotomie, est en général réalisé 1-2 jours avant par voie cervicale. B : Exclusion d’un anévrysme sous-diaphragmatique étendu par une endoprothèse allant de la région thoracique jusqu’à la bifurcation iliaque; par une laparotomie, le tronc coeliaque (TC), l’artère mésentérique supérieure (AMS) et les artères rénales (ARD et ARG) sont débranchés et réanastomosées à une artère iliaque au moyen d’une prothèses tubulaire à 4 branches (debranching).
Il persiste souvent de petites communications entre l'intérieur de la prothèse et l'anévrysme, appelées endofuites: elles peuvent survenir par défaut d’accolement aux extrémités de la prothèse, ou être dues à des déchirures du matériel (Vidéo). Ces fuites surviennent dans 17-20% des cas en salle d'opération, et dans 9% des cas à 30 jours [11]. Le Doppler couleur à l'ETO est la meilleure technique pour les mettre en evidence. Elles se répartissent en 4 catégories (Figure 27.127) [4,12].
- I: fuite entre la prothèse et la paroi aortique au niveau du collet;
- II: fuite par des vaisseaux collatéraux débitant dans la lésion exclue;
- III: défauts dans la prothèse;
- IV: porosité normale de la prothèse (disparaît avec le dépôt de fibrine).
Vidéo: petite endofuite au niveau du collet distal d'une endoprothèse de l'aorte descendante.
Vidéo: petite endofuite au niveau du collet distal d'une endoprothèse de l'aorte descendante.
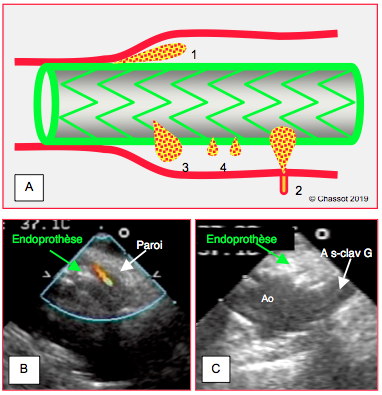
Figure 27.127 : Endofuites caractéristiques de l’endoprothèse. A : schéma des différents types d’endofuites. 1 : fuite au niveau du collet. 2 : fuite de branches vasculaires. 3 : défauts dans la prothèse. 4 : porosité normale de la prothèse. B : image ETO d’une endofuite de type 1 située au collet, entre la prothèse et la paroi aortique. C : court-axe de la crosse montrant une endoprothèse située à ras le départ de l’artère sous-clavière gauche.
Les types I et III sont considérés comme des échecs de la procédure et requièrent un traitement endovasculaire immédiat. Les fuites de type II sont surveillées s'il s'agit de petits vaisseaux mais peuvent être embolisées ou ligaturées chirurgicalement s'il s'agit de vaisseaux importants. La porosité n'est plus un problème avec les nouvelles prothèses. Il existe une cinquième type consistant en une expansion continue du sac anévrysmal sans fuite clairement visible [2]. Autour de la prothèse, l'anévrysme, exclu de la circulation, se thrombose et diminue progressivement de diamètre.
Interventions chirurgicales
Les interventions chirurgicales et les procédures hybrides (chirurgie à ciel ouvert + endoprothèse) sont décrites en détail dans le Chapitre 18 (voir Chirurgie de l'aorte ascendante, Chirurgie de la crosse aortique, Endoprothèses de l'aorte thoracique, Opérations hybrides)
| Endoprothèse de l’aorte thoracique descendante |
|
La prothèse est un tube de Dacron™ armé imperméable introduit par voie percutanée (cathétérisme fémoral). Conditions de réalisation:
- Vaisseau fémoral > 7.5 mm et axe ilio-aortique libre
- Collet d’amarrage ≤ 30 mm de diamètre et ≥ 15 mm de longueur
- Longueur de la lésion < longueur de la prothèse
- Rupture pariétale < 1/3 de la circonférence
- Contrôle de la mise en place par fluoroscopie, ultrasons intravasculaires (IVOS) et ETO
Indications: anévrysme, dissection, déchirure traumatique, athérome ulcéré.
|
© CHASSOT PG, BETTEX D. Novembre 2011, Août 2019; dernière mise à jour, Mars 2020
Références
- BETTEX DA. New techniques in endovascular surgery: challenges for the anaesthetist ? Anaesthesia Intern 2012; 6:28-33
- ERBEL R, ABOYANS V, BOILEAU C, et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases. Eur Heart J 2014; 35:2873-926
- FORT ACP, RUBIN LA, MELTZER AJ, et al. Perioperative management of endovascular thoracoabdominal aortic aneurysm repair. J Cardiothorac Vasc Anesth 2017; 31:1440-59
- GRABENWÖGER M, ALFONSO F, BACHET J, et al. Thoracic endovascular aortic repair (TEVAR) for the treatment of aortic diseases: a position statement from the EACTS and the ESC, in collaboration with the EAPCI. Eur Heart J 2012; 33:1558-63
- GREENHALGH RM, POWELL JT. Endovascular repair of abdominal aortic aneurysm. N Engl J Med 2008; 358:494-501
- HUGHES GC, SULZER CF, McCANN RL, SWAMINATHAN M. Endovascular approaches to complex thoracic aortic disease. Semin Cardiothorac Vasc Anesth 2008; 12:298-319
- KIHARA C, MURATA K, WADA Y, et al. Impact of intraoperative transesophageal echocardiography in cardiac and thoracic aortic surgery: experience in 1011 cases. J Cardiol 2009; 54:282-8
- NOWAK-MACHEN M. The role of transesophageal echocardiography in aortic surgery. Best Pract Res Clin Anaesthesiol 2016; 30:317-29
- SVENSSON LG, KOUCHOUKOS NT, MILLER DC, et al. Expert consensus document on the treatment of descending thoracic aortic disease using endovascular stent-grafts. Ann Thorac Surg 2008; 85:S1-41
- SWAMINATHAN M, MATHEW J. Aortic surgery and atheroma assessment. In: MATHEW JP, NICOARA A, AYOUB CM, SWAMINATHAN M. Clinical manual and review of transesophageal echocardiography, 3rd edition. New York: McGraw-Hill, 2019, 413-34
- VALLABHANENI SR, HARRIS PL. Lessons learned from the EU-ROSTAR registry on endovascular repair of abdominal aortic aneurysm repair. Eur J Radiol 2001; 39:34-41
- VEITH FJ, BAUM RA, OHKI T, et al. Nature and significance of endoleaks and endotension: summary of opinions expressed at an international conference. J Vasc Surg 2002; 35:1029-35
