Dysplasie arythmogène du ventricule droit
Dans cette affection rare, le myocarde du ventricule droit est progressivement remplacé par une infiltration de fibrocytes et d'adipocytes qui prédomine dans la chambre de chasse, l’apex et la région tricuspidienne ; les trabéculations du VD sont souvent hypertrophiées mais la paroi est amincie; la chambre de chasse est dilatée (> 3 cm) [10]. Ceci s'accompagne d'une dysfonction droite progressive sévère et de troubles du rythme. L'incidence est estimée à 1:5'000 patients. A l’échocardiographie, la paroi libre est akinétique, et seule la contraction du septum interventriculaire assurée par le VG propulse du sang dans l’artère pulmonaire. L'infiltrat de la paroi libre par le tissu adipeux donne un signal hyperéchogène [6]. La régurgitation tricuspidienne due à la dilatation est de basse vélocité (< 2 m/s) à cause de la mauvaise fonction systolique droite (Vidéos et Figure 27.47).
Vidéo: vue 4-cavités d'une défaillance droite sur dysplasie arythmogène du VD; les cavités droites sont dilatées, la paroi libre du VD est inerte et infiltrée de matériel hyperéchogène. Seule la contraction du septum interventriculaire assure la propulsion du sang dans l'artère pulmonaire.
Vidéo: insuffisance tricuspidienne dans le même cas de dysplasie arythmogène du VD; la force de contraction droite est si faible que le flux de l'IT est laminaire et de basse vélocité (Vmax < 0.5 m/s).
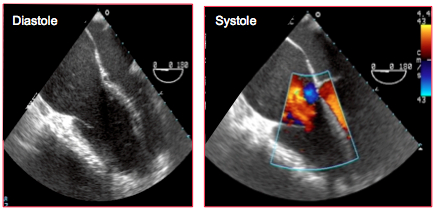
Figure 27.47 : Dysplasie arythmogène du ventricule droit. Le VD et l’OD sont dilatés, le septum interventriculaire bombe dans le VG qui est comprimé ; la texture myocardique de la paroi libre du VD est hyperéchogène ; la FE du VD est < 15%. Au Doppler couleur, la Vmax de l’IT est très basse (0.5 – 1.0 m/s) à cause de la défaillance systolique et de la dilatation massive de l’anneau tricuspidien ; en systole, le flux rétrograde de l’IT est laminaire. Entre l’image en diastole (à gauche) et en systole (à droite), seule la position du septum interventriculaire a changé ; par la contraction du VG, c’est lui qui assure la propulsion du sang dans l’AP.
| Dysplasie arythmogène du VD |
| Remplacement progressif du tissu myocardique par des adipocytes et des fibrocytes, le plus souvent dans le VD, conduisant à une dysfonction ventriculaire droite sévère. Aspect grumeleux hyperéchogène de la paroi libre du VD. |
Maladie de Tako-tsubo
La ballonisation apicale aiguë transitoire du VG consiste en une dysfonction de l'apex du VG mimant un infarctus mais ne montrant aucune lésion coronarienne à l'angiographie. Elle a été décrite tout d'abord au Japon, où on lui a donné le nom de maladie de Tako-tsubo parce que la dysfonction akinétique de l'apex ventriculaire gauche donne des images ressemblant au pot à col étroit qu'utilisent les pêcheurs japonais pour piéger les poulpes. La clinique est identique à celle d'un infarctus aigu, mais l’affection présente des caractéristiques particulières (Vidéos et Figure 27.48) [1,2,3,4].
Vidéo: vue 4-cavités d'une maladie de Takotsubo mettant en évidence la ballonisation apicale typique.
Vidéo: vue long-axe du même cas de maladie de Takotsubo.
- Akinésie transitoire circonférentielle et étendue de la région apicale (82% des cas), médioventriculaire (15%) ou focale (3%) du VG, ne suivant pas la distribution segmentaire des territoires coronariens ; hyperkinésie de la base du VG (Takotsubo 1) (Takotsubo 2).
- Dysfonction ventriculaire globale, pouvant conduire à des arythmies sévères ou au choc cardiogène ; la FE est abaissée (0.2 – 0.4), mais la récupération est rapide (en général, 48 heures à 2 semaines).
- Dans 25% des cas, l’hyperkinésie des segments basaux peut conduire à une obstruction dynamique de la chambre de chasse du VG ("effet CMO" avec gradient > 25 mmHg), qui s'accompagne d'un basculement du feuillet mitral antérieur dans la CCVG (SAM systolic anterior motion) et d'une IM méso-systolique [11].
- Chez environ 20% des patients, le VD est également touché et présente une akinésie apicale dilatée (signe de McConnel inversé) [3].
- Environ 10% des patients développent un thrombus intraventriculaire au niveau de la zone akinétique.
- Récupération totale de la cinétique pariétale et de la fonction dans les jours ou les semaines qui suivent l'événement [9].
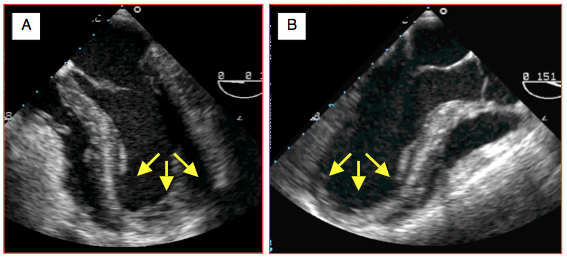
Figure 27.48 : Ballonisation apicale aiguë transitoire du VG (maladie de Tako-tsubo) en vues échocardiographiques transoesophagiennes. L’apex est ballonisé (flèches), akinétique et se comporte comme un ballon inerte. A : vue 4-cavités 0°. B : vue long-axe du VG 150°.
La zone touchée ne correspond pas à une distribution vasculaire mais couvre plusieurs segments sans en suivre la géométrie classique ; la masse ventriculaire atteinte est disproportionnellement importante par rapport à la faible élévation des enzymes cardiaques.
| Cardiomyopathie de Takotsubo |
| Critères diagnostiques de la ballonisation aiguë transitoire du VG: - Ballonisation akinétique le plus souvent apicale du VG sans rapport avec les territoires coronariens - Altération de l'ECG et élévation très modérée des troponines - Absence de lésions coronariennes à l'angiographie - Absence d'étiologie (myocardite, phéochromocytome, lésion intracrânienne), sauf un stress émotionnel intense dans deux tiers des cas Le reste du VG est normo- ou hyperkinétique, avec un risque d'obstruction dynamique de la chambre de chasse. La récupération est en général totale en quelques jours ou semaines. |
Non-compaction du VG
La non-compaction du VG est une cardiomyopathie fréquemment associée à des cardiopathies congénitales, caractérisée par la persistance de myocarde primitif constitué de nombreuses trabéculations très proéminentes entrecoupées de profonds récessus communicant avec la cavité ventriculaire (présence de flux). Ces malformations sont localisées dans la paroi apicale, latérale moyenne et inférieure moyenne [5]. A ces endroits, la paroi ventriculaire semble constituée de deux couches distinctes : une couche profonde épaisse et trabéculée et une mince couche sous-épicardique continue normale. La maladie est associée à une dysfonction du VG et à des arythmies graves.
L'échocardiographie montre des trabéculations proéminentes et des sinusoïdes profonds dans lesquels circule le sang de la cavité ventriculaire, situés dans la zone apicale du VG et s'étendant plus ou moins loin sur les parois latérale et inférieure. Ces segments sont hypocontractiles et représentent ≥ 25% de la masse myocardique [7]. Le rapport entre l'épaisseur de la zone non-compactée et celle de la zone compactée est > 2:1 en télésystole dans les cas sévères [8]. L'image Doppler couleur montre le flux sanguin circulant en profondeur entre les trabéculations (Figure 27.49).
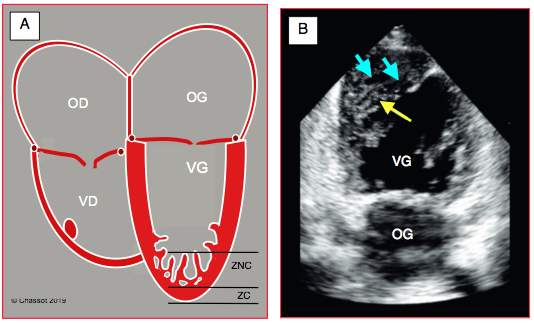
Figure 27.49 : Non-compaction du VG. A: silhouette des 4 cavités cardiaques; la zone apicale du VG présente au moins 4 grosses trabéculations peu contractiles; cette morphologie embryonnaire concerne toute la région sous-endocardique de la paroi, la région sous-épicardique étant occupée par du myocarde normalement compacté. Le rapport entre la zone non-compactée (ZNC) et la zone compactée (ZC) est > 2:1. B: image échocardiographique de non-compaction du ventricule gauche (vue transthoracique apicale 2-cavités). La zone apicale du VG est envahie par les trabéculations du tissu non-compacté (flèches bleues); on y reconnaît les profonds recessus plongeant entre les trabéculations (flèche jaune) [D'après: Hussein A, Karimianpour A, Collier P, et al. Isolated noncompaction of the left ventricle in adults. J Am Coll Cardiol 2015; 66:578-85].
| Non-compaction du VG |
| Persistance de tissu embryonnaire non-compacté hypocontractile, en général dans la zone apicale du VG. Cardiomyopathie rare caractérisée par une insuffisance cardiaque, des arythmies et des thrombo-embolies. |
© CHASSOT PG, BETTEX D. Novembre 2011, Août 2019; dernière mise à jour, Mars 2020
Références
- BYBEE KA, KARA T, PRASAD A, et al. Systematic review: Transient left ventricular apical ballooning: A syndrome that mimics ST-segment elevation myocardial infarction. Ann Intern Med 2004; 141:858-65
- BYBEE KA, PRASAD A. Stress-related cardiomyopathy syndromes. Circulation 2008; 118:397-409
- CITRO R, LYON AR, MEIMOUN P, et al. Standard and advanced echocardiography in takotsubo (stress) cardiomyopathy: clinical and prognostic implications. J Am Soc Echocardiogr 2015; 28:57-74
- DE CHAZAL HM, DEL BUONO MG, KEYSER-MARCUS L, et al. Stress cardiomyopathy diagnosis and treatment. JACC state-of-the-art review. J Am Coll Cardiol 2018; 72:1955-71
- ENGLBERDING R, YELBUZ TM; BREITHARDT G. Isolated non-compaction of the left ventricular myocardium – a review of the literature two decades after the initial case description. Clin Res Cardiol 2007; 96:481-8
- FONTAINE G, GALLAIS Y, FORNES P, et al. Arrhythmogenic right ventricular dysplasia/cardiomyopathy. Anesthesiology 2001; 95:250-4
- HUSSEIN A, KARIMIANPOUR A, COLLIER P, et al. Isolated noncompaction of the left ventricle in adults. J Am Coll Cardiol 2015; 66:578-85
- JENNI R, OECHSLIN E, SCHNEIDER J, et al. Echocardiographic and pathoanatomical characteristics of isolated left ventricular noncompaction: a step towards classification as a distinct cardiomyopathy. Heart 2001; 86:666-71
- KOMAMURA K. Takotsubo cardiomyopathy: pathophysiology, diagnosis and treatment. World J Cardiol 2014; 6:602-9
- MARCUS FI, McKENNA WJ, SHERRIL D, et al. Diagnosis of arrhythmogenic right ventricular cardiomyopathy/dysplasia: proposed modifications of the Task Force criteria. Eur Heart J 2010; 31:806-14
- PARODI G, DEL PACE S, SALVADORI C, et al. Left ventricular apical ballooning syndrome as a novel cause of acute mitral regurgitation. J Am Coll Cardiol 2007; 50:647-9