Nosologie
Une IT minime à modérée est présente chez 70% des sujets normaux à partir de 60 ans [13]. La grande majorité des insuffisances triscuspidiennes n’est pas liée à une pathologie de la valve, mais est secondaire à une dilatation de l’anneau tricuspidien due à une surcharge du VD (Vidéos).
Une IT minime à modérée est présente chez 70% des sujets normaux à partir de 60 ans [13]. La grande majorité des insuffisances triscuspidiennes n’est pas liée à une pathologie de la valve, mais est secondaire à une dilatation de l’anneau tricuspidien due à une surcharge du VD (Vidéos).
- Valvulopathie gauche on insuffisance du VG entraînant une hypertension pulmonaire postcapillaire;
- Hypertension pulmonaire précapillaire, quelle qu’en soit la cause;
- Dysfonction du VD (insuffisance, cardiomyopathie, ischémie ou infarctus).
Vidéo: insuffisance tricuspidienne secondaire à une hypertension pulmonaire; les cavités droites sont dilatées alors que les cavités gauches sont comprimées.
Vidéo: insuffisance tricuspidienne secondaire à une défaillance terminale du VD; la capacité éjectionnelle du ventricule est si faible que la vélocité de l'IT est très basse (< 0.5 m/s); son flux rétrograde systolique est laminaire au Doppler couleur.
La lésion primaire des feuillets tricuspidiens est une affection plus rare (25% des cas opérés), qui relève de nombreuses étiologies [2,12,22].
- Maladie d'Ebstein: les feuillets postérieur et septal sont bas-insérés (déplacement apical de ≥ 20 mm par rapport à leur position normale) et se retrouvent en position intraventriculaire; la cavité du VD est rétrécie, toute sa portion basale étant "atrialisée". Le feuillet antérieur peut être insuffisant pour permettre l’occlusion, ou redondant et basculer dans l’OD (Vidéo) ; dans les deux cas, l’IT est importante.
- RAA: encore fréquent dans les pays non-industrialisés, la maladie conduit à une combinaison d’insuffisance et de sténose par restriction, fusion commissurale, et fibrose des feuillets et des cordages (Vidéos). Un ou plusieurs feuillets et leur point de coaptation sont déplacés à l'intérieur de l'OD.
- Dégénérescence myxoïde (Barlow) ou fibro-élastique (Marfan) avec prolapsus et bascule de feuillet; en général associée à un prolapsus mitral (Vidéos).
- Fibro-élastose endomyocardique : rétraction des feuillets et des cordages, fréquente en Afrique tropicale; souvent accompagnée de thrombus apical dans le VD et de défaillance droite.
- Traumatisme: rupture de pilier ou déchirure de feuillet (Vidéos).
- Endocardite: incidence particulièrement élevée chez les toxicomanes et les porteurs de cathéter implanté (pace-maker).
- Syndrome carcinoïde : dépôts de plaques fibreuses sur l'endocarde, épaississement et restriction des feuillets qui semblent adhérer à la paroi ventriculaire (Vidéo). L'IT est habituellement accompagnée d'une sténose.
- Iatrogénie : une sonde de pacemaker-défibrillateur ou un cathéter artériel pulmonaire empêchent l’occlusion des feuillets et provoquent une IT bénigne dans 39% des cas [10].
- Toxicité médicamenteuse: méthysergide, ergot de seigle, fenfluramine, phentermine, aminorex, benfluorex, pergolide.
Vidéo: maladie d'Ebstein; bas-insertion du feuillet septal et du feuillet postérieur, insertion normale du feuillet antérieur qui est long et prolabant. Les feuillets ne coaptent pas en systole.
Vidéo: vue 4-cavités dans un cas de rhumatisme articulaire aigu; les deux valves atrio-ventriculaires sont sténosées, les ventricules sont petits et les oreillettes très grandes. La valve tricuspide, rétractée et peu mobile, n'occlut pas en systole.
Vidéo: flux Doppler couleur dans le même cas que la vidéo précédente; présence d'une IT centrale modérée.
Vidéo: prolapsus majeur du feuillet postérieur de la valve tricuspide.
Vidéo: flux Doppler couleur dans le même cas montrant une insuffisance tricuspidienne sévère.
Vidéo: rupture traumatique de cordages du feuillet antérieur entraînant un prolapsus majeur.
Vidéo: vue 3D du même cas, montrant le cordage rompu.
Vidéo: lésion carcinoïde de la valve tricuspide; les feuillets sont rigides et rétractés, la valve est sténosée et insuffisante, elle n'occlut pas en systole.
Vidéo: flux Doppler couleur dans le même cas, montrant un flux accéléré et tourbillonnaire en diastole et une insuffisance modérée-à-sévère en systole.
Echocardiographie
Les images échocardiographique de l’IT sont typiques (Figure 26.130). Le jet couleur dans l'OD est le signe d'appel le plus commun. Son étendue est un moyen pratique de diagnostiquer la présence d’une IT et d’en évaluer grossièrement l’importance, mais elle n’est pas une technique adéquate pour une quantification précise, car elle dépend de la force de contraction du VD, des RAP, de la POD et des réglages de l'appareil [15]. Comme la dilatation de l'anneau tricuspidien est excentrique en direction antéro-latérale, le jet d'IT est souvent dirigé vers le septum interauriculaire.
Vidéo: vue transgastrique admission du VD 100° permettant la planimétrie du jet d'IT dans l'oreillette droite et la mesure de la vena contracta.
Vidéo: vue admission-chasse du VD mettant l'insuffisance tricuspidienne en ligne avec le faisceau Doppler. L'IT est en général dirigée vers le septum interauriculaire parce que le feuillet septal tend à être restrictif.
Vidéo: insuffisance tricuspidienne massive en vue admission du VD. La lésion est d'origine traumatique (rupture du feuillet antérieur).
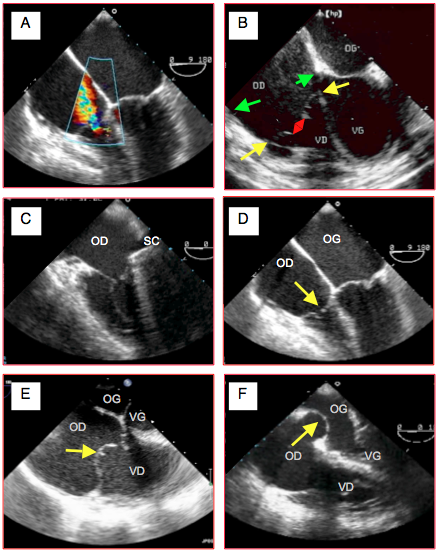
Figure 26.130 : Images ETO d’insuffisance tricuspidienne. A : IT modérée-à-sévère sur RAA en vue 4-cavités 0°. B maladie d’Ebstein ; les feuillets septal et postérieur de la valve sont bas-insérés (flèches jaunes) ; insertion normale : flèches vertes. Les feuillets ne se rejoignent pas en systole (double flèche rouge), ce qui génère une IT sévère. C : vue 4-cavités (position en bas oesophage) d’une insuffisance tricuspidienne massive sur carcinoïde ; les feuillets sont rigides et restrictifs; ils ne coaptent pas en systole. SC : sinus coronaire. D : vue identique d'une IT sur RAA; les feuillets sont épaissis et peu mobiles; il persiste un orifice en systole (flèche). E : : rupture traumatique de cordages entraînant un basculement du feuillet antérieur. F : bascule du septum interauriculaire qui est tendu dans l’OG.
La découverte d'une IT au flux couleur déclenche trois questions essentielles que l'examen détaillé devra résoudre [20].
Les images échocardiographique de l’IT sont typiques (Figure 26.130). Le jet couleur dans l'OD est le signe d'appel le plus commun. Son étendue est un moyen pratique de diagnostiquer la présence d’une IT et d’en évaluer grossièrement l’importance, mais elle n’est pas une technique adéquate pour une quantification précise, car elle dépend de la force de contraction du VD, des RAP, de la POD et des réglages de l'appareil [15]. Comme la dilatation de l'anneau tricuspidien est excentrique en direction antéro-latérale, le jet d'IT est souvent dirigé vers le septum interauriculaire.
Vidéo: vue transgastrique admission du VD 100° permettant la planimétrie du jet d'IT dans l'oreillette droite et la mesure de la vena contracta.
Vidéo: vue admission-chasse du VD mettant l'insuffisance tricuspidienne en ligne avec le faisceau Doppler. L'IT est en général dirigée vers le septum interauriculaire parce que le feuillet septal tend à être restrictif.
Vidéo: insuffisance tricuspidienne massive en vue admission du VD. La lésion est d'origine traumatique (rupture du feuillet antérieur).

Figure 26.130 : Images ETO d’insuffisance tricuspidienne. A : IT modérée-à-sévère sur RAA en vue 4-cavités 0°. B maladie d’Ebstein ; les feuillets septal et postérieur de la valve sont bas-insérés (flèches jaunes) ; insertion normale : flèches vertes. Les feuillets ne se rejoignent pas en systole (double flèche rouge), ce qui génère une IT sévère. C : vue 4-cavités (position en bas oesophage) d’une insuffisance tricuspidienne massive sur carcinoïde ; les feuillets sont rigides et restrictifs; ils ne coaptent pas en systole. SC : sinus coronaire. D : vue identique d'une IT sur RAA; les feuillets sont épaissis et peu mobiles; il persiste un orifice en systole (flèche). E : : rupture traumatique de cordages entraînant un basculement du feuillet antérieur. F : bascule du septum interauriculaire qui est tendu dans l’OG.
La découverte d'une IT au flux couleur déclenche trois questions essentielles que l'examen détaillé devra résoudre [20].
- La fuite est-elle banale ou anormale ?
- La fuite est-elle due à une maladie primaire de la valve (feuillets pathologiques) ou est-elle secondaire à une dilatation annulaire (feuillets normaux)?
- Quelle est l'importance hémodynamique de l'IT ?
Les critères d’une insuffisance tricuspidienne sévère sont essentiellement échocardiographiques (Tableau 26.9) [4,8,15,27,28].
- Non-coaptation centrale des feuillets, qui sont normaux (IT secondaire) ou anormaux (IT primaire par bascule dans l'OD, rupture de cordage, rétraction, ou perforation); écart entre les feuillets > 8 mm (Vidéo).
- Dilatation de l’anneau tricuspidien (diamètre annulaire ≥ 3.6 cm ou 2.1 cm/m2 en vue 4-cavités); aucune vue 2D n'offre une bonne corrélation avec la mesure chirurgicale du diamètre de l'anneau [18]. La reconstruction 3D "en-face" permet par contre la mesure du diamètre antéroseptal-postérolatéral, qui est mieux corrélé à la mesure chirurgicale. Ce diamètre ne correspond à aucun plan 2D précis, mais il est le plus grand diamètre au niveau duquel a lieu la plus grande variation systolo-diastolique; ce dynamisme est perdu lors de dilatation droite [1,9]. Un diamètre > 4 cm en 4-cavités en télédiastole est considéré comme une indication à une plastie simultanée au cours d'opération sur le cœur gauche [19].
- Un jet couleur occupant plus du tiers de l’OD, atteignant la paroi postérieure ou d'une surface de > 10 cm2 parle en faveur d'une IT sévère. L’évaluation doit se faire dans 2 plans orthogonaux (4-cavités 0° et bicave modifié 100°, par exemple), avec une limite de Nyquist à 0.5-0.8 m/s. Mais un jet central tend à surestimer l'IT alors qu'un jet excentrique tend à la sousestimer. D'autre part, le jet couleur dépend des conditions hémodynamiques et du réglage de l'échelle couleur. Il n'est donc pas un critère quantitatif adéquat; il n'est recommandé que comme signe d'appel. En cas de large orifice et de dysfonction sévère du VD, la vélocité de l'IT reste basse et le flux laminaire sans aliasing, même en cas d'insuffisance massive; on ne voit qu'un va-et-vient de sang entre l'OD et le VD (Figure 26.131) (Vidéo).
- Au Doppler continu, une trace spectrale de la vélocité dense et au contour net traduit une IT importante; sa densité est proportionnelle au nombre d'hématies que contient le flux. Le pic de Vmax est mésosystolique. Un tracé de forme triangulaire avec un pic protosystolique indique que la POD est élevée (onde "v" prononcée sur la courbe de PVC). La Vmax est de 2-4 m/s, mais elle dépend de la fonction du VD et de la PAP; elle ne donne aucune indication sur l'importance du volume régurgité car elle est souvent basse dans les IT massives (Figure 26.132).
- Diamètre du jet à la vena contracta > 0.7 cm; pour être certain que la mesure soit bien perpendiculaire à l'axe du flux, la zone de convergence en amont doit être bien visible (limite de Nyquist à 50-60 cm/s). La mesure doit se faire dans deux plans différents, car la surface de la VC n'est souvent pas circulaire mais elliptique (Figure 26.133). Ainsi dans les IT secondaires, la VC est en général plus large en vue admission-chasse du VD à 60° qu'en vue 4-cavités, parce que la première passe par la commissure entre le feuillet septal et le feuillet antérieur (voir Figure 26.125) [19]. En 3D, une surface de vena contracta (VC) > 0.4 cm2 dans l'IT structurelle et > 0.55 cm2 dans l'IT fonctionnelle signe une IT sévère [3].
- Zone de convergence proximale du flux (PISA, proximal isovelocity surface area): un rayon de 1er aliasing > 9 mm (échelle de couleur de 28 cm/s) signe une IT sévère. Cette méthode est peu utilisée dans l'IT car la vélocité y est basse et la zone hémisphérique aplatie, ce qui tend à sousestimer l'importance de la régurgitation (Figure 26.134).
- Orifice de régurgitation ≥ 0.4 cm2, volume de régurgitation ≥ 45 mL; en 3D, la surface de l'orifice de régurgitation est > 0.55 cm2. Ces valeurs ne sont pas bien établies et restent très discutées. De plus, elles sont respiro-dépendantes: la surface de l'orifice de régurgitation augmente en inspirium spontané [6].
- Dans l'IT secondaire, le niveau de coaptation des feuillets est maintenu en-dessous du plan de l'anneau par la dilatation du VD; à l'ETO, les feuillets et le plan de l'anneau forment une surface triangulaire en forme de tente. Dans l'IT sévère, la distance entre le plan de l'anneau et le niveau de coaptation est > 0.6 cm; la surface de tente est > 1.0 cm2. Des valeurs > 0.8 cm et > 1.6 cm2 respectivement sont des prédicteurs de fuite résiduelle après plastie chirurgicale [6,7].
- Flux diastolique antérograde accéléré à travers la valve tricuspide lorsque le volume régurgité est important: Vmax E > 1 m/s en l'absence de sténose.
- Dilatation de l’OD (diamètre ≥ 5 cm, surface > 18 cm2, volume > 35 mL/m2); bombement du septum interauriculaire dans l’OG.
- Dilatation du VD; bascule diastolique du septum interventrriculaire dans le VG dont la silhouette en court-axe prend une forme en "D". La fonction systolique du VD est affectée par une IT sévère. Bien qu'ils soient dépendants des conditions de charge, les critères fonctionnels comme la fraction d'éjection, le déplacement apical de l'anneau tricuspidien (TAPSE) ou la déformation systolique longitudinale (global longitudinal strain) sont tous diminués.
- Dilatation du sinus coronaire et de la veine cave inférieure (diamètre > 2.5 cm); disparition des variations respiratoires de la VCI.
- Inversion de la composante systolique du flux dans la VCI et les veines sus-hépatiques, qui sont dilatées et pulsatiles (limite de Nyquist < 0.4 m/s). Le diagnostic est rendu malaisé par la présence physiologique de deux petits épisodes de reflux en VCI: l'un pendant la contraction auriculaire (onde "a") et l'autre en télésystole-protodiastole (onde "v"). L’absence de l'inversion systolique n’exclut pas une IT sévère, car le reflux peut être absorbé par l’OD si celle-ci est très dilatée (Figure 26.135). D'autre part, le flux systolique veineux est influencé par la POD, par la compliance des cavités droites, par la respiration (les mesures doivent être effectuées en apnée), et par les troubles du rythme (FA, bloc AV, pacemaker). Cette inversion de la composante systolique se retouve également dans le sinus coronaire.
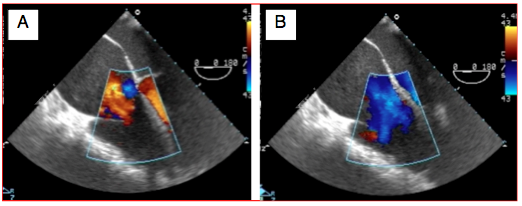
Figure 26.131 : Jet d'IT dans un cas de dysfonction sévère du VD. Entre la systole (A) et la diastole (B), les feuillets tricuspidiens ne bougent pratiquement pas. Le jet d'insuffisance tricuspidienne apparaît comme un flux rétrograde laminaire sans tourbillons ni aliasing (rouge-orange), parce que sa vélocité est basse vu l'impossibilité pour le VD de générer des pressions suffisantes. Le flux diastolique est normalement laminaire (bleu). Le septum interauriculaire est bombé en permanence dans l'OG.
Vidéo: vue 4-cavités d'une insuffisance tricuspidienne sévèrs dans un cas de syndrome carcinoïdien. Les cavités droites sont dilatées, le septum interventriculaire présente un mouvement paradoxal. Les feuillets de la valve tricuspide sont immobiles.
Vidéo: vue X-plane du même cas, avec le flux Doppler couleur montrant une IT massive.
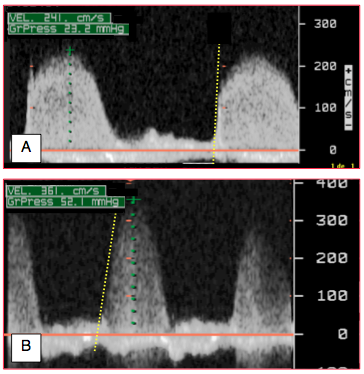
Figure 26.132 : Image Doppler spectrale d'insuffisance tricuspidienne. A: IT sévère, avec une trace pleine et dense, et une Vmax de 2.4 m/s (gradient de pression 23 mmHg). B: IT modeste, avec une trace moins dense et une Vmax de 3.6 m/s (gradient de pression 52 mmHg). La première est survenue sur une lésion de RAA avec un large orifice de régurgitation; la fonction du VD est encore normale (pente ascentionnelle de l'IT très verticale). La deuxième est secondaire à une hypertension pulmonaire (PAPsyst 65 mmHg) ayant déjà induit une baisse de fonction du VD (pente de l'IT plus faible).
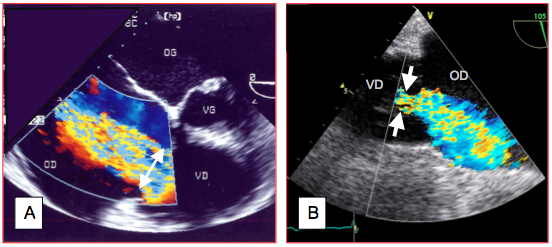
Figure 26.133 : Quantification d’une insuffisance tricuspidienne sévère. A : très large vena contracta (2.2 cm) lors d’une IT massive sur RAA (vue 4-cavités). Cette vue surestime l'importance de l'IT, car l'orifice de régurgitation correspond à la commissure entre les feuillets antérieur et postérieur. B : planimétrie du jet couleur (11.5 cm2) et mesure du diamètre de la vena contracta (0.8 cm) en vue transgastrique (vue admission du VD 100°).
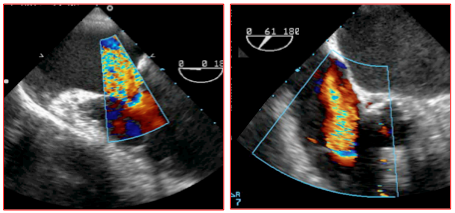
Figure 26.134 : Deux exemples de la zone d'accélération concentrique (PISA) sur la face ventriculaire d'une IT, en vue 4-cavités 0° et en vue admission-chasse du VD 60°. La vena contracta est large (> 1 cm) ; il existe un PISA important, mais l'hémisphère tend à s'aplatir par rapport à celui de l'insuffisance mitrale qui est franchement circulaire.
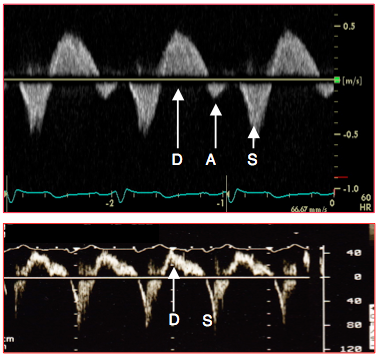
Figure 26.135 : Flux en veine sus-hépatique (ETO en position transgastrique). On remarque un reflux systolique (S), alors que le flux normal devrait être antérograde. D: flux diastolique antérograde. A: léger reflux lié à la contraction auriculaire.
Une certaine confusion peut régner au sujet du diamètre de l'anneau tricuspidien, car il en existe plusieurs versions [1,5,6].
- Diamètre septo-latéral (petit diamètre, 2.8 ± 0.5 cm), mesuré en vue 4-cavités.
- Diamètre antéro-postérieur (grand diamètre, 3.5 ± 0.3 cm), mesuré entre 60° et 100° (vue admission-chasse du VD et vue bicave modifiée, respectivement).
- Diamètre chirurgical, mesuré dans le champ opératoire sur un cœur flaccide entre la commissure septo-antérieure et la commissure postéro-antérieure, soit les 2 extrémités du feuillet antérieur; un diamètre chirurgical de 7.0 cm correspond à un diamètre septo-latéral de 4.0 cm.
- Diamètre de dilatation maximale, situé entre le septum et la commissure antéro-postérieure (correspond à la paroi libre du VD).
- La corrélation avec le diamètre chirurgical maximal est meilleure lorsque la mesure échocardiographique est réalisée en 3D dans l'axe antéroseptal-postérolatéral [1].
- Le seuil de dilatation de l'anneau tricuspidien est un diamètre de 3.6 cm en vue 4-cavités.
- L'indication opératoire habituellement reconnue pour une plastie de l'anneau tricuspidien dans l'IT fonctionnelle est de 4.0 cm en vue 4-cavités en télédiastole.
En 3D, l'acquisition en full-volume permet une reconstruction de la valve par découpe (cropping) du volume enregistré dans une vue en-face comme si elle était examinée depuis l'oreillette. Par convention, on l'oriente avec le feuillet septal à 6 heures, le feuillet antérieur à 11 heures et le feuillet postérieur à 3 heures, ce qui correspond à la vue qu'en a le chirurgien lorsqu'il ouvre l'OD. Cette vue permet la mesure précise du diamètre antéroseptal-postérolatéral de l'anneau tricuspidien, alors qu'aucune vue 2D ne passe strictement par ce plan [1]. Le biais sur la mesure des diamètres de l'anneau tricuspidien est de 0.03 cm en 3D, alors qu'il est de 0.21 cm en 2D; la probabilité d'être dans une limite de 0.2 cm avec la mesure chirurgicale est de 66% pour le 3D, mais de 25% pour le 2D [1]. La représentation 3D est très utile pour la localisation des pathologies (prolapsus, rupture de cordage) et de l'origine du jet d'insuffisance; elle permet également la planimétrie de la valve et de l'orfice de régurgitation (Figure 26.136) [16]. Comme la mesure de la surface de la vena contracta en 3D n'est pas tributaire de présupposés géométriques, la valeur retenue pour définir une IT sévère est sensiblement plus grande qu'en 2D (0.75 cm2 au lieu de 0.4 cm2) [15].
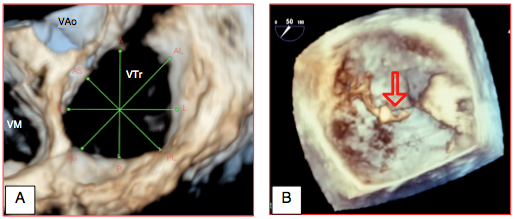
Figure 26.136 : Image 3D de la valve tricuspide depuis l'OD (vue "en-face"). A: valve normale avec ses différents diamètres. B: image d'un prolapsus du feuillet antérieur sur rupture traumatique.
En cas d'IT aiguë, comme dans une rupture traumatique ou une destruction endocarditique, l'OD n'est pas dilatée; le reflux systolique dans la VCI, les veines sus-hépatiques et le sinus coronaire est très prononcé. Hormis ces cas aigus, l'absence de dilatation de l'OD et du VD signe une IT mineure ou modérée; elle exclut une IT sévère.
IT fonctionnelle
Dans l'IT fonctionnelle, la dilatation de l'anneau à lieu dans la direction antéro-latérale puisque la structure fibreuse est interrompue à ce niveau. Les feuillets antérieur et postérieur s'écartent progressivement du feuillet septal [6]. Ce déplacement tend à diriger le jet d'IT vers le septum interauriculaire parce que le feuillet septal devient fonctionnellement restrictif. Ceci présente l'avantage de le placer dans un axe très voisin de celui du Doppler en ETO. Avec sa dilatation, l'anneau tricuspidien perd sa forme en selle et s'aplatit. Il s'élargit principalement dans l'axe septo-latéral (diamètre en 4-cavités). Dans l'IT fonctionnelle, l'indication opératoire à une plastie tricuspidienne simultanément à une intervention sur le cœur gauche est posée lorsque le diamètre de l'anneau est > 4 cm mesuré en 4-cavités 0° en télédiastole, quelle que soit l'importance de la régurgitation [6,15]. Cette attitude diminue l'IT, améliore la capacité fonctionnelle et abaisse la mortalité à long terme de 30% [5].
L'importance de l'IT au jet couleur est diminuée par l'anesthésie et par la modification des conditions de charge pour le VD; elle est un critère moins fiable que les dimensions anatomiques de l'anneau et la position des feuillets en systole [6]. Bien qu'elle ne soit pas une pathologie du cœur droit, l'insuffisance tricuspidienne fonctionnelle aggrave considérablement la situation du VD lorsque celui-ci subit une surcharge de pression, par exemple suite à une hypertension pulmonaire. Elle ajoute une surcharge de volume à la surcharge de pression. Ceci augmente la dilatation du VD, ce qui accroît secondairement l'IT, et le cœur droit entre ainsi dans un cercle vicieux.
La présence d’une IT permet de calculer la PAP systolique par le truchement de l’équation simplifiée de Bernoulli (voir Chapitre 25, Equation de Bernoulli)). Cette équation stipule que le gradient de pression entre deux cavités est égal à 4 fois le carré de la vélocité maximale du flux sanguin entre ces deux cavités: ΔP = 4 (Vmax)2. En systole, la Vmax de l'IT est fonction du ΔP entre le VD et l'OD. En l'absence de pathologie sur la valve pulmonaire (rarissime chez l'adulte), la pression pulmonaire systolique (PAPs) est donc la somme du ΔP VD - OD et de la pression moyenne de l'OD (voir Figure 25.161).
PAPs = (4 • V2IT) + POD
La POD est mesurée par la PVC ou estimée par le degré de collapsibilité de la veine cave inférieure: en hypovolémie, les variations respiratoires du diamètre de la VCI (mesuré en mode TM par voie transgastrique ou sous-xyphoïdienne) sont excessives lorsque le malade est hypovolémique.

Figure 26.136 : Image 3D de la valve tricuspide depuis l'OD (vue "en-face"). A: valve normale avec ses différents diamètres. B: image d'un prolapsus du feuillet antérieur sur rupture traumatique.
En cas d'IT aiguë, comme dans une rupture traumatique ou une destruction endocarditique, l'OD n'est pas dilatée; le reflux systolique dans la VCI, les veines sus-hépatiques et le sinus coronaire est très prononcé. Hormis ces cas aigus, l'absence de dilatation de l'OD et du VD signe une IT mineure ou modérée; elle exclut une IT sévère.
IT fonctionnelle
Dans l'IT fonctionnelle, la dilatation de l'anneau à lieu dans la direction antéro-latérale puisque la structure fibreuse est interrompue à ce niveau. Les feuillets antérieur et postérieur s'écartent progressivement du feuillet septal [6]. Ce déplacement tend à diriger le jet d'IT vers le septum interauriculaire parce que le feuillet septal devient fonctionnellement restrictif. Ceci présente l'avantage de le placer dans un axe très voisin de celui du Doppler en ETO. Avec sa dilatation, l'anneau tricuspidien perd sa forme en selle et s'aplatit. Il s'élargit principalement dans l'axe septo-latéral (diamètre en 4-cavités). Dans l'IT fonctionnelle, l'indication opératoire à une plastie tricuspidienne simultanément à une intervention sur le cœur gauche est posée lorsque le diamètre de l'anneau est > 4 cm mesuré en 4-cavités 0° en télédiastole, quelle que soit l'importance de la régurgitation [6,15]. Cette attitude diminue l'IT, améliore la capacité fonctionnelle et abaisse la mortalité à long terme de 30% [5].
L'importance de l'IT au jet couleur est diminuée par l'anesthésie et par la modification des conditions de charge pour le VD; elle est un critère moins fiable que les dimensions anatomiques de l'anneau et la position des feuillets en systole [6]. Bien qu'elle ne soit pas une pathologie du cœur droit, l'insuffisance tricuspidienne fonctionnelle aggrave considérablement la situation du VD lorsque celui-ci subit une surcharge de pression, par exemple suite à une hypertension pulmonaire. Elle ajoute une surcharge de volume à la surcharge de pression. Ceci augmente la dilatation du VD, ce qui accroît secondairement l'IT, et le cœur droit entre ainsi dans un cercle vicieux.
La présence d’une IT permet de calculer la PAP systolique par le truchement de l’équation simplifiée de Bernoulli (voir Chapitre 25, Equation de Bernoulli)). Cette équation stipule que le gradient de pression entre deux cavités est égal à 4 fois le carré de la vélocité maximale du flux sanguin entre ces deux cavités: ΔP = 4 (Vmax)2. En systole, la Vmax de l'IT est fonction du ΔP entre le VD et l'OD. En l'absence de pathologie sur la valve pulmonaire (rarissime chez l'adulte), la pression pulmonaire systolique (PAPs) est donc la somme du ΔP VD - OD et de la pression moyenne de l'OD (voir Figure 25.161).
PAPs = (4 • V2IT) + POD
La POD est mesurée par la PVC ou estimée par le degré de collapsibilité de la veine cave inférieure: en hypovolémie, les variations respiratoires du diamètre de la VCI (mesuré en mode TM par voie transgastrique ou sous-xyphoïdienne) sont excessives lorsque le malade est hypovolémique.
- En ETO et sous ventilation contrôlée, une variation de diamètre > 20% entre l'inspirium et l'expirium signe l'hypovolémie;
- En ETT et en respiration spontanée, le seuil pour une hypovolémie est une variation respiratoire > 50%.
- En hypervolémie, la VCI est dilatée (diamètre > 2.5 cm) et ne pulse pas.
Les valeurs de pression correspondantes sont 5 mmHg en hypovolémie, 10 mmHg en normovolémie et 12-15 mmHg en hypervolémie. La corrélation de cette technique de calcul de la PAPsyst avec la valeur réelle mesurée par cathétérisme n'est en moyenne que de 0.7 [11]. L'estimation de la PAPs n'est pas possible en cas d'IT sévère lorsque la Vmax est basse à cause de la grande taille de l'orifice de régurgitation [20]. La présence d'une IT altère la lecture du débit cardiaque par thermodilution au moyen d'un cathéter pulmonaire de Swan-Ganz: la thermodilution sous-estime le débit réel en cas d’insuffisance majeure primaire, mais le surestime lorsque l’IT est due à une défaillance droite [26].
Plastie chirurgicale de l’IT
La présence d’une IT fonctionnelle modérée à sévère péjore le pronostic de toute intervention cardiaque et tend à s’aggraver ultérieurement malgré la correction des valvulopathies gauches [21,23]. De ce fait, les indications à la plastie tricuspidienne simultanée à une intervention en CEC sur le cœur gauche sont devenues plus larges et souvent posées en fonction de l’examen ETO peropératoire [2,5,21,24,28].
Les prédicteurs d'un échec de la plastie lors d'une IT secondaire sont essentiellement les marqueurs d'une dilatation excessive: diamètre diastolique de l'anneau tricuspidien > 4.4 cm, diamètre maximal du VD > 4.9 cm, hauteur de tente > 1.1 cm [7,17].
Plusieurs techniques de correction sont à disposition du chirurgien (voir Figure 11.61) (Vidéos).
Vidéo: vue après plastie tricuspidienne pour rupture traumatique de l'appareil sous-valvulaire du feuillet antérieur. La coaptation est excellente.
Vidéo: minime insuffisance résiduelle après plastie pour un prolapsus du feuillet postérieur.
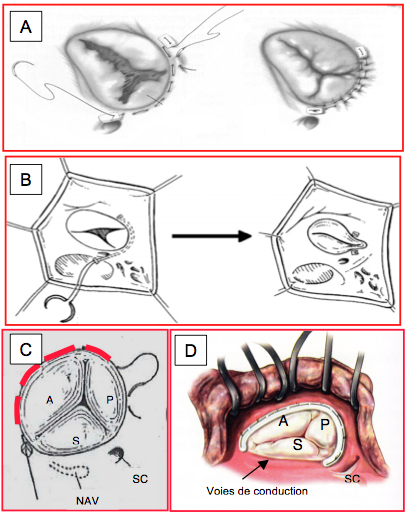
Figure 11.61 : Plastie tricuspidienne vue par une atriotomie de l’OD comme elle se présente dans le champ opératoire. A: annuloplastie postérieure. B: bicuspidalisation selon Kay. C : plastie selon De Vega ; des points coulissants sont disposés sur l’anneau, de la commissure antéro-septale à la commissure postéro-septale ; ils permettent de le rétrécir à volonté en le calibrant avec une jauge 27 [20]. D : anneau prothétique tricuspidien ; il est interrompu au niveau du septum pour éviter de léser les voies de conduction lors de sa mise en place [Savage RM, ed. Intraoperative transesophageal echocardiography. Philadelphia : Lippincott Williams & Wilkins, 2005, 440]. NAV : nœud atrio-ventriculaire. SC : sinus coronaire. A : feuillet antérieur. P : feuillet postérieur. S : feuillet septal.
Les résultats fonctionnels sont meilleurs et la survie à 15 ans doublée avec un anneau flexible par rapport à une plastie selon De Vega [25]. Les critères d’une réussite sont plus souples qu’après une correction mitrale, car une fuite résiduelle est bien tolérée [14,25].
© CHASSOT PG, BETTEX D. Octobre 2011, Juin 2019; dernière mise à jour, Mars 2020
Références
| Insuffisance tricuspidienne |
| IT mineure présente chez 70% des sujets sains Origine organique (feuillets anormaux), ou fonctionnelle (feuillets normaux) due à l’âge, à la surcharge de volume ou de pression, à la dysfonction VD Imagerie bidimensionnelle de l'IT sévère - Non-coaptation des feuillets (écart ≥ 8 mm) - Dilatation OD et VD, bombement du septum interauriculaire dans l’OG - Dilatation et pulsatilité de la VCS, de la VCI et des veines sus-hépatiques Flux Doppler - Etendue du jet couleur IT sévère : > 30% OD - PISA IT sévère : r ≥ 0.9 cm - Vena contracta IT sévère : diamètre ≥ 0.7 cm - Reflux systolique dans VCI et veines sus-hépatiques - Orifice de régurgitation > 0.4 cm2, volume régurgité > 45 mL - La Vmax IT est fonction du ΔP VD – OD, non de la sévérité de l’insuffisance |
| Message pour le chirurgien en cas de pathologie tricuspidienne |
| Description : taille et lésions de chacun des 3 feuillets, restriction ou prolapsus, dégénérescence myxoïde, rupture de cordage, fibrose, degré de coaptation, espacement des feuillets en systole, distance de tente. Dimensions : taille de l’anneau en vue 4-cavités 0° (diamètre septo-latéral) et en vues admission-chasse VD 60° - bicave modifiée 100° (diamètre antéro-postérieur); dimensions de l’OD et du VD, bombement septal vers la gauche. Doppler : nombre, importance et direction des jets d’IT, Vmax IT, PISA et vena contracta, Vmax et ΔP du flux diastolique. |
Plastie chirurgicale de l’IT
La présence d’une IT fonctionnelle modérée à sévère péjore le pronostic de toute intervention cardiaque et tend à s’aggraver ultérieurement malgré la correction des valvulopathies gauches [21,23]. De ce fait, les indications à la plastie tricuspidienne simultanée à une intervention en CEC sur le cœur gauche sont devenues plus larges et souvent posées en fonction de l’examen ETO peropératoire [2,5,21,24,28].
- IT sévère avec dilatation de l'anneau tricuspidien > 4.0 cm en vue 4-cavités en télédiastole (recommandation de classe I);
- Dilatation de l'anneau tricuspidien > 4.0 cm en vue 4-cavités en télédiastole, même si l'IT est seulement modérée (recommandation IIa);
- IT modérée avec hypertension pulmonaire non réversible par la chirurgie sur le cœur gauche (recommandation IIb);
- Absence de coaptation des feuillets (écart ≥ 8 mm);
- Distance de tente > 8 mm et surface de tente > 1.6 cm2.
Les prédicteurs d'un échec de la plastie lors d'une IT secondaire sont essentiellement les marqueurs d'une dilatation excessive: diamètre diastolique de l'anneau tricuspidien > 4.4 cm, diamètre maximal du VD > 4.9 cm, hauteur de tente > 1.1 cm [7,17].
Plusieurs techniques de correction sont à disposition du chirurgien (voir Figure 11.61) (Vidéos).
Vidéo: vue après plastie tricuspidienne pour rupture traumatique de l'appareil sous-valvulaire du feuillet antérieur. La coaptation est excellente.
Vidéo: minime insuffisance résiduelle après plastie pour un prolapsus du feuillet postérieur.
- Annuloplastie par sutures de rétrécissement (plastie selon DeVega);
- Plastie par insertion d'un anneau de Carpentier; cet anneau est interrompu au niveau septal pour éviter les lésions du noeud auriculo-ventriculaire et du faisceau de His;
- Réimplantation de cordages en cas de rupture, résection de prolapsus (IT flail leaflet post col);
- Plastie d'augmentation de feuillets;
- Remplacement de la valve par une prothèse.

Figure 11.61 : Plastie tricuspidienne vue par une atriotomie de l’OD comme elle se présente dans le champ opératoire. A: annuloplastie postérieure. B: bicuspidalisation selon Kay. C : plastie selon De Vega ; des points coulissants sont disposés sur l’anneau, de la commissure antéro-septale à la commissure postéro-septale ; ils permettent de le rétrécir à volonté en le calibrant avec une jauge 27 [20]. D : anneau prothétique tricuspidien ; il est interrompu au niveau du septum pour éviter de léser les voies de conduction lors de sa mise en place [Savage RM, ed. Intraoperative transesophageal echocardiography. Philadelphia : Lippincott Williams & Wilkins, 2005, 440]. NAV : nœud atrio-ventriculaire. SC : sinus coronaire. A : feuillet antérieur. P : feuillet postérieur. S : feuillet septal.
Les résultats fonctionnels sont meilleurs et la survie à 15 ans doublée avec un anneau flexible par rapport à une plastie selon De Vega [25]. Les critères d’une réussite sont plus souples qu’après une correction mitrale, car une fuite résiduelle est bien tolérée [14,25].
- IT résiduelle < modérée (Vidéo) (si > modérée : reprise);
- ΔPmax < 4 mmHg;
- Vena contracta < 0.3 cm;
- Absence de PISA et de reflux systolique dans la VCI et les veines sus-hépatiques.
Vidéo: minime insuffisance résiduelle après plastie tricuspidienne pour RAA.
| Plastie tricuspidienne |
| Indications: - IT primaire modérée à sévère avec symptômes d’insuffisance droite et dilatation du VD - IT fonctionnelle: diamètre de l'anneau > 4 cm si intervention sur les valves gauches Critères de réussite: - IT résiduelle < modérée - Absence de PISA et de reflux systolique en VCI - ΔPmax < 4 mmHg |
© CHASSOT PG, BETTEX D. Octobre 2011, Juin 2019; dernière mise à jour, Mars 2020
Références
- BHATT HV, SPIVACK J, PATEL PR, et al. Correlation of 2-dimensional and 3.dimensional echocardiographic analysis to surgical measurements of the tricuspid valve annular diameter. J Cardiothorac Vacs Anesth 2019; 33:137-45
- BRUCE CJ, CONNOLLY HM. Right-sided valve disease deserves a little more respect. Circulation 2009; 119:2726-34
- CHEN TE, KWON SH, ENRIQUEZ-SARANO M, et al. Three-dimensional color Doppler echocardiographic quantification of tricuspid regurgitation orifice area: comparison with conventional two-dimensional measures. J Am Soc Echocardiogr 2013; 26:1143-52
- CHERRY SV, JAIN P, RODRIGUEZ-BLANCO YF, FABBRO M. Noninvasive evaluation of native valvular regurgitation: a review of the 2017 American Society of Echocardiography Guidelines for the perioperative echocardiographer. J Cardiothorac Vasc Anesth 2018; 32:811-22
- DREYFUS GD, CORBI PJ, CHAN KMJ, et al. Secondary tricuspid regurgitation or dilatation: which should be the criteria for surgical repair ? Ann Thorac Surg 2005; 79:127-32
- DREYFUSS GD, MARTIN RP, CHAN KMJ, et al. Functional tricuspid reguritation. A need to revise our understanding. J Am Coll Cardiol 2015; 65: 2331-6
- FUKUDA S, GILLINOV AM, McCARTHY PM; et al. Determinants of recurrent or residual functional tricuspid regurgitation after tricuspid annuloplasty. Circulation 2006; 114:1582-7
- HAHN RT. State-of-the-art review of echocardiographic imaging in the evaluation and treatment of functional tricuspid regurgitation. Circ Cardiovasc Imaging 2016; 9:e005332
- HAI T, AMADOR Y, MAHMOOD F, et al. Changes in tricuspid annular geometry in patients with functional tricuspid regurgitation. J Cardiothorac Vasc Anesth 2017; 31:2106-14
- HOKE U, AUGER D, THIJSSEN J, et al. Significant lead-induced tricuspid regurgitation is associated with poor prognosis as long.term follow-up. Heart 2014; 100:960-8
- JANDA S, SHAHIIDI N, GIN K, et al. Diagnostic accuracy of echocardiography for pulmonary hypertension: a systematic review and meta-analysis. Heart 2011; 97:612-22
- KIM JB, SPEVACK DM, TUNICK PA, et al. The effect of transvenous pacemaker and implantable cardioverter defibrillator lead placement on tricuspid valve function: an observational study. J Am Soc Echocardiogr 2008; 21:284-7
- KLEIN AL, BURSTOW DJ, TAJIK AJ, et al. Age-related prevalence of valvular regurgitation in normal subjects. A comprehensive color flow examination of 118 volunteers. J Am Soc Echocardiogr 1990; 3:54-63
- KUWAKI K, MORISHITA K, TSUKAMOTO M, ABE T. Tricuspid valve surgery for functional tricuspid valve reguitation associated with left-sided valvular disease. Eur J Cardiothorac Surg 2001; 20:577-82
- LANCELLOTTI P, TRIBOUILLOY C, HAGENDORFF A, et al. Recommendations for the echocardiographic assessment of native valvular regurugitation: an executive summary from the EACI. Eur Heart J Cardiovasc Imaging 2013; 14:611-44
- LANG RM, BADANO LP, TSANG W, et al. EAE/ASE recommendations for image acquisition and display using three-dimensional echocardiography. Eur Heart J Cardiovasc Imaging 2012; 13:1-46
- MASLOW A, ABISSE S, PARIKH L, et al. Echocardiographic predictors of tricuspid ring annuloplasty repair failure for functional tricuspid regurgitation. J Cardiothorac Vasc Anesth 2019; 33:2624-33
- MASLOW A, SCHWARTZ C, SINGH AK. Assessment of the triicuspid valve: a comparison of four transesophageal echocardiographic windows. J Cardiothorac Vasc Anesth 2004; 18:719-24
- MONTEALEGRE-GALLAGOS M, GERMAN R, JIANG L, et al. Tricuspid valve: an intraoperative echocardiographic perspective. J Cardiothorac Vasc Anesth 2014; 28:761-70
- MURARU D, ANWAR AM, SONG JK. Heart valve disease: tricuspid valve disease. In: LANCELOTTI P, ZAMORANO JL, HABIB G, BADANO L. The EACVI Textbook of echocardiography. Oxford: Oxford University Press, 2017, 299-312
- NATH J, FOSTER E, HEIDENREICH PA. Impact of tricuspid regurgitation on long-term survival. J Am Coll Cardiol 2004; 43:405-9
- ROGERS JH, BOLLING SF. The tricuspid valve. Current perspective and evolving management of tricuspid regurgitation. Circulation 2009; 119:2718-25
- SINGH SK, TANG GH, MAGANTI MD, et al. Midterm outcomes of tricuspid valve repair versus replacement for organic tricuspid disease. Ann Thorac Surg 2006; 82:1735-41
- TAMBORINI G, FUSINI L, MURATORI M, et al. Right heart chamber geometry and tricuspid annulus morphology in patients undergoing mitral valve repair with and without tricuspid valve annuloplasty. Int J Cardiovasc Imaging 2016; 32:885-94
- TANG GH, DAVID TE, SINGH SK, et al Tricuspid valve repair with an annuloplasty ring results in improved long-term outcomes. Circulation 2006; 114(suppl I):577-81
- THUNBERG CA, GAITAN BD, GREWAL A, et al. Pulmonary hypertension in patients undergoing cardiac surgery: Pathophysiology, perioperative management, and outcomes. J Cardiothorac Vasc Anesth 2013; 27:551.72
- TRIBOUILLOY C, ENRIQUEZ-SARANO M, BAILEY MR, et al. Quantificatioon of tricuspid regurgitation by measuring the width of the vena contracta with Doppler color flow imaging: a clinical study. J Am Coll Cardiol 2000; 36:472-8
- ZOGHBI WA, ADAMS D, BONOW RO, et al. Recommendations for noninvasive evaluation of native valvular regurgitation: a report from the ASE developped in collaboration with the SCMR. J Am Soc Echocardiogr 2017; 30:303-71
