Le syndrome aortique aigu (SAA) est une entité dans laquelle sont regroupées des affections aortiques potentiellement létales qui nécessitent une prise en charge immédiate intensive, le plus souvent chirurgicale. Elles sont caractérisées par une disruption de la media et une séparation des couches de la paroi aortique par une extravasation sanguine (voir Figure 18.9) [6].
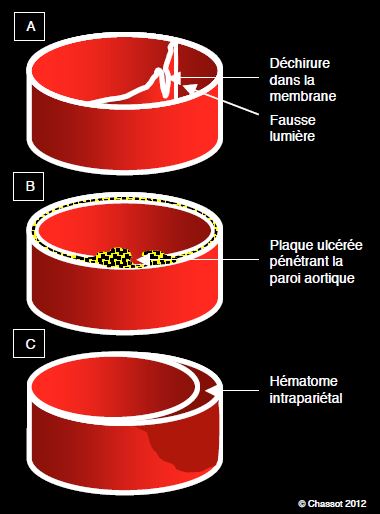
Figure 18.9 : Lésions pariétales aortiques. A : dissection ; une membrane sépare la vraie et la fausse lumières ; l’origine est une déchirure intimale. B : une plaque athéromateuse ulcérée pénètre dans la paroi aortique et érode les couches ; elle peut provoquer une dissection ou une rupture. C : hématome intrapariétal sur rupture de vasa vasorum ; il cause une dissection au sein de la paroi mais sans contact avec le flux sanguin [2].
Une déchirure intimale (dissection), un ulcère térébrant dans une plaque athéromateuse ou une rupture de vasa vasorum (hématome intramural) permettent au sang de s’infiltrer au sein de la media, qui se distend et peut se rompre. Cliniquement, le SAA se manifeste par une douleur soudaine, térébrante et violente, qui peut être thoracique, cervicale, dorsale ou abdominale selon la pathologie. La douleur est souvent accompagnée d’un état de choc et d’une cascade de symptômes : troubles neurologiques transitoires (15-40% des cas), différences de pression entre les membres, ischémie digestive, souffle d’insuffisance aortique, compression d’organes voisins (trachée, bronche souche gauche, œsophage, nerf phrénique, nerf récurent). Certains éléments anamnestiques renforcent la probabilité de SAA: syndrome de Marfan, bicuspidie aortique, chirugie cardiaque préalable, dilatation aortique connue. La mortalité à 30 jours est de 25-50%. Les origines sont diverses [3,5,6].
- Dissection (70% des cas de SAA)10
- Type A: aorte ascendante; mortalité 1-2%/heure; traitement chirurgical (mortalité opératoire 10-25%).
- Type B: aorte descendante; traitement primairement médical (mortalité 9-15%).
- Hématome intramural (10-25% des cas de SAA)
- Rupture de vasa vasorum ; rarement, dissection localisée sans déchirure intimale visible.
- 60% des cas dans l’aorte descendante.
- Risque de rupture : 20-45% si épaisseur de paroi > 16 mm ; régression spontanée : 10%.
- Athérome térébrant (ulcération pénétrante d'une plaque) (2-10% des cas de SAA)
- Plaque athéromateuse bourgeonnante et ulcérée, infiltrant la paroi et provoquant une hémorragie intrapariétale qui conduit à la dissection ou à la rupture.
- Le plus souvent dans l’aorte descendante, accompagné d’une réaction inflammatoire importante.
- Risque de rupture : 38%.
- Indication opératoire (préférence pour une endoprothèse): diamètre > 20 mm et profondeur > 10 mm.
- Rupture traumatique ou iatrogène
- Traumatisme thoracique fermé.
- Canulation aortique de CEC.
- Mandrins ou cathéters intravasculaires, contre-pulsion intra-aortique.
Le SAA est subdivisé en deux types selon la localisation de la pathologie. Cette subdivision est basée sur l'option thérapeutique préférentielle.
- Type A : toutes les affections englobant l’aorte ascendante ; sanction thérapeutique chirurgicale d'urgence.
- Type B : toutes les affections épargnant l’aorte ascendante; la thérapeutique est primairement médicale (β-bloqueur, vasodilatateur, opiacés), la chirurgie étant réservée aux complications (le plus souvent endoprothèse).
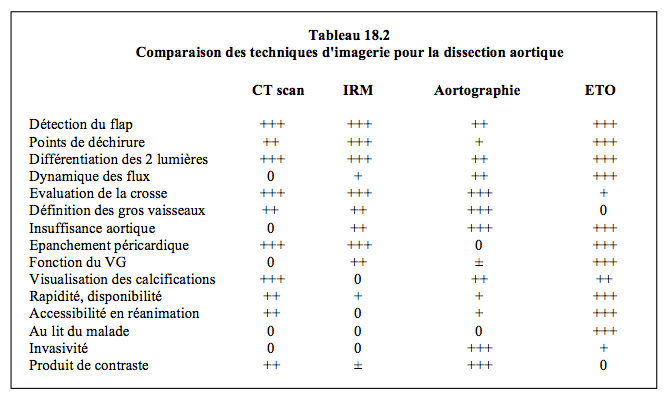
La dissection aortique est la pathologie la plus fréquente (70% des cas). L’insuffisance valvulaire aortique, la tamponnade et l’épanchement pleural sont des complications courantes. Les facteurs de risque principaux sont l’hypertension artérielle, l’athéromatose, le tabagisme, l’abus de stimulants (cocaïne, amphétamines) et l’affaiblissement génétique de la média et des vasa vasorum. Le diagnostic est suspecté par la clinique et par l’élévation des D-dimères (> 500mcg/L, diagnostic différentiel avec l'embolie pulmonaire) et des smMHC (smooth muscle myosin heavy chain, > 10 ng/mL). Il est confirmé par un CT-scan et/ou une échocardiographie transoesophagienne (ETO). L'IRM n'est pas envisageable dans les conditions d'une réanimation mais présente d'excellentes sensibilité et spécificité. L'échocardiographie transthoracique (ETT) est un examen de triage en urgence. Les ultrasons intravasculaires (IVUS) sont très utiles pendant la mise en place d'une endoprothèse parce qu'ils offrent une grande précision dans la localisation des lésions. La radiographie du thorax et l’angiographie ont peu de pertinence (Tableau 18.2) [7,8].
- CT-scan (multibarettes)
- Rapide, très sensible et très spécifique, il diagnostique les principales causes de SAA ; sa résolution spatiale est supérieure à celle de l'IRM.
- Désavantages : déplacement du malade, produit de contraste.
- IRM
- Très sensible et très spécifique, elle diagnostique les principales causes de SAA sans utiliser de produit de contraste ni de radiations ionisantes; idéal pour le suivi.
- Désavantages : lenteur, impossibilité en urgence/réanimation, porteurs de prothèses métalliques exclus, impossibilité de poursuivre la prise en charge invasive pendant l’examen.
- ETO
- Très sensible et très spécifique pour les dissections et les anévrysmes, possible au lit du malade ou dans le déchocage, réanimation possible pendant l’examen; mise en évidence de tamponnade, insuffisance aortique et ischémie myocardique; visualisation des flux à travers les déchirures. Capacité de guidage pour la pose d'endoprothèse et de reconstruction de la valve aortique.
- Désavantages : semi-invasif, non-visibilité de l’aorte ascendante distale et des gros vaisseaux, artéfacts.
- ETT
- Examen de triage simple, rapide, non-invasif et réalisé au lit du malade; met en évidence tamponnade, insuffisance aortique et ischémie myocardique.
- Désavantages: vue de l'aorte limitée à la racine de l'ascendante (voie parasternale long-axe) et à la crosse (vue sus-sternale).
- Rx thorax
- Rapide et simple, mais peu spécifique et très peu sensible; le déplacement d'une sonde gastrique est un signe d'hématome.
- Angiographie
- Sensible et spécifique pour les dissections et les plaques ulcérées, mais non pour les hématomes intramuraux ou les petites déchirures ; la seule indication actuelle est la nécessité éventuelle d'une coronarographie ou d'une angiographie carotidienne.
- Désavantages : déplacement du malade, invasivité, dose élevée de contraste.
- IVUS
- Très précis pour la localisation des lésions en peropératoire (endoprothèse).
- Désavantages: invasif (canulation artérielle) et onéreux.
La prise en charge immédiate du SAA consiste à limiter le stress de paroi sur l’aorte, à assurer la réanimation et à définir au plus vite les options thérapeutiques.
- Baisse du dP/dt par un béta-bloqueur (esmolol, labetalol); doit intervenir avant la vasodilatation artérielle à cause du risque de tachycardie réflexe lors de cette dernière.
- Baisse de la pression artérielle avec un vasodilatateur systémique (nitroprussiate, clevidipine).
- Analgésie (opioïdes), sédation, éventuellement anesthésie et intubation.
- Réanimation liquidienne, transfusions et facteurs de coagulation selon besoins.
D’une manière générale, les lésions de l’aorte ascendante sont une indication à la chirurgie d’emblée : excision de la déchirure d’entrée, remplacement de l’aorte ascendante par une prothèse tubulaire et matelassage de la dissection distale, accompagnée ou non d’intervention sur la valve aortique (plastie, resuspension, prothèse), éventuellement opération hybride (voir Opérations hybrides). La mortalité opératoire oscille entre 10% et 15% [3,6].
Les lésions de l’aorte descendante font l’objet d’un traitement médical, sauf en cas de complications : dissection progressive, menace de rupture, expansion de > 1 cm/an, diamètre > 5.5 cm, ischémie viscérale, paraplégie, douleur persistante, hypertension réfractaire. Dans les dissections de type B, la mortalité opératoire est de 18% pour la chirurgie à ciel ouvert, de 7% pour l’endoprothèse et de 6% pour le traitement médical seul [1,4,9]. Malheureusement, on ne dispose d’aucune donnée sur le devenir à long-terme des endoprothèses.
Les athéromes térébrants et les hématomes intramuraux sont des indications à une intervention chirurgicale d’urgence lorsqu’ils sont situés dans l’aorte ascendante (type A), mais à un traitement médical suivi ou non d’une endoprothèse lorsqu’ils sont localisés dans la descendante (type B) [5,6].
| Syndrome aortique aigu |
|
Affections qui consistent en une dilacération intrapariétale de l'aorte et qui réclament un traitement immédiat, le plus souvent chirurgical. Comprend:
- Dissection
- Hématome intramural
- Athérome térébrant
- Rupture traumatique
Prise en charge:
- Baisse du dP/dt
- Hypotension contrôlée
- Réanimation liquidienne
Traitement prioritaire:
- Lésions de l'aorte ascendante (type A): option chirurgicale
- Lésions de l'aorte descendante (type B): traitement médical, chirurgie en cas de
complications
Examens de choix: CT-scan, ETO, IRM (impossible lors de réanimation)
|
© CHASSOT PG, TOZZI P, BETTEX D, Octobre 2010, Dernière mise à jour, Avril 2018
Références
- ARAUJO PV, JOVILIANO EE, RIBEIRO MS, et al. Endovascular treatment of acute aortic syndrome. Ann Vasc Surg 2012; 26:516-20
- COADY MA, IKONOMIDIS JS, CHEUNG AT, et al. Surgical management of descending thoracic aortic disease: open and endovascular approaches. Circulation 2010; 121:2780-804
- ERBEL R, ABOYANS V, BOILEAU C, et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases. Eur Heart J 2014; 35:2873-926
- FATTORI R, CAO P, DE RANGO P, et al. Interdisciplinary expert consensus document on management of type B aortic dissection. J Am Coll Cardiol 2013; 61:1661-78
- LANSMAN SL, SAUNDERS PC, MALEKAN RE, et al. Acute aortic syndome. J Thorac Cardiovasc Surg 2010; 140:S92-7
- NIENABER CA, POWELL JT. Management of acute aortic syndromes. Eur Heart J 2012; 33:26-35
- NIENABER CA. The role of imaging in acute aortic syndromes. Eur Heart J Cardiovasc Imag 2013; 14:15-23
- NOWAK-MACHEN M. The role of transesophageal echocardiography in aortic surgery. Best Pract Res Clin Anaesthesiol 2016; 30:317-29
- OLSSON C, THELIN S, STAHLE E, et al. Thoracic aortic aneurym and dissection: increasing prevalence and improved outcomes reported in a nation-wide population-based study of more then 14000 cases from 1987 to 2002. Circulation 2006; 114:2611-8
