Si la transfusion sanguine présente tant de risques, on est en droit de se poser la question dans l'autre sens: l'anémie est-elle dangereuse ? Autrement dit, quelle est la valeur minimale d'Hb que l'on peut tolérer sans risque ? On peut aborder ce problème sous trois angles différents: la tolérance à l'anémie du sujet sain, le risque clinique associé à l'anémie en périopératoire, et la sensibilité à l'anémie d'organes particulièrement fragiles comme le coeur ou le cerveau.
Chez l'animal, l'augmentation de l'extraction d'O2 et du débit cardiaque permettent de maintenir la consommation d'O2 (VO2) normale jusqu'à un taux d'Hb de 45 g/L [14,38]. Chez le volontaire sain, une diminution de moitié du transport d'O2 (7.3 ml/kg/min au lieu de 14 ml/kg/min) n'entraîne aucun signe d'inadéquation de l'oxygénation périphérique; ceci peut être aisément réalisé avec un Ht de 20% (Hb 70 g/L) et un débit cardiaque encore normal [23]. En peropératoire, la curarisation permet de diminuer encore la consommation d'O2 d'environ 10-30%, ce qui se traduit par une élévation de la SvO2 de 5-10% [13]. De ce point de vue, on peut accepter un Ht de 20% et une Hb de 60 g/L en peropératoire chez un individu sans comorbidités qui ne saigne pas activement. La limite inférieure tolérable sans conversion à un métabolisme anaérobique peut être définie par les critères suivants [33] :
- Ht : 20%;
- Hb : 60 g/L;
- PvO2 : 32 mmHg, SvO2 : 50%;
- Coefficient d'extraction d'O2 : 50%;
- Consommation d'O2 à 50% de sa valeur de base.
Les patients qui refusent les transfusions pour des motifs religieux ont souvent des valeurs d'Hb très basses dans le postopératoire. En analysant 300 d'entre eux qui avaient des valeurs d'Hb en dessous de 80 g/L, on voit que la mortalité est de 0% et la morbidité de 9% lorsque l'Hb la plus basse enregistrée est située entre 70 et 80 g/L; lorsque l'Hb est entre 40 et 50 g/L, la mortalité est de 34% et la morbidité de 58%; la mortalité est de 100% en dessous de 25 g/L [3]. Après ajustement pour l'âge et le score APACHE, le risque de mort augmente par un facteur de 2.5 pour chaque 10 g/L d'Hb en dessous de 60 g/L. La même analyse réalisée 12 ans plus tard sur un collectif de 293 patients montre une courbe analogue mais décalée vers une meilleure survie, avec un risque de mortalité qui augmente par un facteur de 2.04 par 10 g/L Hb en dessous de 60 g/L [28]; la différence tient au développement d'une multimodulaire gestion de l'épargne sanguine (voir Stratégies globales). Ces données concernent des malades qui ne souffrent pas de cardiopathie et ont une tolérance à l'effort considérée comme normale (Figure 28.8).
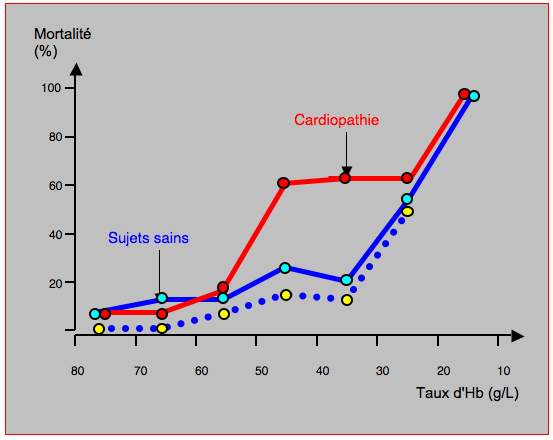

Figure 28.8 : Mortalité en fonction du degré d'anémie postopératoire (taux d’Hb dégressifs) dans deux études portant sur des patients refusant toute transfusion [3,28]. Trait bleu [3] et pointillé bleu [28]: sujets sains. Trait rouge: sujets souffrant de cardiopathies [3]. La mortalité augmente significativement en dessous de 40 g/L chez les sujets sains, et en dessous de 60 g/L chez les patients en insuffisance cardiaque. Elle s’élève à 100% en dessous de 20 g/L.
Un seuil de transfusion à un taux d'Hb de 60 g/L est donc logique dans cette situation. Toutefois, trois organes sensibles à l'ischémie - le coeur, le cerveau et les reins - doivent faire tempérer cette conclusion. En effet, la résistance globale de l'organisme à l'anémie est définie par celle de ses organes qui sont les plus dépendants du transport d'O2. Or une pathologie liée à ces organes peut modifier les seuils de transfusion recommandés.
Anémie et cardiopathies
Les besoins du coeur, dont le coefficient d'extraction d'O2 voisine 60-70%, varient selon l'effort qui lui est demandé et selon son état fonctionnel. D'autre part, son apport en O2 varie selon le degré de sténose coronarienne. Lorsque le contenu en O2 diminue, le flux coronarien augmente pour maintenir le DO2 constant, pour autant que la réserve coronarienne soit satisfaisante et que l'accélération de la fréquence ne soit pas exagérée. Sur un collectif de 55 volontaires sains hémodilués en normovolémie jusqu'à une Hb de 50 g/L, par exemple, 3 sujets ont développé des sous-décalages transitoires du segment ST; ils présentaient une augmentation de fréquence cardiaque très supérieure à celle des autres sujets (133% versus 43%) [22].
Les patients souffrant de cardiopathies sont plus sensibles à l'anémie que les individus sains, et leur survie est en général significativement améliorée par l'élévation du contenu sanguin en oxygène. Dans l'étude sur des malades anémiques non transfusés dans le postopératoire, on voit que la brusque augmentation de mortalité, qui a lieu en dessous de 40 g/L d'Hb chez les sujets sains, survient déjà lorsque l'Hb passe la barre de 60 g/L chez les malades souffrant de cardiopathies (Figure 28.8) [3]. En chirurgie cardiaque, la valeur de l'hématocrite le plus bas enregistré au cours de l'opération est associée à une augmentation de la mortalité hospitalière, mais seulement lorsque cet hématocrite est inférieur à 23% [4]: alors qu'elle est de 1.5% à un Ht de 23%, la mortalité double à un Ht de 21%, et passe à 4.5% lorsque l'Ht est inférieur à 19%. Trois études cliniques ont démontré un taux d'évènements ischémiques plus élevé chez les malades dont l'Ht était inférieur à 25-28% par rapport à ceux qui étaient supérieurs à cette valeur [11,12,26]. Le risque de mortalité postopératoire est multiplié par 4 et par 10 lorsque le taux d'Hb préopératoire est respectivement de 90 et de 70 g/L chez des malades en insuffisance cardiaque [2]. En chirurgie coronarienne, l’anémie préopératoire (Hb < 100 g/L) est un facteur de risque indépendant pour les complications postopératoires cardiaques, rénales et cérébrales (odds ratio 1.71-2.0) [17,20]. Le taux d’hémorragie, de complications pulmonaires et d’infections augmente respectivement de 4 fois (OR 4.37), de 3 fois (OR 2.85) et de 2 fois (OR 1.84) lorsque l’Ht est < 22% [11].
On retrouve cette association entre anémie et morbi-mortalité lors de cardiopathie en-dehors du contexte chirurgical. La survie, la fonction ventriculaire et la fonction rénale sont améliorées chez les patients en insuffisance cardiaque stade NYHA III-IV dont l'Hb est maintenue au-dessus de 125 g/L par l'administration d'EPO [30]. Après infarctus du myocarde chez des malades âgés de plus de 65 ans, la survie est meilleure lorsque l'Ht est supérieur à 30% [44]; dans cette série, la survie est améliorée dans le groupe transfusé lorsque l'Ht est inférieur à 30%, mais diminuée si l'Ht est supérieur à 36%. Cependant, une réduction du taux d'Hb à environ 100 g/L au cours d'une hémodilution aiguë est parfaitement tolérée par des malades ischémiques, valvulaires ou âgés [34,35]. Dans ces situations, toute modification du segment ST (sous-décalage > 0.1 mV ou sus-décalage > 0.2 mV) en cours de spoliation sanguine doit inciter à transfuser des érythrocytes. On peut donc conclure qu'un seuil de transfusion situé entre 80 et 90 g/L d'Hb est sûr chez les patients souffrant de cardiopathies.
Anémie et fonction cérébrale
Les besoins en O2 du cerveau sont couverts avec une Hb aussi basse que 40 g/L, car ce dernier est capable d'augmenter son flux sanguin jusqu'à 500% et son coefficient d'extraction jusqu'à 50% pour compenser la chute du CaO2 [36]. Il n'y a aucune altération des fonctions cognitives fine pour une Hb de 60 g/L, mais des altérations mnémotechniques subtiles et réversibles surviennent en dessous de cette valeur, sans qu'apparaisse pour autant une modification du status neurologique [41,42]. En chirurgie cardiaque, augmenter l'Ht au-dessus de 25% n'améliore ni l'oxygénation cérébrale ni les risques neurologiques postopératoires [39]. Le degré d'anémie peropératoire n'est pas associé à l'incidence des AVC postopératoires [38,39]. Par contre, le taux d’AVC postopératoire s'aggrave linéairement lorsque l'Ht peropératoire le plus bas est < 24% ; chaque 1% de diminution de l’Ht augmente le risque d’ictus de 10% [16]. Les tissus situés dans la zone de pénombre qui borde la zone ischémique lors d'AVC ou de traumatisme crânien peuvent bénéficier d'un meilleur apport d'O2 sous forme dissoute lorsque la FiO2 est de 1.0 [8]. La régulation du flux sanguin cérébral par la PaCO2 a plus d'importance que le taux d'Hb dans l'oxygénation cérébrale lorsque ce dernier est supérieur à 70 g/L [27]. Comme le métabolisme est diminué sous anesthésie, une Hb de 60 g/L est donc parfaitement satisfaisante pour les besoins cérébraux en peropératoire si la volémie et la pression sont maintenues.
Anémie et fonction rénale
La médullaire rénale fonctionne normalement à des PitO2 voisines de la valeur critique; le rein est donc un organe très sensible aux variations de DO2. Lors de pontages aorto-coronariens en CEC, il existe une relation directe entre l'Ht le plus bas en peropératoire et la créatininémie la plus élevée en postopératoire; cette dernière augmente de 40% lorsque l'Ht peropératoire est inférieur à 15%, alors qu'elle ne monte que de 20% lorsque l'Ht est entre 25 et 30% [37]. Une étude portant sur 1'760 patients ayant subi des pontages aorto-coronariens a mis en évidence un phénomène paradoxal [10]: la fonction rénale et le taux d'insuffisance rénale postopératoires s'aggravent linéairement lorsque l'Ht le plus bas est inférieur à 24%, et la mortalité s'accroît de manière directement liée à l'importance de la lésion rénale. Mais, à valeur similaire d'Ht, les patients transfusés présentent systématiquement une péjoration de leur fonction rénale par rapport à ceux qui ne sont pas transfusés; leur mortalité est plus élevée (3.8% versus 1.4%) et leur incidence d'insuffisance rénale plus importante (12% versus 3.4%) (Figure 28.9) [10]. On est donc placé devant un dilemme troublant: l'anémie aggrave la situation, mais la transfusion, au lieu de la corriger, ajoute un facteur délétère supplémentaire [29].
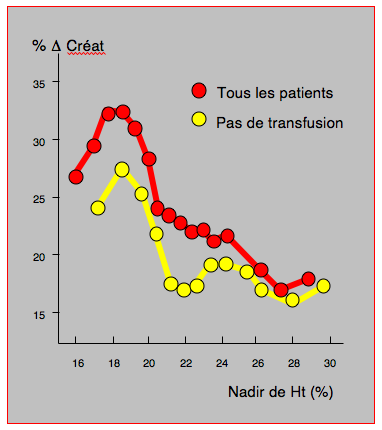

Figure 28.9 : Variation de la créatinine postopératoire en fonction de l'Ht le plus bas. La fonction rénale et le taux d'insuffisance rénale postopératoires s'aggravent linéairement lorsque l'Ht le plus bas est inférieur à 24%. Mais, à valeur similaire d'Ht, les patients transfusés présentent systématiquement une péjoration de leur fonction rénale par rapport à ceux qui ne sont pas transfusés [10].
Anémie et volémie
Ces données sont valables dans les situations hémodynamiquement stables à volémie normale, car on n'a parlé jusqu'ici que d'anémie normovolémique. Il n'en va pas de même dans les situations instables de choc hémorragique avec pertes sanguines profuses (voir Transfusion massive). Dans cette situation, où les critères principaux sont l'hémodynamique du patient et son degré d'acidose, les concentrés érythrocytaires agissent comme un excellent expandeur de volume en plus de leur fonction de transporteurs d'oxygène [32]. Il est essentiel de ne pas prendre du retard sur les transfusions, quelle que soit la valeur de l'Hb pour autant qu'elle reste entre 60 et 80 g/L. Même sans avoir affaire à une hémorragie massive, la perte continue de sang en peropératoire ou après l'intervention commande l'administration d'érythrocytes avant que le seuil théorique ne soit atteint.
Compensations
Lorsqu'il doit fonctionner avec une insuffisance de son transporteur d'O2, l'organisme adopte un certain nombre de mesures compensatrices pour maintenir un DO2 suffisant aux cellules [5].
- Augmentation du débit cardiaque.
- Vasodilatation microcirculatoire (production accrue de NO).
- Maintien de la normovolémie par hémodilution; la baisse de viscosité du sang améliore le retour veineux et abaisse la postcharge; le volume systolique augmente.
- Augmentation de la ventilation-minute.
- Déplacement de la courbe de dissociation de l'Hb vers la droite.
- Augmentation de l'extraction tissulaire d'O2.
- Production rénale d'érythropoïétine.
L’anémie préopératoire est beaucoup plus fréquente qu’on ne l’imagine. Son incidence se situe entre 20 et 45% des patients [1,17,20,25,29,31]. Les seuils définissant l’anémie sont [9] :
- Hb < 130 g/L (Ht < 39%) chez l’homme.
- Hb < 120 g/L (Ht < 36%) chez la femme ; ceci ne tient pas compte du fait que le volume circulant de la femme est plus faible que celui de l’homme à poids corporel égal ; la même hémorragie représente donc une perte plus importante en pourcentage du volume sanguin [23].
- Anémie modérée-à-sévère : Hb < 90 g/L (Ht < 29%) (femme ou homme).
En chirurgie non-cardiaque, la mortalité et la morbidité à 30 jours augmentent de 40% chez les patients anémiques en préopératoire (OR 1.42-1.44 et OR 1.35-1.56, respectivement) [25] ; même mineure (Hb 90-130 g/L), l’anémie entraîne un risque significatif (+ 40%). Dans une cohorte de 39'309 patients européens, la présence d’une anémie modérée ou d’une anémie sévère multiplie la mortalité hospitalière par un facteur de 2 (OR 1.99) et de presque 3 (OR 2.82), respectivement [1]. En peropératoire, 45% des patients sont transfusés uniquement parce que leur Hb préopératoire est trop basse [31]. Or, des études comparatives ont démontré que même une seule poche de sang suffit à augmenter significativement les risques de mortalité et de complications postopératoires par rapport à ceux de patients appariés non-transfusés [7,21,43]. Même si la chirurgie est destinée à en éliminer la cause, l’anémie doit être corrigée avant l’opération car le pronostic global en est amélioré [24].
En chirurgie cardiaque, une anémie préopératoire est décelable dans 31% des cas, et sa présence entraîne également une aggravation de la mortalité (OR 1.42) [2,19]. Celle-ci s'élève de 16% par 10 g/L de baisse dans la concentration d'Hb [19]. En chirurgie coronarienne, l’anémie préopératoire (Hb < 100 g/L) est un facteur de risque indépendant pour les transfusions (OR 2.75) et pour les complications postopératoires cardiaques, rénales ou cérébrales (OR 1.71-2.0) [17,19,20]. Le taux d’hémorragie, de complications pulmonaires et d’infections augmente respectivement de 4 fois (OR 4.37), de 3 fois (OR 2.85) et de 2 fois (OR 1.84) lorsque l’Ht est < 22% [11]. Les patients anémiques ont une plus grande susceptibilité pour l’insuffisance rénale postopératoire que ceux qui ont une Hb normale avant l’opération (incidence 4.1% versus 1.6%), mais ils sont aussi deux fois plus enclins à développer une insuffisance rénale secondaire aux transfusions (6.6% versus 3.2%) [18].
Il est donc totalement illogique que des patients se présentent en salle d'opération pour une intervention élective avec une Hb inférieure à la norme, alors que la correction de leur anémie en préopératoire aurait amélioré leur pronostic et prévenu l'administration de sang. L'anémie doit être considérée comme une contre-indication à une chirurgie majeure élective [5]. Qu’elle soit effectuée par un généraliste, par un anesthésiste ou par le chirurgien, une consultation préopératoire 3-4 semaines avant l’intervention laisse amplement le temps d’investiguer et de corriger le défaut en globules rouges (voir Phase préopératoire) [9].
| Risques lié à l’anémie |
|
La limite inférieure du taux d’Hb tolérable par un individu sain sans souffrance tissulaire ni acidose ni dysfonction organique est 60 g/L (Ht 20%).
En chirurgie cardiaque, la mortalité augmente lorsque l’Hb minimale peropératoire est < 55 g/L ou l’Hb préopératoire < 90 g/L. Chez les patients à risque (cardiopathie ischémique, néphropathie, AVC, âge avancé), la limite inférieure de l’Hb tolérable sans signes de souffrance organique est de 80-90 g/L. L'Ht le plus bas en CEC ne doit pas descendre en-dessous de 22-25% sans quoi le taux de complications augmente.
L’anémie préopératoire (Hb < 130 g/L) est dangereuse car doublement pénalisante :
- Elle augmente la morbidité et la mortalité postopératoires proportionnellement à son importance
- Elle augmente les chances d’être transfusé, donc de subir une aggravation supplémentaire de morbi-mortalité
|
Anémie et transfusion : risques cumulés
Partir en salle d’opération avec un déficit en globules rouges augmente inévitablement le risque d’être transfusé. Bien qu’elle corrige le transport d’oxygène, la transfusion comporte ses propres problèmes et sa propre morbi-mortalité. De ce fait, le bilan n’est pas nul, mais doublement négatif : les risques de la transfusion s’additionnent à ceux de l’anémie. Plusieurs études démontrent ce point.
- La mortalité et l’insuffisance rénale postopératoire augmentent linéairement avec la profondeur de l’anémie. Mais, à valeur similaire d'Ht, les patients transfusés présentent systématiquement une péjoration de leur fonction rénale par rapport à ceux qui ne le sont pas; leur mortalité est plus élevée (3.8% versus 1.4%) et leur incidence d'insuffisance rénale plus importante (12% versus 3.4%) (Figure 28.9) [10].
- Chez les patients en insuffisance cardiaque, l’anémie et l’insuffisance rénale sont associées à une péjoration du pronostic clinique (OR 1.12 et 2.54, respectivement) ; mais l’administration de globules rouges dans ce contexte fait plus que tripler la mortalité (OR 3.81) [15].
- La mortalité après pontages aorto-coronariens est triplée (HR 2.92) chez les patients anémiques et transfusés par rapport à ceux qui ne sont ni anémiques ni transfusés, mais seulement doublée (HR 2.08) chez ceux qui sont anémiques mais non transfusés ou transfusés mais non anémiques [6].
- La mortalité à 3 ans présente un risque cumulé lié à la transfusion (HR 1.34) et à l'anémie (anémie modérée HR 1.44, sévère HR 1.80) [40].
Ainsi, l'anémie est un facteur de risque, mais la transfusion également. Et les deux se potentialisent. Il faut donc trouver un point d’équilibre entre les dangers de chacun des deux termes. Graphiquement, ce point est au nadir d’une courbe en "U" obtenue en superposant celles des deux effets (Figure 28.10).
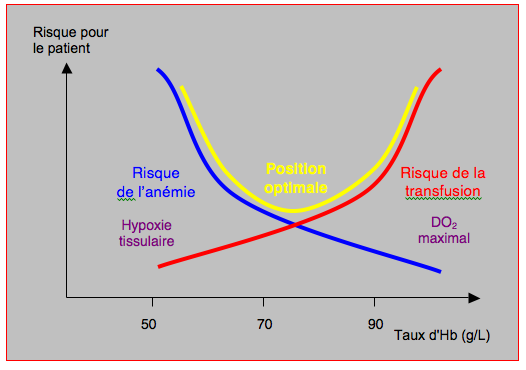

Figure 28.10 : L’aggravation de l’anémie (courbe bleue) s’accompagne d’un risque progressif d’hypoxie tissulaire, qui est certaine < 50 g/L d’Hb; elle entraîne une dysfonction multi-organique. Mais la correction de l’anémie par la transfusion comporte ses propres risques de morbi-mortalité (courbe rouge). L’impact de ces deux risques pour le patient peut se représenter sous la forme d’une courbe en "U" (courbe jaune). La position optimale n’est pas l’équivalent de l’Hb maximale.
Pour se maintenir à ce point, il est capital d’avoir des réserves suffisantes et de perdre le moins possible de globules rouges. Il s'agit en fait d'augmenter et de conserver la masse sanguine propre du patient au lieu de lui administrer du sang étranger (voir Stratégies globales de la gestion du sang).
| Anémie et transfusion |
| L’anémie augmente le risque opératoire proportionnellement à sa profondeur, mais sa correction par la transfusion de concentrés érythrocytaires péjore le pronostic au lieu de l’améliorer, même si elle corrige la valeur de l’hémoglobine (anaemia is bad, transfusion is worse). Les patients ne bénéficient vraiment de la transfusion que lorsqu’ils sont sévèrement anémiques (Hb < 70 g/L) ou hémodynamiquement instables. L'évidence démontre que le sang autologue est un bien précieux que le patient doit conserver, ou régénérer s'il est anémique; elle démontre aussi que la transfusion de sang allologue est le plus mauvais moyen de corriger une anémie, sauf en situation aiguë. |
© CHASSOT PG, MARCUCCI C, SPAHN DR. Juin 2011; dernière mise à jour, Décembre 2019
Références
- BARON DM, HOCHRIESER H, POSCH M, et al. Preoperative anaemia is associated with poor clinical outcome in non-cardiac surgery patients. Br J Anaesth 2014; 113:416-23
- CARSON JL, DUFF A, POSES RM, et al. Effect of anaemia and cardiovascular disease on surgical mortality and morbidity. Lancet 1996; 348:1055-60
- CARSON JL, NOVECK H, BERLIN JA, GOULD SA. Mortality and morbidity in patients with very low postoperative Hb levels who decline blood transfusion. Transfusion 2002; 42:812-8
- DEFOE GR, ROSS CS, OLMSTEAD EM, et al. Northern New England Cardiovascular Disease Study group: Lowest hematocrit on bypass and adverse outcomes associated with coronary artery bypass grafting. Ann Thorac Surg 2001; 71:769-76
- DHIR A, TEMPE DK. Anemia and patient blood management in cardiac surgery – Literature review and current evidence. J Cardiothorac Vasc Anesth 2018; 32:2726-42
- ENGOREN M, SCHWANN TA, HABIB RH, et al. The independent effects of anemia and transfusion on mortality after coronary artery bypass. Ann Thorac Surg 2014; 97:514-21
- FERRARIS VA, DAVENPORT DL, SAHA SP, et al. Surgical outcomes and transfusion of minimal amounts of blood in the operating room. Arch Surg 2012; 147:49-55
- FLYNN EP, AUER RN. Eubaric hyperoxemia and experimental cerebral infarction. Ann Neurol 2002; 52:566-72
- GOODNOUGH LT, MANIATIS A, EARNSHAW P, et al. Detection, evaluation, and management of preoperative anaemia in the elective orthopaedic surgical patient: NATA guidelines. Br J Anaesth 2011; 105:13-22
- HABIB RH, ZACHARIAS A, SCHWANN TA, et al. Role of hemodilutional anemia and transfusion during cardiopulmonary bypass in renal injury after coronary revascularization: Implications on operative outcome. Crit Care Med 2005; 33:1749-56
- HANNAN EL, SAMADASHVILI Z, LAHEY SS, et al. Predictors of postoperative hematocrit and association of hematocrit with adverse outcomes for coronary artery bypass graft surgery patients with cardioplmonary bypass. J Card Surg 2010 ; 25 :638-46
- HOGUE CW, GOODNOUGH LT, MONK TG. Perioperative myocardial ischemic episodes are related to hematocrit level in patients undergoing radical prostatectomy. Transfusion 1998; 38:924-31
- IRISH CL, MURKIN JM, CLELAND A, et al. Neuromuscular blocked significantly decreases systemic oxygen consumption during hypothermic cardiopulmonary bypass. J Cardiothorac Vasc Anesth 1991; 5:132-4
- JAMNICKI M, KOCIAN R, VAN DER LINDEN P, ZAUGG M, SPAHN DR. Acute normovolemic hemodilution: Physiology, limitations and clinical use. J Cardiothorac Vasc Anesth 2003; 17:747-54
- KAO DP, KRESO E, FONAROW GC, et al. Characteristics and outcomes among heart failure patients with anemia and renal insuficiency with and without blood transfusions. Am J Cardiol 2011; 107:69-73
- KARKOUTI K, DJAIANI G, BORGER MA, et al. Low hematocrit during cardiopulmonary bypass is associated with increased risk of perioperative stroke in cardiac surgery. Ann Thorac Surg 2005; 80:1381-7
- KARKOUTI K, WIJEYSUNDERA DN, BEATTIE S, et al. Risk associated with preoperative anaemia in cardiac surgery. A multicenter cohort study. Circulation 2008; 117:478-84
- KARKOUTI K, WIJEYSUNDERA DN, YAU TM, et al. Influence of erythrocyte transfusion on the risk of acute kidney injury after cardiac surgery differs in anemic and nonanemic patients. Anesthesiology 2011; 115:523-30
- KLEIN AA, COLLIER TJ, BRAR MS, et al. The incidence and importance of anaemia in patients undergoing cardiac surgery in the UK: the first Association of Cardiothoracic Anaesthetists national audit. Anaesthesia 2016; 71:627-35
- KULIER A, LEVIN J, MOSER R, et al. Impact of preoperative anemia on outcome in patients undergoing coronary artery bypass surgery. Circulation 2007; 116:471-9
- LEAL-NOVAL SR, MUÑOZ-GOMEZ M, JUMENEZ-SANCHEZ M, et al. Red blood cell transfusion in non-bleeding critically ill patients with moderate anemia: is there a benefit ? Intensive Care Med 2013; 39:45-53
- LEUNG JM, WEIKOPF RB, FEINER J, et al. Electrocardiographic ST-segment changes during acute, severe isovolemic hemodilution in humans. Anesthesiology 2000; 93:1004-10
- LIEBERMAN JA, WEISKOPF RB, KELLEY SD, et al. Critical oxygen delivery in conscious humans is less than 7.3 ml O2 x kg-1 x min-1. Anesthesiology 2000; 92:407-13
- MUÑOZ M, GOMEZ-RAMIREZ S, KOZEK-LANGENEKER S, et al. “Fit-to-fly”: overcoming barriers to preoperative haemoglobin optimization in surgical patients. Br J Anaesth 2015; 115:15-24
- MUSALLAM KM, TAMIM HM, RICHARDS T, et al. Preoperative anaemia and postoperative outcomes in non-cardiac surgery: a retrospective cohort study. Lancet 2011; 378:1396-407
- NELSON AH, FLEISHER LA, ROSENBAUM SH. Relationship between postoperative anemia and cardiac morbidity in high-risk vascular patients in the intensive care unit. Crit Care Med 1993; 21:860-6
- RUCKER J, TESLER J, FEDORKO L, et al. Normocapnia improves cerebral oxygen delivery during conventional oxygen therapy in carbon-monoxyde exposed research subjects. Ann Emerg Med 2002; 40:611-8
- SHANDER A, JAVIDROOZI M, NAQVI S, et al. An update on mortality and morbidity in patients with very low postoperative hemoglobin levels who decline blood transfusion. Transfusion 2014; 54:2688-95
- SHANDER A, JAVIDROOZI M, OZAWA S, HARE GMT. What is really dangerous: anaemia or transfusion ? Br J Anaesth 2011; 107(S1):i41-i59
- SILVERBERG DS, WEXLER D, SHEPS D, et al. The effect of correction in mild anemia in severe, resistant congestive heart failure using subcutaneous erythropoietin and intravenous iron: A randomized controlled study. J Am Coll Cardiol 2001; 37:1775-80
- SPAHN DR. Anemia and patient blood management in hip and knee surgery. A systematic review analysis. Anesthesiology 2010; 113:482-95
- SPAHN DR, BOUILLON B, CERNY V, et al. Management of bleeding and coagulopathy following major trauma: an updated European guideline. Crit Care 2013; 17:R76
- SPAHN DR, DETTORI N, KOCIAN R, CHASSOT PG. Transfusion in the cardiac patient. Crit Care Clin 2004; 20:269-79
- SPAHN DR, SEIFERT B, PASCH T, SCHMID ER. Haemodilution tolerance in patients with mitral valve regurgitation. Anesthesia 1998; 53:20-4
- SPAHN DR, ZOLLINGER A, SCHLUMPF RB, et al. Hemodilution tolerance in elderly patients without known cardiac disease. Anesth Analg 1996; 82:681-6
- SUNGURTEKIN H, COOK DJ, ORSZULAK TA, et al. Cerebral response to hemodilution during hypothermic cardiopulmonary bypass in adults. Anesth Analg 1999; 89:1078-83
- SWAMINATHAN M, PHILIPS-BUTE BG, CONLON PJ, et al. The association of lowest hematocrit during cardiopulmonary bypass with acute renal injury after coronary artery bypass surgery. Ann Thorac Surg 2003; 76:784-91
- VAN DER LINDEN P, DE HERT S, MATHIREU N, et al. Tolerance of acute isovolemic hemodilution: Effect of anesthetic depth. Anesthesiology 2003; 99:97-104
- VAN WERMESKERKEN GK, LARDENOYE JW, HILL SE, et al. Intraoperative physiologic variables and outcome in cardiac surgery: Part II. Neurologic outcome. Ann Thorac Surg 2000; 69:1077-83
- VON HEYMANN C, KAUFNER L, SANDER M, et al. Does the severity of preoperative anemia or blood transfusion have a stronger impact on long-term survival after cardiac surgery? J Thorac Cardiovasc Surg 2016; 152:1412-20
- WEISKOPF RB, KRAMER JH, VIELE MK, et al. Acute severe isovolemic anemia impairs cognitive function and memory in humans. Anesthesiology 2000; 92:1646-52
- WEISKOPF RB, FEINER J, VIELE MK, et al. Oxygen reverses deficits of cognitive function and memory and increased heart rate induced by acute severe isovolemic anemia. Anesthesiology 2002; 96:871-7
- WHITLOCK EL, KIM H, AUERBACH AD. Harms associated with single unit perioperative transfusion: retrospective population-based analysis. BMJ 2015; 350: h3037
- WU WC, RATHORE SS, WANG Y, et al. Blood transfusion in elderly patients with acute myocardial infarction. N Engl J Med 2001; 345:1230-6
